综合实验题的特点与解法
时间:2020-03-07 11:26 来源:未知 作者:张劲辉 点击: 次 所属专题: 综合实验题
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
综合实验题就是给出整套实验装置图并就物质在各部分装置中发生的反应、仪器的功用、实验操作等方面提出问题要求作答的试题。
综合实验题既能考察学生在中学阶段动手实验的情况,又能考察学生的基本实验操作技能,还能考察学生设计实验、探究性质、分析处理数据、得出结论、准确表述实验过程和结论的探究性学习能力。因此,综合实验题一直以来是再现率较高、权重较大的高考题型,在近几年新课程高考中,更是频繁出现,而且融化工流程、表格数据分析和图像表达于一体,呈现出新特点。
本文从题目所涉及的内容,把综合实验题分为探究物质性质型、设计实验方案制备和检验物质型、定性和定量结合分析型、探究反应原理型四类,并就每类题型举例说明其特点和解法,希望对高考复习起指导作用。
1、综合实验题的特点
为达到制备物质或检验物质性质的实验目的,通常需要组装一整套比较复杂的实验仪器。以这类实验为内容,给出实验装置图,针对各仪器的作用或其中发生的反应提出问题要求作答的试题就是综合实验题。
综合实验题既能考察考生中学阶段动手实验的情况,又能考察考生基本实验操作技能,还能考察学生设计实验、探究性质、分析处理数据、得出结论、准确表述实验过程和结论的探究性学习能力。因此,综合实验题一直以来是再现率较高、权重较大的高考题型,在近几年新课程高考试题中,更是频繁出现,而且溶化工流程、表格数据分析和图像表达于一体,呈现出新特点。
1.1注重对教材典型实验的整合、拓展和延伸,重视对综合分析问题能力的考查。
例1.实验室进行某项实验并检验反应产物的装置如下图:
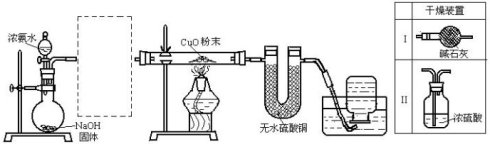
将足量浓氨水从分液漏斗中加入烧瓶中后,如图进行实验,实验现象记录如下:
①黑色氧化铜粉末变为光亮红色;②无水硫酸铜粉末变蓝色③集气瓶中收集到一种无色气体。
请回答下列问题:
(1)虚线框内是否应添加必要的干燥装置?______(填“是”或“否”)。若需要,应选择的干燥装置是__________(填编号,若不需要,该空可不填)
(2)在实验中NaOH固体的作用是________________________________________。
(3)最终集气瓶中收集到的气体是 。
CuO粉末处发生化学反应方程式为 。
解析:从左向右,第一套仪器取自教材中的H2O2遇MnO2制氧气,原理为NH3+H2O  NH3·H2O
NH3·H2O  NH4++OH-遇NaOH,OH-浓度增大,平衡逆向移动,于是产生氨气;第二套仪器为干燥装置,如不安装此仪器,就无法判断NH3与CuO反应是否生成了水,又氨气与硫酸反应会生成硫酸盐,所以不用浓硫酸干燥而用碱石灰干燥;第三套仪器取此氢气还原氧化铜,由于NH3氮元素处于最低价态,这决定了NH3具有还原性;第四、五部分仪器则是为了检验反应产物和吸收未反应的氨气的。
NH4++OH-遇NaOH,OH-浓度增大,平衡逆向移动,于是产生氨气;第二套仪器为干燥装置,如不安装此仪器,就无法判断NH3与CuO反应是否生成了水,又氨气与硫酸反应会生成硫酸盐,所以不用浓硫酸干燥而用碱石灰干燥;第三套仪器取此氢气还原氧化铜,由于NH3氮元素处于最低价态,这决定了NH3具有还原性;第四、五部分仪器则是为了检验反应产物和吸收未反应的氨气的。
参考答案:(1)是,I
;(2)NaOH溶于水产生大量的热,并且电离产生大量的OH-,使NH3+H2O  NH3·H2O
NH3·H2O  NH4++OH-平衡向左移动,最终NH3·H2O分解产生NH3。(3)N2(1分);2NH3+3CuO3Cu+N2+3H2O
NH4++OH-平衡向左移动,最终NH3·H2O分解产生NH3。(3)N2(1分);2NH3+3CuO3Cu+N2+3H2O
点评:综合实验题是对教材中物质制备和性质实验的整合。解答这类试题的前提是考生必须熟练掌握元素化合物性质,知道各种仪器的结构、适用范围和工作原理,掌握气体制备、除杂、收集、尾气处理等一系列基本实验操作,熟练掌握教材中的一些典型实验装置,弄清物质在实验系统装置中的流向及在各部分仪器里发生的变化。
1.2注重实验方案设计和原理探究,重视对创新思维能力的考查。
例2、(2008年海南卷,16)现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。已知实验中可能会发生下列反应:
①2Mg+O2=2MgO;②3Mg+N2=Mg3N2;③2Mg+CO2=2MgO+C;
④Mg+H2O=MgO+H2↑;⑤Mg3N2+6H2O3=Mg(OH)2+2NH3↑
可供选择的装置和药品如下图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。
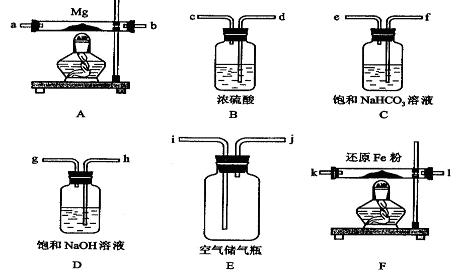
回答下列问题;
(1)在设计实验方案时,除装置A、E外,还应选择的装置(填字母代号)及其目的分别______________________________________;
(2)连接并检查实验装置的气密性。实验开始时,打开自来水的开关,将空气从5升的储气瓶压入反应装置,则气流流经导管的顺序是(填字母代号)_________ _________;
(3)通气后,如果同时点燃A、F装置的酒精灯,对实验结果有何影响?原因是什么?
(4)请设计一个实验,验证产物是氮化镁。
解析与答案:(1)B、D、F。选择b目的是除去空气中的水蒸气;选择D目的是除去空气中的CO2;选择F目的是除去空气中的O2。
(2)H→G→D→C→K→L→A→B
(3)制得的氮化镁将不纯;因为a装置没有排完空气前就加热会让空气中的氧气、CO2、水蒸气等与镁反应。
(4)将产物取少量置于试管中,加入适量水,将润湿的红色石蕊试纸置于试管口,如果能够看到润湿的红色石蕊试纸变蓝,则说明产物是氮化镁。
点评:本题以镁与氮气的反应为命题素材,综合考查了物质制备、除杂和设计实验验证产物等基本知识,特别考查实验设计能力。综合实验设计要解决下列问题:需要什么试剂、通过什么反应来制备物质或验证物质的性质,即根据实验目的,弄清实验原理;通过什么设备来达到实验目的,即根据反应物的状态和反应条件、要否除杂等确定实验装置;哪一套实验方案最简洁,即实验方案的评价和筛选。
1.3注重定性实验和定量实验的有机结合,重视对数据分析处理能力的考查。
例3、(2009浙江理综,28)单晶硅是信息产业中重要的基础材料。通常用炭在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500℃),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
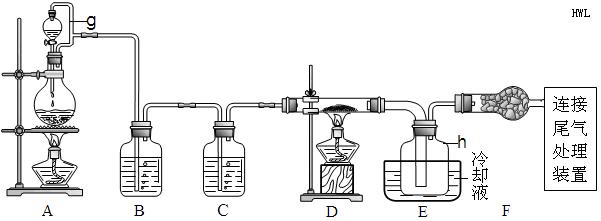
相关信息如下:①四氯化硅遇水极易水解;
②硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
③有关物质的物理常数见下表:
物质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
沸点/℃ | 57.7 | 12.8 | — | 315 | — |
熔点/℃ | -70.0 | -107.2 | — | — | — |
升华温度/℃ | — | — | 180 | 300 | 162 |
请回答下列问题:
(1)写出装置A中发生反应的离子方程式 。
(2)装置A中G管的作用是 ;装置C中的试剂是 ;
装置E中的H瓶需要冷却的理由是 。
(3)装置E中H瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的杂质元素是 (填写元素符号)。
(4)为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4-+8H+5Fe3++Mn2++4H2O
①滴定前是否要滴加指示剂? (填“是”或“否”),请说明理由 。
②某同学称取5.000g 残留物后,经预处理后在容量瓶中配制成100 mL 溶液,移取25.00 mL 试样溶液,用1.000×10-2mol/L KMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液20.00 mL,则残留物中铁元素的质量分数是 。
解析:装置A是氯气发生装置,因浓盐酸有挥发性,故分液漏斗要加盖,加盖后如没有G管,则盐酸就不易流下去。A中的离子方程式为MnO2+4H++2Cl- Mn2++Cl2↑+2H2O,A中G管的作用是平衡压强,使液体顺利流出并防止漏气。B为除杂装置,内盛饱和氯化钠溶液,既能除去HCl,又不损耗Cl2;C装置为干燥装置,,内盛浓硫酸。D为氯气与粗硅反应生成SiCl4,H瓶收集粗产物,精馏粗产品可得高纯度四氯化硅,由表中数据可以看出,蒸出SiCl4气体时,BCl3早已成气体被蒸出,而AlCl3、FeCl3、PCl5升华温度均低于SiCl4,所以当SiCl4蒸出后,而AlCl3、FeCl3、PCl5还为固体留在瓶里。而检验残留物中铁元素则是通过氧化还原滴定来进行的,最后结果则要根据题中所取样品的精确度取四位有效数字。
Mn2++Cl2↑+2H2O,A中G管的作用是平衡压强,使液体顺利流出并防止漏气。B为除杂装置,内盛饱和氯化钠溶液,既能除去HCl,又不损耗Cl2;C装置为干燥装置,,内盛浓硫酸。D为氯气与粗硅反应生成SiCl4,H瓶收集粗产物,精馏粗产品可得高纯度四氯化硅,由表中数据可以看出,蒸出SiCl4气体时,BCl3早已成气体被蒸出,而AlCl3、FeCl3、PCl5升华温度均低于SiCl4,所以当SiCl4蒸出后,而AlCl3、FeCl3、PCl5还为固体留在瓶里。而检验残留物中铁元素则是通过氧化还原滴定来进行的,最后结果则要根据题中所取样品的精确度取四位有效数字。
参考答案:(1)MnO2+4H++2Cl- Mn2++Cl2↑+2H2O;(2)平衡压强,使液体顺利流出并防止漏气;浓硫酸;产物SiCl4沸点低,需要冷凝收集;(3)Al、P、Cl;(4)①否;KMnO4溶液的紫红色可指示反应终点;②4.480%;
Mn2++Cl2↑+2H2O;(2)平衡压强,使液体顺利流出并防止漏气;浓硫酸;产物SiCl4沸点低,需要冷凝收集;(3)Al、P、Cl;(4)①否;KMnO4溶液的紫红色可指示反应终点;②4.480%;
点评:该题综合考查了氯气的制法、粗硅的提纯、氧化还原滴定等实验知识,对物质制备和定性分析进行了有机结合,对有效数字的运算规则也有要求。解答这类题的基础是熟练掌握教材中基本的物质制备和性质实验,并掌握中和滴定等实验操作,同时还要熟悉不同仪器的精确度,如台式天平的精确度为0.1g,分析天平的精确度为0.001g,量筒的精确度为0.1mL,滴定管和移液管的精确度为0.01mL,对实验所测的数据要根据仪器的精确度进行四舍五入的处理,然后再根据反应的化学方程式进行计算。
2.综合实验题的解题方法
综合实验题一般由题头、装置图、问题或数据处理等几部分组成。题头是说明本实验是制备物质还是探究物质性质,即说明实验的目的;装置图则给出实验所需要的设备;问题部分则是针对实验原理和装置图提出一些问题,有要求写出某部分装置里发生的化学反应或离子反应的方程式的,有要求说明某个仪器的作用的,有问某一个仪器中所盛装的试剂是什么的,有要求描述实验操作方法和步骤的(此时必须用操作性语言,如果用原理性语言回答是不给分的),有问仪器之所以这样连接或实验之所以这样操作的原因和理由的,也有要求进行实验数据处理的等等。
解综合实验题,首生要认真阅读题头,弄清实验的目的,根据目的进一步弄清实验的原理。例如上述例3的实验目的是在实验室中模拟工业制备高纯硅,其原理是先制得干燥纯净的氯气,再让氯气与粗硅反应生成易气化的SiCl4,从而把硅元素从粗硅中加以分离,然后再用氢气还原SiCl4制得高纯硅。整个过程的化学方程式为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,Si+2Cl2===SiCl4,SiCl4+2H2 ===Si+4HCl。由反应可知生成的氯气中还含有HCl和H2O等杂质,需要除杂。
MnCl2+Cl2↑+2H2O,Si+2Cl2===SiCl4,SiCl4+2H2 ===Si+4HCl。由反应可知生成的氯气中还含有HCl和H2O等杂质,需要除杂。
其次是弄清楚物质在整套装置中的流向及所到之处发生的反应和可能出现的现象。这是解这类题的关键。读懂了装置图及物质流经各部分仪器时发生的反应,就基本上等于解答了题目。
第三步是结合上两步的阅读和分析,对题目提出的问题进行解答。
当然,也有些综合实验题可能涉及的原理是考生在高中阶段没有学过的知识,但这个知识并不影响解答问题。这时,如果考生沿着这三步去分析,可能在第一步或第二步就被卡住了,即要弄清整道题所涉及的反应原理和整套装置的作用和工作原理就成为不可能,这时,考生就没有必要去按从前到后的顺序一步一步地进行,可以先浏览一下整道试题,带着问题去读题头和装置图,只要问题能得已解决就行。这样可以节省答题时间,比较快捷地解答问题。
以上为解答综合实验题的一般方法,具体问题应具体分析。要达到熟练解答此类试题的目的,还需要熟练掌握基本实验操作方法,熟悉各种仪器的结构、用途和工作原理,牢记常见气体的实验室制法,更重要的还需要做一定数量的综合实验题,以训练自已的解题技巧和解题速度

- 全部评论(0)
