有机物分子式确定的基本思路与方法
时间:2012-11-23 15:40 来源:未知 作者:胡中宇 点击: 次 所属专题: 有机物分子式计算
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
有机化学计算的重点是分子式、结构式的确定以及有机混合物的组成、含量的求算.其前部分的确定途径可用下图表示:
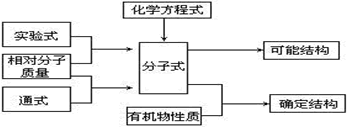
确定有机物分子式和结构式的基本思路是:

1. 直接求解法
核心内容是先求出1mol有机物中所含各元素原子的物质的量
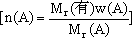
由此确定其分子式。它适用于有机物摩尔质量(或能先求出)及元素组成已知条件下的计算。
例1、引起国人共愤的“结石宝宝”事件中的罪魁祸首是三聚氰胺,实验测得其蒸气对氢气的相对密度为63,又知其分子组成中含C:28.57%、H:4.76%、N:66.67%,试确定其分子式。
解析:三聚氰胺的相对分子质量为63×2=126,故1mol三聚氰胺分子中含C原子、H原子、N原子的物质的量分别为:
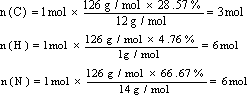
故其分子式为C3H6N6。
2. 最简式(实验式)法
先求出有机物分子中各元素原子个数最简整数比,以此为依据得出最简式,然后依据有机物的相对分子质量或类别确定其分子式。分子中原子个数最简整数比的求解方法为:
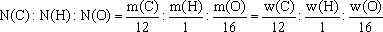
此方法适用于各元素质量分数(或质量)已知或可求出的条件下的计算。
例2、28g某气态烃在标准状况下的体积为11.2L,其中含碳85.7%,求其分子式。
解析:该烃的相对分子质量为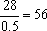 ,该烃分子中碳与氢的最简整数比为:N(C):
,该烃分子中碳与氢的最简整数比为:N(C):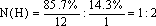 。最简式为CH2,设该烃的分子式为(CH2)n,14n=56,得n=4,分子式为C4H8。
。最简式为CH2,设该烃的分子式为(CH2)n,14n=56,得n=4,分子式为C4H8。
3. 单位物质的量法
通常用于一定量有机物完全燃烧时所得产物的量已知情况下的计算,主要过程是由CO2、H2O的量求出C、H原子物质的量,然后转化为1mol有机物中所含碳氢(氧)原子的物质的量,进一步确定其化学式。
例3、某有机物9.0g,完全燃烧后得到CO28.8g、H2O 1.8g。该有机物蒸气的密度是相同状况下H2密度的45倍,则该有机物的分子式为( )。
A. C4H10O2 B. C2H2 C. C2H4O3 D. C2H2O4
解析:该有机物相对分子质量为2×45=90,9.0g有机物的物质的量为:
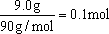 ,
,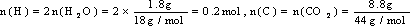 =0.2mol。
=0.2mol。
因 ,
,
故该有机物中一定还含有氧元素,含氧原子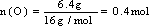 ,n(有机物):n(C):n(H):n(O)=0.1mol:0.2mol:0.2mol:0.4mol=1:2:2:4,分子式为C2H2O4。答案:D
,n(有机物):n(C):n(H):n(O)=0.1mol:0.2mol:0.2mol:0.4mol=1:2:2:4,分子式为C2H2O4。答案:D
注意:运用此种解法解题,有时需要确定有机物中是否含有氧元素,方法是将m(C)+m(H)与m(有机物)进行比较,若二者相等,无氧;若前者小,有氧;若前者大,计算的数据有错误。
4. 组成通式法
此方法的核心是利用各类有机物的组成通式进行计算。适用于有机物的种类已知或可以先确定出种类的题目。
例4、某气态不饱和烃对氢气的相对密度为27,0.54g该烃恰好与浓度为0.2mol/L的溴水100mL完全反应,使溴水完全褪色,求该烃的分子式。
解析:Mr(烃)=27×2=54。该烃与溴反应的物质的量之比为
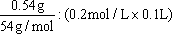 =1:2
=1:2
该烃为炔烃(或二烯烃),通式为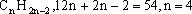 。分子式为C4H6。
。分子式为C4H6。
5. 燃烧通式法
计算的核心内容是根据有机物完全燃烧反应前后气体体积或燃烧时耗氧量及生成CO2、H2O的量的关系,利用有机物燃烧通式:
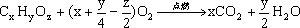 (烃中z=0)
(烃中z=0)
来确定有机物分子式。
例5、10mL某种气态烃,在50mL氧气中充分燃烧,得到液态水和体积为35mL的混合气体(所有气体体积都是在同温同压下测定的),则该气态烃可能是( )。A. 甲烷 B. 乙烷 C. 丙烷 D. 丁炔
解析:设该烃的分子式为CxHy
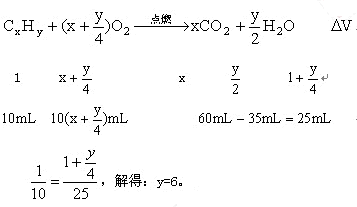
又因为烃完全燃烧时,需氧气过量或适量,则必须满足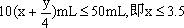 。
。
利用燃烧反应方程式,要抓住以下关键:①气体体积变化;②气体压强变化;③气体密度变化;④混合物平均相对分子质量等,同时可结合适当方法,如平均值法、十字交叉法、讨论法等技巧可速解有机物的分子式.
①当条件不足时,可利用已知条件列方程,进而解不定方程,结合烃CxHy中的x、y为正整数,烃的三态与碳原子数相关规律(特别是烃为气态时,x≤4)及烃的通式和性质,运用化学──数学分析法,即讨论法,可简捷地确定气态烃的分子式。
②当烃为混合物时,一般是设平均分子式,结合反应式和体积求出平均组成,利用平均值的含义确定各种可能混合烃的分子式.有时也利用平均相对分子质量来确定可能的组成,此时,采用十字交叉法计算较为简捷.
③两混合烃,若其平均相对分子质量小于或等于26,则该烃中必含甲烷。
④两混合气态烃,充分燃烧后,生成CO2气体的体积小于2倍原混合烃的体积,则原混合烃中必含CH4.若生成水的物质的量小于2倍原混合烃的物质的量,则必含C2H2。
⑤气体混合烃与足量的氧气充分燃烧后,若总体积保持不变,则原混合烃中的氢原子平均数为4;若体积扩大,氢原子平均数大于4;若体积缩小,氢原子平均数小于4,即必含C2H2(温度在100℃以上)。
6.余数法.
①用烃的相对分子质量除14,视商数和余数.

其中商数A为烃中的碳原子数.
此法运用于具有确定通式的烃(如烷、烯、炔、苯的同系物等).
②若烃的类别不确定:CxHy,可用相对分子质量M除以12,看商和余数.

③由一种烃的分子式,求另一可能烃的分子式可采用增减法推断,其规律如下:


- 全部评论(0)
