常见的框图结构探讨
时间:2020-02-23 17:37 来源:未知 作者:张县 点击: 次 所属专题: 框图推断 无机推断
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
高考中的推断题有两种基本类型——文字型和图表型。文字型推断题已在上一章简单介绍过,这类题目的信息来源比较单一,通常经过仔细分析和简单的推测,我们都可以准确地确定答案,而这一类题目的真正考点通常并不落在推断上,而更多是对各版块化学知识的综合考查。图表型推断题的考点则主要落在推断的过程中,题目中会给出图表信息和文字信息,要求答题者综合所学知识,将有用信息快速提取出,然后将图表中的转化关系补充完全。由于信息量大,抽象与形象思维并用,因而图表型的推断题在难度上远远超过了前者,一份化学试卷的区分度也往往在这一道题上体现,拿下这一道题,无疑会给你的分数大大地添砖加码。
虽然无机图表推断题难度较大,但对于高考而言,有两点原则是绝对不会改变的:首先,框图中的绝大多数物质都必然是“中学化学中的常见物质”,绝大多数反应也必然是高中课堂上会提及的反应,也就是说,任何一道推断题都必然能仅利用中学阶段的知识求解;其次,作为图表推断题,整道题的在知识综合性上的难度并不会很大,题目的考查内容一般仅限于氧化还原反应、离子反应的理论,元素化合物的基本知识和较简单的计算,推断方面的难度和理论知识方面的难度绝不会失衡,即一般不会出现“一山放过一山拦“的现象。这两点原则是同学们在进行推断题训练的过程中一定要重视的。
(1)图表推断题的审题与解答流程
图表推断题的题干由“图”和“文”两部分组成,审题时也必须将两个部分全部读完。在解题的实践中,我们能得到下面的三种做推断题的方式:
①“图文对应式”:先读完题目的文字,圈画下关键信息,然后分析框图,将题目信息与框图逐一对应,在这个过程中寻找突破口,并将框图全部填完,最后根据所填的内容回答下面的问题。
这种方法是大多数同学所采用的方法,也是绝大多数化学教师讲解题目时所采用的方法。这种方法是最符合一般人的逻辑思维过程的,有一定的合理性,对基础薄弱的同学是非常适用的。但它最致命的缺陷就是——慢。答题者必须将“推”和“答”的过程完全分开,从而不得不耗费大量的时间;而且在推断的过程中,答题者往往会得处理大量的无用信息,这也在无形中消耗了考试中宝贵的时间。据笔者的调查,一位普通的同学采用这种方法做完一道超过十个框的框图推断题至少需要10分钟的时间,有时因为紧张,很可能会出现推了15分钟却毫无结果的最糟糕情况,也就是常说的“推不出”。但由于受人脑的思维模式限制,除了靠大量的题海式训练,这个问题很难解决。
②“图猜文验式”:先看图(或先快速浏览叫简短的文字信息),通过快速的发散联想在框图上主观地确定一些信息,然后利用其它的文字信息进行验证。通过“猜—验”的模式将框图中的有效信息填上后,再利用下面的问题进行进一步的验证。
这是一种“反常规”的思维方法,需要大量的积累和很强的逻辑思维能力,也需要答题者有一定的“悟性”,似乎很难应付千变万化的题目。但事实上,当答题者的知识基础较为牢固后,实施这种方法的难度并不大,而收效却相当显著。这种方法优化了“推”的过程,有助于快速把握有效信息,能将答题的速度提高50%以上。
③“以答带推式”:快速浏览一遍文字信息和框图后,立刻看问题,争取从问题中“挖”出一些暗示信息,然后再回到题目中进行推断。
这种方法尤其适用于上面提到的“一图两(多)解型”推断题。要注意的是,读问题并不是“猜答案”,而是读出命题人在命题过程中的“疏忽”,尤其是命题人设置的一些综合性题目更容易泄露出一些有效信息。这种方法不能算是解题方法,也不一定适用于每一道题,但同学们在解答推断题时,还是应该训练“图文题一体化”的审题模式,最好不要只盯着前面的题干,将全部内容推完后才开始答题。
(2).常见的框图结构探讨
省略部分反应物和生成物的框图结构
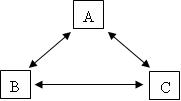
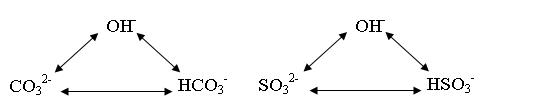
(1)三角关系型
“三角转化关系”是推断题中经常提到的一种重要的转化关系,一般的“三角关系”是三者之间均可相互转化的形式,如课本上提到过的“铁三角”。而推断题中常出现的是上图中的简化型的“三角关系”。这种转化模式中,B相当于由A到C的一个中间物质,其性质应是较为多样的。下面给出几组非常重要的“三角关系”。
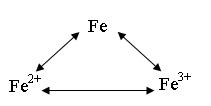
①铁三角
“铁三角”的转化是无机推断题中永恒的热点,考察的变化很多,但基本的原则是始终如一的。单质Fe和Fe2+离子都是还原剂,而Fe3+是氧化剂,Fe2+/Fe和Fe3+/Fe2+构成两组氧化还原电对。在相应的氧化剂或还原剂作用下,即可实现氧化还原电对中氧化型与还原型的相互转化。而Fe单质直接转化为Fe3+,需要通过O2、Cl2、硝酸等强氧化剂的作用,将Fe3+转化为Fe单质,则应用还原剂还原Fe的+3价氧化物。当然,在三角转化关系之外,我们还应注意这三者同时出现的反应Fe+2Fe3+==3Fe2+。
下面是一组填入上面的简化三角关系图的情况:
A. Fe B. FeCl2 C. FeCl3
Fe+2HCl==FeCl2+H2↑ 2FeCl2+Cl2==2FeCl3 2Fe+3Cl2 2FeCl3
与Fe元素有关的另一组重要的情况
A. Fe3+(FeCl3、Fe2(SO4)3等) B. Fe(OH)2 C. Fe(OH)3
Fe3++3OH-== Fe(OH)3↓ Fe2++2OH-== Fe(OH)2↓ 4Fe(OH)2+O2+2H2O==4Fe(OH)3
特别要注意的是B→C的反应现象为“沉淀先变成灰绿色,后变成红褐色”。
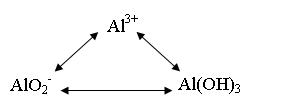
②铝三角
“铁三角”是“氧化还原三角”,而“铝三角”则是“离子反应三角”,二者正好代表了高中阶段重点接触的两种基本反应。铝三角的成因是Al(OH)3的两性,即Al(OH)3在溶液体系中存在两种电离方式H++AlO2-+H2O Al(OH)3 Al3++3OH-,Al(OH)3在酸中溶解变成Al3+,在碱中溶解变成AlO2-,基于上面的两个可逆反应,便形成了三角转化关系。同样,我们也应注意这三者同时出现的反应Al3++3AlO2-+6H2O==4Al(OH)3↓
下面是一组填入上面的简化三角关系图的情况:
A. Al3+ B. Al(OH)3 C. AlO2-
Al3++3OH-== Al(OH)3↓ Al(OH)3+ OH-== AlO2--+2H2O Al3++4OH-== AlO2--+2H2O
当然,任意调换三者的位置,我们都可以得到一组合理的能填入上面的简化三角关系图的情况。
若考虑Al单质,还可以得到下面的填法:
A. Al B. Al3+ C. AlO2-
2Al+6H+==2Al3++3H2↑ Al3++4OH-== AlO2--+2H2O 2Al+2OH-+2H2O==2AlO2-+3H2↑
或可填成 A. Al B. AlO2- C. Al3+
2Al+2OH-+2H2O==2AlO2-+3H2↑ AlO2-+4H+ ==Al3++2H2O 2Al+6H+==2Al3++3H2↑
③“碱—正盐—酸式盐”三角
“碱—正盐—酸式盐”三角关系是我们从初中阶段就开始接触到的经典转化关系,和“铝三角“一样,它也是一个基于电解质溶液和离子反应原理的转化关系。这一三角关系的关键环节是酸式盐离子HCO3-,在溶液中,其存在着电离和水解的双重平衡;在固体状态下,酸式盐能分解成正盐。而利用沉淀反应的方法可以实现CO32-→OH-,HCO3-→OH-的转化。同样,我们也应该注意三者同时出现的反应 OH-+HCO3-==CO32-+H2O
下面是一组填入上面的简化三角关系图的情况:
A. Na2CO3 B. NaOH C. NaHCO3
CO2+H2O+Na2CO3==2NaHCO3 Na2CO3+Ca(OH)2==CaCO3↓+2NaOH CO2+NaOH==NaHCO3(过量CO2通入NaOH溶液中)
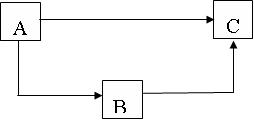
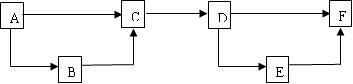
实际的题目中,命题人常常会将Na单质和其氧化物加入到上面的“NaOH—Na2CO3—NaHCO3”关系中,构成复合反应关系,如下面得这个简单的框图,它实际上是由两个前面的“简化三角关系图”复合而成的,若A为Na单质,有下面的填法:
A . Na B. Na2O C. Na2O2 D. NaOH E. Na2CO3 F. NaHCO3
4Na+O2==2Na2O 2Na+O2==Na2O2 2Na2O+O2==2Na2O2 2Na2O2+2H2O==4NaOH+O2↑
CO2+2NaOH==Na2CO3+H2O CO2+H2O+Na2CO3==2NaHCO3 CO2+NaOH==NaHCO3
藉由反应2Na2O2+2CO2==2Na2CO3+O2↑,当D为Na2CO3时同样能填出右边的三个空。
除了上面三个典型的三角关系外,若充分挖掘高中化学中的反应方程式,我们还可以以“N、S、Cl、Mg、C、Si、P”等各种常见元素为中心写出很多个三角关系图(不一定要完全能相互转化),并据此填出上面的简化三角关系图,这项工作交由读者们自己来完成。同学们列关系图时,一定要注意自己所列的是“氧化还原关系图(如”铁三角“)”还是“离子反应关系图(如“碱—正盐—酸式盐”三角)”,这是充分掌握这些反应关系的前提。
(2)直线型
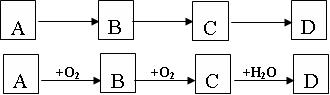
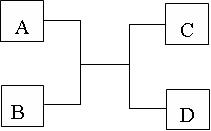
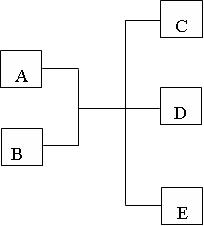
直线转化是框图中常见的结构,而命题人最青睐的莫过于上面的“连续氧化型”的线型框图。连续氧化型框图中B、C是一种元素的两种不同价态的化合物,而A可以是单质,也可以是化合物。连续氧化型框图中“A+O2→B”、“B+O2→C”是“主干部分”,而有些框图通常还会在最后加上“C+H2O→D”一步,或在前面加上“D+H2O→A”。在直线型的框图中,A、B、C、D中一般都含有同一种元素。
下面是以某种元素为主线的符合连续氧化条件的几组常见物质:
①主线元素:C
A. C(CH4、C2H4、C2H2、C2H6等烃类)B. CO C. CO2 D.H2CO3
A→B为碳或烃类的不完全燃烧,B→C为CO的燃烧,如
2C+O2==2CO(CH4+3O2==2CO+4H2O等) 2CO+O2==2CO2 CO2+H2O==H2CO3
②主线元素:S
A. S(H2S、FeS2等) B. SO2 C. SO3 DH2SO4
A→B为S或H2S的完全燃烧或煅烧FeS2等含硫的矿物,B→C为SO2的接触氧化,C→D为SO3的吸收,硫酸工业的流程也符合这一转化关系,如
S+O2==SO2(2H2S+3O2==2SO2+2H2O或4FeS2+11O2==2Fe2O3+8SO2)
③主线元素:N
A. N2(NH3) B. NO C. NO2 DHNO3
A→B为N2与O2放电时反应或NH3的催化氧化,B→C为NO的氧化,C→D为NO2与H2O的重新生成NO的反应,如
N2+O2![]() 2NO(4NH3+5O2==4NO+6H2O) 2NO+O2==2NO2 3NO2+H2O==2HNO3+NO
2NO(4NH3+5O2==4NO+6H2O) 2NO+O2==2NO2 3NO2+H2O==2HNO3+NO
④主线元素:Na、O
A. Na B. Na2O C.Na2O2 DNaOH
这一关系中虽然A、B、C、D中都含有Na元素,但决定了这一关系的实际上是O元素的价态变化。A→B为Na在空气中的氧化,B→C为Na2O的进一步氧化,C→D为Na2O2与H2O的放出O2的反应,如4Na+O2==2Na2O 2Na2O+O2==2Na2O2 2Na2O2+2H2O==4NaOH+O2↑
⑤有机物的连续氧化
有机化学中醇→醛→酸转化正好也能构成一个连续氧化关系,而将D移至A前,构成“D+H2O→A”的转化,然后加入“A+C→E”的转化,便可得到“卤代烃→醇→醛→酸→酯”的完整转化关系,如CH3CH2Br+H2O→CH3CH2OH+HBr 2CH3CH2OH+O2→2CH3CHO+2H2O
2CH3CHO+O2→CH3COOH CH3COOH+ C2H5OH→CH3COOCH2CH3+H2O
对于一般的直线型转化关系,当A、B、C、D中含有同一种元素时,我们可以写出很多组情况。读者们可以用“接龙”的方法进行训练,即先写出A物质,然后根据某个反应条件使A转化为B,A与B中至少有一种元素相同;不断重复这一过程直至填出A、B、C、D为止(或者一直填下去,直至填不出下一个物质为止)。这不失为充分训练元素化合物推断的一种好方法。下面给出几组示例:
①H2→H2O→NaOH→Mg(OH)2 ②CaC2→C2H2→CO2→CO32-
③NH4HCO3→NH3→NO→NO2 ④Na→Na2O2→Na2CO3→NaOH
⑤Mg→MgO→Mg2+→Mg(OH)2 ⑥Al3+(AlO2-)→Al(OH)3→Al2O3→Al
⑦Na2SiO3→H2SiO3→ SiO2→Si ⑧P→P2O5→H3PO4→Ca3PO4
⑨NaCl→Cl2→Ca(ClO)2→HClO ⑩Cu→CuO→Cu2+→Cu(OH)2
完整给出反应物和生成物的结构
(3)A+B==C+D型
两种反应物反应生成两种生成物,这是一种较为常见的反应关系。我们初中时所接触的置换反应和复分解反应,以及高中阶段所学的一些氧化还原反应的形式都满足这一结构特征。下面针对一些较为特殊的情况进行讨论。
①A、C为单质,B、D为化合物(置换反应)
按两种单质A和C的情况,可将置换反应分为:
a. A、C均为金属。有两种情况,一种是较活泼的金属(K、Ca、Na除外)从另一种金属的盐溶液中将另一种金属置换出来;另一种是较活泼的金属在高温下将另一种金属从其氧化物中置换出来,两者的实质都是还原性较强的金属和氧化性较强的离子反应,生成还原性较弱的金属和氧化性较弱的离子。如Zn+CuSO4==ZnSO4+Cu 8Al+2Fe3O4==9Fe+4Al2O3
b. A、C均为非金属。同样有两种情况,一种是氧化性单质间的置换反应,另一种是还原性单质间的置换反应。
氧化性单质间的置换反应具体的类型有:
卤素单质(Cl2、Br2、I2)间的置换反应,如Cl2+NaBr==Br2+NaCl Br2+2KI==2KBr+I2
O2、Cl2与-2价的S、-3价的N的反应,如 2H2S+O2==2S+2H2O (有两种情况,一种是O2通入氢硫酸中直接氧化,另一种是H2S在O2中的不完全燃烧)
Cl2+Na2S==2NaCl+S↓ (常用来证明Cl2的氧化性强于S)
3Cl2+2NH3==N2+6HCl(Cl2过量) 3Cl2+8NH3==N2+6NH4Cl (NH3过量)
4NH3+3O2==2N2+6H2O (NH3在纯氧中燃烧的反应)
此外还应注意的是2F2+2H2O==4HF+O2 (F2不能与NaCl、NaBr等盐的溶液发生置换反应)
还原性单质间的置换反应主要是H2、C、Si之间的反应,如C+H2O![]() CO+H2 (制得CO与H2的混合气体称为“水煤气”)2C+SiO2==2CO+Si (工业上制取粗硅的反应)
CO+H2 (制得CO与H2的混合气体称为“水煤气”)2C+SiO2==2CO+Si (工业上制取粗硅的反应)
2H2+SiCl4 ![]() Si+4HCl (工业上将粗硅转化为气态的卤化物后提纯单晶硅的方法)
Si+4HCl (工业上将粗硅转化为气态的卤化物后提纯单晶硅的方法)
c. A为非金属,C为金属。主要是还原性的单质将金属从其氧化物中置换出来的反应,如炼铁的反应 3C+2Fe2O3==4Fe+3CO2 3H2+Fe2O3==2Fe+3H2O
H2、C还原氧化铜的反应 H2+CuO==Cu+H2O C+2CuO==2Cu+CO2
2008年全国理综卷出现的C+PbO==Pb+CO 也属于这一类型
d. A为金属,C为非金属。最常见的自然是高中阶段所学的各种产生H2的反应,如
2Na+2H2O==2NaOH+H2↑ Zn+H2SO4==ZnSO4+H2↑ 3Fe+4H2O(g) Fe3O4+4H2 2Na+2C2H5OH→2C2H5ONa+H-2↑ 还应注意一个经常考到且易忽略的反应 2Mg+CO2==2MgO+C
②A、C为气体,B、D为固体或液体
反应式两边都是“气体+固体或液体”是一种较特殊的情况,此时A或C中至少有一种为化合物,有下面几种常见的情况:
2Na2O2+2CO2==2Na2CO3+O2 (将CO2“转化”成O2的方法)
4FeS2+11O2==2Fe2O3+8SO2 (硫酸工业中制SO2的一种方法)
上面两个方程式在推断题中出现的几率相当高,应引起足够重视!
此外还有 3NO2+H2O==2HNO3+NO (注意NO与NO2间的转化)Fe2O3+3CO==2Fe+3CO2 CO+CuO==Cu+CO2 (注意CO与CO2间的转化)
③A为固体,B为H2O,D为气体,反应在常温下进行
常温下固体与H2O反应生成气体的反应也是一种非常特殊的反应,是考试里的热门考点。2008年全国理综卷便考了CaC2与H2O的反应。这类反应并不多,记住下面的几个例子即可: 2Na+2H2O==2NaOH+H2↑ (活泼金属与H2O的反应)
2Na2O2+2H2O==4NaOH+O2↑(太空舱中提供O2的简易方法)
CaC2+H2O==Ca(OH)2+C2H2↑ (实验室制取C2H2气体的方法)
一些阴离子易水解的盐与水反应也可以放出气体,如Mg3N2+6H2O== 3Mg(OH)2+2NH3↑ Al2S3+6H2O== 2Al(OH)3+3H2S↑
(4)A+B==C+D+E型
“A+B==C+D+E”型的化学方程式在推断题中出现的频率非常高,且通常C、D、E之间还可以发生反应。高中阶段也接触了一定数量的这种结构的反应。下面给出一些符合这一特征的反应方程式。
①氧化还原反应:
I. Cl2+2NaOH==NaClO+NaCl+H2O(Cl2+2Ca(OH)2==Ca(ClO)2+CaCl2+2H2O)
MnO2+4HCl==MnCl2+Cl2↑+H2O KClO3+6HCl==KCl+3Cl2+3H2O
Ⅱ. 浓H2SO4、硝酸发生的反应大多数都属于这种类型
C+2H2SO4(浓)==CO2↑+2SO2↑+2H2O C+4HNO3 (浓)==CO2↑+4NO2↑+2H2O
3C+4HNO3 (浓)==3CO2↑+4NO↑+2H2O
C与浓硫酸、硝酸反应都生成两种气体,这是衍生出其它转化关系的基础,在推断题中出现的频率较高。
Cu+2H2SO4 (浓)==CuSO4+SO2↑+2H2O Cu+4HNO3 (浓)==Cu(NO3)2+2NO2↑+2H2O
3Cu+8 HNO3 (稀)==3Cu(NO3)2+2NO↑+4H2O
2HBr+H2SO4(浓)==Br2+SO2+H2O 2HI+H2SO4(浓)==I2+SO2+H2O
②非氧化还原反应
I. 生成一种能分解为气体和H2O的物质(NH3·H2O、H2CO3、H2SO3、H2O2)的复分解反应一般都满足这种结构,如
Ca(OH)2+2NH4Cl==CaCl2+2NH3↑+2H2O CaCO3+2HCl==CaCl2+H2O+CO2↑
NaHSO3+HCl==NaCl+H2O+SO2↑ 2Na2O2+2H2SO4==2Na2SO4+O2↑+2H2O
Ⅱ. 酸式盐与碱生成难溶物的反应,如
2NaHCO3+ Ca(OH)2==CaCO3↓+Na2CO3+H2O NaHSO4+Ba(OH)2==BaSO4↓+NaOH+H2O
③电解反应
我们熟悉的氯碱工业电解饱和食盐水的反应便是符合这一结构的典型反应。
2NaCl+2H2O![]() NaOH+H2↑+Cl2↑ 这一反应在推断题中出现的频率也相当高,通常会由反应的生成物引出一系列的转化。
NaOH+H2↑+Cl2↑ 这一反应在推断题中出现的频率也相当高,通常会由反应的生成物引出一系列的转化。
电解其它溶液的总反应方程式也常常会出现上面的这一结构,下面便对电解溶液时产物的情况做一个归纳。
阴极:按金属离子的氧化性强弱的放电,即Ag+>Hg2+>Fe3+>Cu2+>H+(NH4+),由于电解液必然存在H2O,一般活动性在H之前的金属在电解时是不可能析出的。NH4+的放电实际上就是H+的放电,产物是NH3和H2。
阳极:一般只考察Cl-与OH-的放电顺序,记住Cl->OH-即可。但必须注意只有阳极为惰性电极时溶液中的Cl-或OH-才会放电,若电极为一般的金属,电解时金属电极先失电子溶解。
具体的实例如:电解NH4Cl溶液 2NH4Cl![]() 2NH3↑+H2↑+Cl2↑
2NH3↑+H2↑+Cl2↑
电解AgNO3溶液 4AgNO3+2H2O![]() 4Ag↓+4HNO3+O2↑
4Ag↓+4HNO3+O2↑
电解CuSO4溶液 2CuSO4+2H2O![]() 2Cu↓+2H2SO4+O2↑
2Cu↓+2H2SO4+O2↑
电解FeCl3溶液 2FeCl3![]() 2FeCl2+Cl2↑
2FeCl2+Cl2↑
电解MgCl2溶液 MgCl2+2H2O![]() Mg(OH)2+Cl2↑+H2↑
Mg(OH)2+Cl2↑+H2↑
不难看出,电解铜、汞、银的硫酸盐、硝酸盐溶液或电解H之前的金属对应的离子的氯盐溶液的方程式都满足“A+B==C+D+E”结构。

- 全部评论(0)