酸的浓度不同,反应情况不同的小结
时间:2022-08-12 10:27 来源:未知 作者:赵胜 点击: 次 所属专题: 常见酸
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
当化学反应进行时,反应物不断被消耗,随反应的进行,反应物浓度不断改变,发生反应情况就会各不相同,现小结如下,并结合有关化学方程式以及相对应的试题解析理解不同反应情况的本质原因。
1.酸的浓度不同,产物可能不同。
如过量的金属与浓酸反应的情况。
①在一定量浓HNO3中投入过量的铜,开始生成的气体是NO2,随着反应不断进行,HNO3浓度变稀,后来生成的气体是NO。
Cu+4HNO3(浓)==Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3(稀)==3Cu(NO3)2+2NO↑+4H2O
体验:1.92g铜投入一定量浓HNO3中,铜完全溶解,生成气体颜色越来越浅,共收集到672mL气体(标准状况)。将盛有此气体的容器倒扣在水中,通入标准状况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积为(
A.504mL
解析:生成气体颜色越来越浅,说明气体产物中既有NO2,又有NO,通入O2后恰好使气体完全溶于水中,说明NO2、NO的混合气体完全反应后又生成硝酸。反应前后最终N元素的化合价没有发生改变,改变的是Cu和O2中O元素的化合价,则铜失去的电子等于氧气得到的电子,即n(Cu)×2=n(O2)×4,因n(Cu) =0.03mol,故n(O2)=0.015mol,标准状况下O2的体积为336mL。选C。
②在一定量热浓H2SO4中投入过量的锌,开始生成的气体是SO2,随着反应不断进行,H2SO4浓度变稀,后来生成的气体是H2。
Zn+2H2SO4(浓)![]() ZnSO4+SO2↑+2H2O
ZnSO4+SO2↑+2H2O
体验:将一定量的锌与100mL18.5mol·L-1的浓硫酸充分反应后,锌完全溶解,同时生成气体A
33.6L(标准状况)。将反应后的溶液稀释至1
L,测得溶液中c(H+)=0.1mol·L-1,则下列叙述中错误的是(
A.反应中消耗的Zn的质量为97.5 g
B.气体A中SO2和H2的体积比为1∶4
C.反应中被还原的元素只有一种
D.反应中共转移电子3mol
解析:生成的33.6L(即1.5mol)气体可能是SO2和H2的混合气体,反应中共转移电子3mol,由电子守恒知消耗的Zn为1.5mol(97.5g);n(H2SO4)=1.85mol,反应后剩余H2SO4为0.05mol,生成的ZnSO4为1.5mol,则生成的SO2为0.3mol,生成的H2为1.2mol,A中SO2与H2的体积比为1∶4;显然,被还原的元素有S、H两种。选C。
思考:过量的铁、铝分别遇冷浓硫酸或冷浓硝酸均发生钝化,常温下发生钝化的原因是什么?加热时分别会发生什么反应?符合什么共性规律?铁、铝过量时分别发生什么反应?会发生完全一样的反应吗?为什么?
常温下钝化原因:冷浓硫酸或冷浓硝酸具有强氧化性,遇铁、铝时发生氧化还原反应生成一层致密的氧化物薄膜,阻碍了反应继续进行。加热后均发生氧化还原反应,符合浓硫酸或浓硝酸与金属反应生成相应的铁盐、气体及水的规律。Fe过量产生Fe2+盐,过量Fe、Al与浓H2SO4反应生成的气体先是SO2后是H2,过量Fe、Al与浓HNO3反应生成的气体先是NO2后是NO。
有关化学方程式如下:
2Fe+6H2SO4(浓)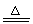 Fe2(SO4)3+3SO2↑+6H2O
Fe2(SO4)3+3SO2↑+6H2O
2Al+6H2SO4(浓)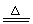 Al2(SO4)3+3SO2↑+6H2O
Al2(SO4)3+3SO2↑+6H2O
Fe过量:Fe+Fe2(SO4)3==3FeSO4
Al过量:2Al+3H2SO4(稀)== Al2(SO4)3+3H2↑
Fe+6HNO3(浓)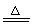 Fe(NO3)3+3NO2↑+3H2O
Fe(NO3)3+3NO2↑+3H2O
Al+6HNO3(浓)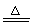 Al(NO3)3+3NO2↑+3H2O
Al(NO3)3+3NO2↑+3H2O
Fe过量:Fe+4HNO3(稀)== Fe(NO3)3+NO↑+2H2O
Fe+2Fe(NO3)3==3Fe(NO3)2
Al过量: Al+4HNO3(稀)==Al(NO3)3+NO↑+2H2O
2.酸的浓度不同,反应形式可能不同。
①过氧化钠和稀盐酸发生复分解反应:
2Na2O2+4HCl(稀)==4NaCl+O2↑+2H2O
过氧化钠和浓盐酸发生氧化还原反应:
Na2O2+4HCl(浓)==2NaCl+Cl2↑+2H2O
②次氯酸钠和稀盐酸发生复分解反应:NaClO+HCl(稀)==HClO+NaCl
次氯酸钠和浓盐酸发生氧化还原反应:
NaClO+2HCl(浓)== NaCl+Cl2↑+H2O
③硫化钠和稀硫酸发生复分解反应:Na2S+H2SO4(稀)==Na2SO4+H2S↑
硫化钠和浓硫酸发生氧化还原反应:
Na2S+2H2SO4(浓)==Na2SO4+S↓+SO2↑+2H2O
体验:实验室常用强氧化剂(如KMnO4、KClO3、MnO2、NaClO等)氧化浓盐酸的方法来制备氯气。某研究性学习小组欲探究用Na2O2与浓盐酸制备并检验氯气。供选用的实验试剂及装置如下(部分导管、蒸馏水略):
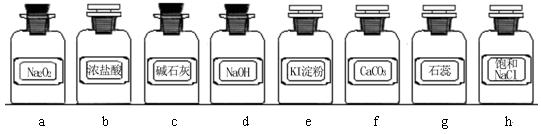
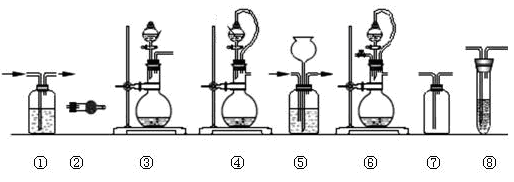
(1)写出用Na2O2与浓盐酸制备氯气的化学方程式_____________________。
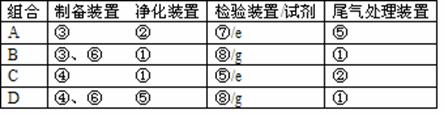
(2)下列装置组合最合理的是__________ (填序号,需考虑实验结束撤除装置时残留有害气体的处理)。
(3)尾气经处理后仍有较多气体排出,其主要原因是(请用化学方程式表示之)
(4)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:①
(5)你是否同意将Na2O2与浓盐酸的反应作为实验室制备氯气的方法之一?(填“是”或“否”);理由是。
解析:这是利用Na2O2的强氧化性来氧化浓盐酸制取Cl2,但由于Na2O2与水、稀盐酸均可反应生成O2,所以Na2O2的利用率降低,且Cl2中混有O2难以分离。制备Cl2时反应生成气体量多而快,烧瓶内气体的压强大,分液漏斗内的液体不易流入烧瓶内,最好能外加调压装置,所以选择④、⑥中带有恒压漏斗的装置作反应装置好,且该装置还可防止浓盐酸的挥发;净化装置可选用盛放水的洗气瓶⑤,该装置能观察导管是否发生堵塞现象;检验Cl2可用盛放石蕊试液的⑧;Cl2尾气处理可用盛放NaOH溶液的洗气瓶①。制备Cl2,用H2O2代替Na2O2进行实验更好,一是原料的利用率提高,二是产生等量的Cl2,H2O2消耗盐酸的量减少,并且H2O2价格便宜。
答案:(1)Na2O2+4HCl(浓)==2NaCl+Cl2↑+2H2O (2)D
(3)2Na2O2+2H2O==4NaOH+O2↑或4Na2O2+4HCl(稀)==4NaCl+2H2O+O2↑
(4)①Na2O2能与水反应,会使原料的利用率降低。②双氧水比Na2O2更经济。 ③产生等量的Cl2,用双氧水消耗的盐酸的量少。④Na2O2能与水反应,生成的NaOH能与盐酸反应。⑤Na2O2能与水反应,生成的NaOH吸收了Cl2。(以上任两点即可) (5)否,产物不纯且难以分离。
3.酸的浓度不同,反应有可能不再发生。
①过量MnO2投入一定量热浓盐酸中,随反应的进行,浓盐酸变稀,稀盐酸的还原性减弱,不再与MnO2发生氧化还原反应。
MnO2+4HCl(浓)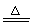 MnCl2+Cl2↑+2H2O,MnO2与HCl(稀)不反应。
MnCl2+Cl2↑+2H2O,MnO2与HCl(稀)不反应。
②过量铜投入一定量热浓硫酸中,随着反应不断进行,浓硫酸变稀,稀硫
酸不具有强氧化性,Cu与稀硫酸将不再发生反应。
Cu+2H2SO4(浓)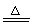 CuSO4+SO2↑+2H2O,Cu与H2SO4(稀)不反应。
CuSO4+SO2↑+2H2O,Cu与H2SO4(稀)不反应。
体验:在化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的情况,下列反应中属于这种情况的是( )
①过量的锌与浓硫酸反应
②过量的氢气与少量的N2在工业生产条件下反应
③过量的浓盐酸与碳酸钙反应
④过量的乙酸和少量乙醇在浓硫酸、加热条件下反应
⑤过量的二氧化锰与浓盐酸在加热条件下反应
⑥过量的铜与浓硫酸在加热条件下反应
A.②③④⑥ B.②④⑤⑥
解析:②④为可逆反应,不能完全反应;①先生成SO2,再生成H2,一定会将H2SO4消耗完;③CaCO3会完全反应;⑤、⑥考虑酸的浓度降到一定程度便不再发生反应。选B。
4.酸的浓度不同,有些本来不能发生的反应有可能发生。
如:稀H2SO4溅在衣服上,水分蒸发后,变成浓H2SO4,也就能使布料脱水炭化。
又如:稀H2SO4与NaCl不反应,但与NaCl可发生复分解反应:
H2SO4(浓)+NaCl==NaHSO4+HCl↑

- 全部评论(0)
