高中常见的原电池电极反应式的书写
时间:2018-03-14 16:44 来源:未知 作者:李萍 点击: 次 所属专题: 电极反应式
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一次电池
1、伏打电池:(负极—Zn、正极—Cu、电解液—H2SO4)
负极:Zn-2e-==Zn2+(氧化反应)
正极: 2H++2e-==H2↑(还原反应)
总反应Zn + 2H+== H2↑+ Zn2+
2、铁碳电池:(负极—Fe、正极—C、电解液H2CO3弱酸性)
负极:Fe-2e-==Fe2+(氧化反应)
正极:2H++2e-==H2↑(还原反应)
总反应Fe+2H+==H2↑+Fe2+(析氢腐蚀)
3、铁碳电池:(负极—Fe、正极—C、电解液 中性或碱性)
负极: 2Fe-4e-==2Fe2+(氧化反应)
正极:O2+2H2O+4e-==4OH-(还原反应)
化学方程式:2Fe+O2+2H2O==2Fe(OH)2(吸氧腐蚀)
4Fe(OH)2+O2+2H2O==4Fe(OH)3 2Fe(OH)3==Fe2O3+3 H2O(铁锈的生成过程)
4.铝镍电池:(负极—Al、正极—Ni电解液 NaCl溶液、O2)
负极: 4Al-12e-==4Al3+(氧化反应)
正极:3O2+6H2O+12e-==12OH-(还原反应)
总反应4Al+3O2+6H2O==4Al(OH)3(海洋灯标电池)
5、普通锌锰干电池:(负极—Zn、正极—C 、电解液NH4Cl、MnO2的糊状物)
负极:Zn-2e-==Zn2+(氧化反应)
正极:2MnO2+2H++2e-==Mn2O3+H2O(还原反应)
化学方程式Zn+2NH4Cl+2MnO2=ZnCl2+Mn2O3+2NH3↑
6、碱性锌锰干电池:(负极—Zn、正极—C、电解液KOH、MnO2的糊状物)
负极:Zn + 2OH-+2e-==Zn(OH)2(氧化反应)
正极:2MnO2+2H2O +2e-==2MnOOH +2OH-(还原反应)
化学方程式Zn +2MnO2+2H2O==Zn(OH)2+MnOOH
7、银锌电池:(负极—Zn、正极--Ag2O、电解液NaOH )
负极:Zn+2OH--2e-==Zn(OH)2(氧化反应)
正极:Ag2O + H2O + 2e-== 2Ag + 2OH-(还原反应)
化学方程式Zn + Ag2O + H2O ==Zn(OH)2+2Ag
8、铝-空气-海水(负极--铝、正极--石墨、铂网等能导电的惰性材料、电解液--海水)
负极 :4Al-12e-==4Al3+(氧化反应)
正极:3O2+6H2O+12e-==12OH-(还原反应)
总反应式为: 4Al+3O2+6H2O===4Al(OH)3(铂网增大与氧气的接触面)
9、镁---铝电池(负极--Al、正极--Mg电解液KOH)
负极(Al): 2Al + 8OH--+6e-= 2AlO2-+4H2O(氧化反应)
正极(Mg): 6H2O + 6e-= 3H2↑+6OH-(还原反应)
化学方程式: 2Al + 2OH-+ 2H2O = 2AlO2-+ 3H2
10、锂电池一型:(负极--金属锂、正极--石墨、电解液LiAlCl4-SOCl2)
负极 :8L i-8e-=8L i+(氧化反应)
正极:3SOCl2+8e-=SO32-+2S+6Cl-(还原反应)
化学方程式8L i+ 3SOCl2=== L i2SO3+6L iCl + 2S,
二次电池(又叫蓄电池或充电电池)
1、铅蓄电池:(负极—Pb正极—PbO2电解液— 浓硫酸)
放电时
负极:Pb-2e-+SO42-=PbSO4(氧化反应)
正极: PbO2+2e-+4H++SO42-=PbSO4+2H2O (还原反应)
充电时
阴极:PbSO4+2H++2e-==Pb+H2SO4(还原反应)
阳极: PbSO4+2H2O-2e-==PbO2+H2SO4+2H+ (氧化反应)
总化学方程式Pb+PbO2+2H2SO4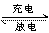 2PbSO4+2H2O
2PbSO4+2H2O
2、铁--镍电池:(负极-- Fe 、正极—NiO2、电解质溶液为KOH溶液)
放电时负极: Fe-2e-+ 2OH-==Fe (OH)2(氧化反应) 正极:NiO2+2H2O +2E—== Ni(OH)2+2OH-(还原反应)
充电时阴极: Fe (OH)2+2e-== Fe+ 2OH-(还原反应) 阳极: Ni(OH)2-2e—+ 2OH-==NiO2+2H2O(氧化反应)
总化学方程式Fe +NiO2+2H2O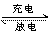 Fe (OH)2+Ni(OH)2
Fe (OH)2+Ni(OH)2
3、LiFePO4电池(正极—LiFePO4,负极—石墨,含Li+导电固体为电解质)
放电时
负极:Li -e-==Li+(氧化反应)
正极:FePO4+L i++e-== L iFePO4(还原反应)
充电时:
阴极:Li++e-== L i(还原反应)
阳极:LiFePO4-e-== FePO4+L i+(氧化反应)
总化学方程式FePO4+L i LiFePO4
LiFePO4
4、镍--镉电池(负极--Cd、正极—NiOOH、电解质溶液为KOH溶液)
放电时
负极: Cd-2e-+ 2OH-==Cd(OH)2(氧化反应)
正极: 2NiOOH +2E—+ 2H2O==2Ni(OH)2+2OH-(还原反应)
充电时
阴极: Cd(OH)2+2e-==Cd+ 2OH-(还原反应)
阳极:2 Ni(OH)2-2e-+ 2OH-== 2NiOOH + 2H2O(氧化反应)
总化学方程式Cd + 2NiOOH + 2H2O Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
5、氢--镍电池:(负极-LaNi5储氢合金、正极—NiOOH、电解质KOH+LiOH)
放电时
负极:LaNi5H6-6e-+ 6OH-==LaNi5+6H2O(氧化反应)
正极: 6NiOOH+6e-+ 6H2O==6Ni(OH)2+6OH-(还原反应)
充电时
阴极:LaNi5+6e-+ 6H2O==LaNi5H6+6OH-(还原反应)
阳极:6Ni(OH)2-6e-+ 6OH-==6NiOOH+ 6H2O(氧化反应)
总化学方程式LaNi5H6+6NiOOH LaNi5+6Ni(OH)2
LaNi5+6Ni(OH)2
6、高铁电池:(负极—Zn、正极---石墨、电解质为浸湿固态碱性物质)
放电时
负极:3Zn-6e-+ 6 OH-== 3 Zn(OH)2(氧化反应)
正极:2FeO42—+6e-+ 8H2O==2Fe (OH)3+10OH-(还原反应)
充电时
阴极:3Zn(OH)2+6e-==3Zn + 6 OH-(还原反应)
阳极:2Fe(OH)3-6e-+ 10OH-==2FeO42—+ 8H2O(氧化反应)
总化学方程式 3Zn + 2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
7、锂电池二型(负极LiC6、正极含锂的二氧化钴LiCOO2、充电时LiCOO2中Li被氧化,Li+还原以Li原子形式嵌入电池负极材料碳C6中,以LiC6表示)
放电时
负极:LiC6- xe-= L i(1-x)C6+x L i+(氧化反应)
正极: L i(1-x)CoO2+xe-+ x L i+== L iCoO2(还原反应)
充电时
阴极:Li(1-x)C6+x L i++xe-=LiC6(还原反应)
阳极:LiCoO2- xe-= L i(1-x)CoO2+x L i+(氧化反应)
总反应方程式Li(1-x)CoO2+L iC6 LiCOO2+Li(1-x)C6
LiCOO2+Li(1-x)C6
燃料电池
根据题意叙述书写常见于燃料电池,由于燃料电池的优点较多,成为了近年高考的方向。燃料电池是原电池中一种比较特殊的电池,它与原电池形成条件有一点相悖,就是不一定两极是两根活动性不同的电极,也可以用相同的两根电极。解决此类问题必须抓住一点:燃料电池反应实际上等同于燃料的燃烧反应,但要特别注意介质对产物的影响。
一、氢氧燃料电池
氢氧燃料电池一般是以惰性金属铂(Pt)或石墨做电极材料,负极通入H2,正极通入 O2,总反应为:2H2+O2=== 2H2O电极反应特别要注意电解质,有下列三种情况:
1、电解质是KOH溶液(碱性电解质)
负极:H2- 2e-+ 2OH-=== 2H2O(氧化反应)
正极:O2+H2O + 4e-===OH-(还原反应)
总反应方程式2H2+O2=== 2H2O
2、电解质是H2SO4溶液(酸性电解质)
负极:H2-2e-=== 2H+(氧化反应)
正极:O2+4H++ 4e-=== 2H2O(还原反应)
总反应方程式2H2+O2=== 2H2O
3、电解质是NaCl溶液(中性电解质)
负极:H2- 2e-=== 2H+(氧化反应)
正极:O2+H2O + 4e-=== 4OH-
总反应方程式2H2+O2=== 2H2O
说明
1、碱性溶液反应物、生成物中均无H+
2、.水溶液中不能出现O2-
3、中性溶液反应物中无H+和OH-
4、酸性溶液反应物、生成物中均无OH-
二、甲醇燃料电池
1.碱性电解质(铂为两极、电解液KOH溶液)
正极:3O2+12e-+ 6H20=== 12OH-(还原反应)
负极:2CH3OH -12e-+16OH—===2CO32-+12H2O(氧化反应)
总反应方程式2CH3OH + 3O2+4KOH=== 2K2CO3+6H2O
2. 酸性电解质(铂为两极、电解液H2SO4溶液)
正极:3O2+12e-+ 12H+== 6H2O(还原反应)(注:乙醇燃料电池与甲醇)
负极:2CH3OH -12e-+2H2O==12H++2CO2(氧化反应)燃料电池原理基本相)
总反应式2CH3OH + 3O2=== 2CO2+4H2O(氧化反应)
三、CO燃料电池(总反应方程式均为:2CO + O2= 2CO2)
1、熔融盐(铂为两极、Li2CO3和Na2CO3的熔融盐作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气)
正极:O2+4e-+ 2CO2= 2CO32--(还原反应)
负极:2CO+2CO32-- 4e-==4CO2(氧化反应)
2、酸性电解质(铂为两极、电解液H2SO4溶液)
正极: O2+4e-+ 4H+== 2H2O(还原反应)
负极: 2CO - 4e-+ 2H2O ==2CO2+4H+(氧化反应)
四、肼燃料电池(铂为两极、电解液KOH溶液)
正极:O2+2H2O + 4e-== 4OH—(还原反应)
负极: N2H4+4OH——4e-== N2+4H2O(氧化反应)
总反应方程式N2H4+O2=== N2+2H2O
五、甲烷燃料电池
1.碱性电解质(铂为两极、电解液KOH溶液)
正极: 2O2+2H2O + 8e-== 8 OH—(还原反应)
负极: CH4+10OH—-- 8e-== CO32-+ 7H2O(氧化反应)
总反应方程式CH4+2KOH+ 2O2=== K2CO3+3H2O
2、酸性电解质(铂为两极、电解液H2SO4溶液)
正极: 2O2+8e-+ 8H+== 4H2O(还原反应)
负极: CH4- 8e-+ 2H2O == 8H++ CO2(氧化反应)
总反应方程式CH4+2O2=== CO2+2H2O
六、丙烷燃料电池(铂为两极、正极通入O2和CO2、负极通入丙烷、电解液有三种)
1、电解质是熔融碳酸盐(K2CO3或Na2CO3)
正极: 5O2+20e-+ 10CO2== 10CO32-(还原反应)
负极: C3H8—20e-+ 10CO32-== 3CO2+4H2O(氧化反应)
总反应方程式C3H8+5O2=== 3CO2+4H2O
2、酸性电解质 (电解液H2SO4溶液)
正极:5O2+20e-+26H+== 10H2O(还原反应) 负极: C3H8- 20e-+ 6H2O == 3CO2 + 20 H+(氧化反应)
总反应方程式C3H8+5O2=== 3CO2+4H2O
3、碱性电解质(铂为两极、电解液KOH溶液)
正极 : 5O2+20e-+ 10H2O == 20OH—(还原反应)
负极: C3H8—20e-+26 OH—== 3CO32-+ 17H2O(氧化反应)
总反应方程式C3H8+5O2+6KOH === 3 K2CO3+7H2O
七、乙烷燃料电池(铂为两极、电解液KOH溶液)
正极 :7O2+28e-+ 14H2O == 28OH-(还原反应)
负极: 2C2H6—28e-+36 OH-== 4CO32-+24H2O(氧化反应)
总反应方程式2C2H6+7O2+8KOH=== 4K2CO3+10H2O

- 全部评论(0)
