氨气溶于水会不会促进水的电离?还是抑制?
时间:2019-08-24 09:12 来源:未知 作者:化学自习室 点击: 次 所属专题: 水的电离
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
氨气溶于水抑制水的电离。
该体系内有两个化学平衡:
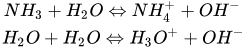
氨气与水反应,生成氢氧根离子并消耗水。直观来看,体系pH上升表明氢氧根离子的浓度有了数量级的改变;而由于是水溶液体系,水的消耗是可以忽略不计的。因此,水的电离平衡中产物增加,反应物基本不变,根据勒夏特列原理,平衡左移,水的电离被抑制。
定性来看,根据体系电荷守恒
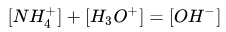
水的电离平衡

有
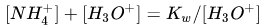
因此
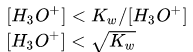
水合氢离子浓度降低。而水合氢离子只参与水的电离平衡反应,因此其浓度降低表征水的电离被抑制。
定量来看,根据体系电荷守恒、物料守恒和两个化学平衡,
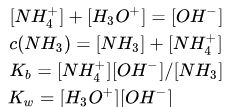
可以推得
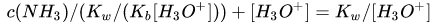
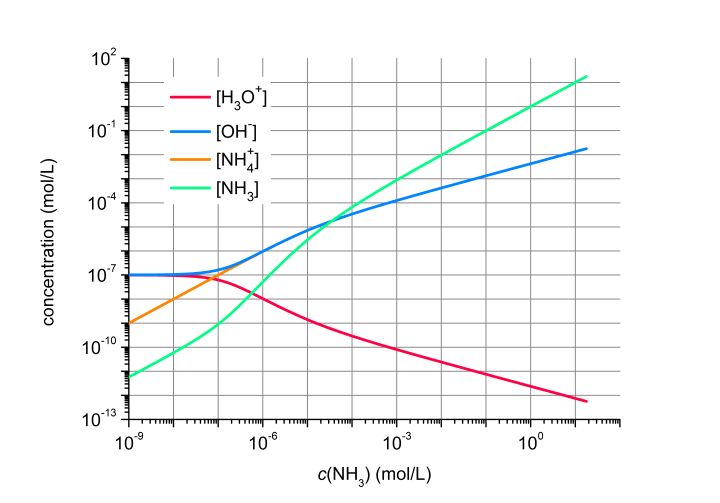
即水合氢离子浓度(或水的电离度)是初始氨气浓度(单位体积内溶解的氨气的物质的量)的一个函数。在合理的浓度范围内画出该函数,可以看到随着氨气溶解,水合氢离子浓度下降,水的电离程度下降,水的电离被抑制。
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
(1225944015) 评论 href="/plus/view.php?aid=17527">氨气溶于水会不会促:那么CO32-+H2O =HCO3-+OH -不也会抑制水电离了?
还没有评论,快来抢沙发吧!
