题型突破—电解质溶液
时间:2020-03-10 12:39 来源:未知 作者:化学自习室 点击: 次 所属专题: 电解质溶液
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、弱电解质的电离平衡
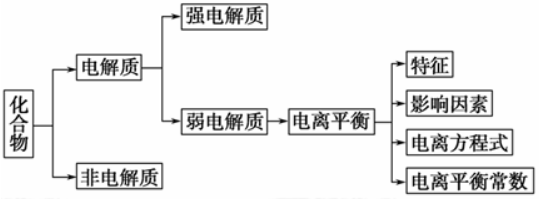
注意:
①能够导电的物质不一定全是电解质,如Cu、氯水等。
②电解质必须在水溶液里或熔化状态下才能有自由移动的离子。
③电解质和非电解质都是化合物,单质既不是电解也不是非电解质。
④溶于水或熔化状态;注意:“或”字。
⑤溶于水和熔化状态两各条件只需满足其中之一,溶于水不是指和水反应。
⑥电解质和非电解质必须是化合物,对于不是化合物的物质既不是电解质也不是非电解质。
⑦溶液的导电能力强弱取决于溶液中离子浓度的大小和离子所带电荷的多少,离子浓度越大,离子所带的电荷越多,溶液的导电性越强。若强电解质溶液中离子浓度很小,而弱电解质溶液中离子浓度大,则弱电解质溶液的导电能力强,因此电解质的强弱与电解质溶液的导电性并无必然联系。
⑧强电解质不一定易溶于水,如难溶的CaCO3、BaSO4都是难溶于水的,但溶于水的部分全部电离,因此硫酸钡、碳酸钡都是强电解质;易溶于水的也不一定是强电解质,如醋酸等,故电解质的强、弱与溶解性无必然联系。
⑨“电解”“电离”和“通电”的区别:“电解”指在通电条件下,电解质发生氧化还原反应,而“电离”是在水溶液中或熔化状态下电解质离解成自由移动离子的过程,没有发生氧化还原反应;“通电”指接通电源,它是电解反应的条件。
方法技巧:
判断弱电解质的四个思维角度
角度一:
依据物质的类别进行判断:在没有特殊说明的情况下,就认为盐是强电解质,强酸(HCl、H2SO4、HNO3)、强碱[NaOH、KOH、Ba(OH)2、Ca(OH)2]为强电解质;而常见的弱酸、弱碱为弱电解质,如H2CO3、H2SO3、HClO、H2SiO3、NH3·H2O等。
角度二:
弱电解质的定义,即弱电解质不能完全电离,如测0.1mol·L-1的CH3COOH溶液的pH>1。
角度三:
弱电解质溶液中存在电离平衡,条件改变,平衡移动,如pH=1的CH3COOH加水稀释10倍1<pH<2。(见下表)
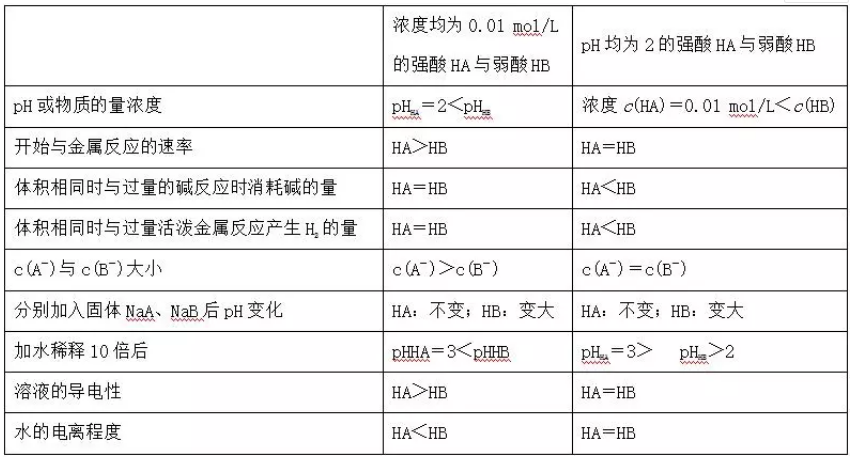
角度四:
弱电解质形成的盐类能水解,如判断CH3COOH为弱酸可用下面两个现象:
①配制某浓度的醋酸钠溶液,向其中加入几滴酚酞试液。现象:溶液变为浅红色。
②用玻璃棒蘸取一定浓度的醋酸钠溶液滴在一小块pH试纸上,测其pH,现象:pH>7。
二、水的电离及溶液的酸碱性
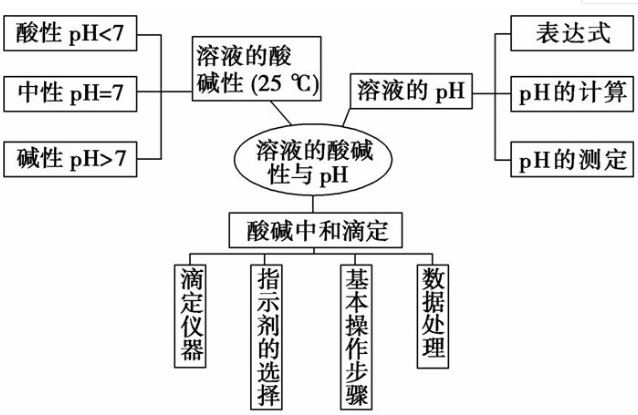
注意:
(1)Kw只受温度影响,改变其他条件水的电离程度会发生变化,但只要温度不变,则Kw不变。
(2)水的离子积是水电离平衡时的性质,不仅适用于纯水,也适用于酸性或碱性的稀溶液。不管哪种溶液均有c(H+)水=c(OH-)水。即任何稀水溶液中都存在这一关系。因此,在酸溶液中酸本身电离出来的H+会抑制水的电离,c(H+)酸·c(OH-)水=Kw;而在碱溶液中,碱本身电离出来的OH-也会抑制水的电离,c(OH-)碱·c(H+)水=Kw。
(3)外界条件改变,水的电离平衡发生移动,但任何时候由水电离出的H+和OH-总是相等的。如Na2CO3溶液中OH-全部由水电离产生,而水电离产生的H+除一部分存在于溶液中,其他则存在于HCO3-和H2CO3中。故有c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)。
(4)水的离子积常数表示在任何水溶液中均存在水的电离平衡,都有H+和OH-共存,只是相对含量不同而已。并且在稀酸或稀碱溶液中,当温度为25 ℃时,Kw=c(H+)·c(OH-)=1×10-14mol2·L-2为同一常数。
(5)溶液中的c(H+)和水电离出来的c(H+)是不同的:
①常温下水电离出的c(H+)=1×10-7mol·L-1,若某溶液中水电离出的c(H+)<1×10-7mol·L-1,则可判断出该溶液中加入了酸或碱抑制了水的电离;若某溶液中水电离出的c(H+)>1×10-7mol·L-1,则可判断出该溶液中加入了可以水解的盐或活泼金属促进了水的电离。
②常温下溶液中的c(H+)>1×10-7mol·L-1,说明该溶液是酸溶液或水解显酸性的盐溶液;c(H+)<1×10-7mol·L-1,说明是碱溶液或水解显碱性的盐溶液。
方法技巧
1、误差分析:
(1)原理(以标准盐酸滴定待测NaOH溶液为例):
cB=![]() ;
;
VB——准确量取的待测液的体积;
cA——标准溶液的浓度。
故有:cB正比于VA。
(2)常见误差

2、有关溶液酸碱性的判断和pH的计算:
(1)水电离的c(H+)或c(OH-)的计算(25 ℃)
①中性溶液:c(H+)=c(OH-)=1.0×10-7mol·L-1。
②溶质为酸的溶液:H+来源于酸电离和水电离,而OH-只来源于水。如计算pH=2的盐酸中水电离出的c(H+):方法是先求出溶液中的c(OH-)=10-12mol/L,即水电离出的c(H+)=c(OH-)=10-12mol/L。
③溶质为碱的溶液:OH-来源于碱电离和水电离,而H+只来源于水。如pH=12的NaOH溶液中,c(H+)=10-12mol·L-1,即水电离产生的c(OH-)=c(H+)=10-12mol·L-1。
④水解呈酸性或碱性的盐溶液:H+和OH-均由水电离产生。如pH=2的NH4Cl溶液中由水电离出的c(H+)=10-2mol·L-1;如pH=12的Na2CO3溶液中由水电离出的c(OH-)=10-2mol·L-1。
(2)关于pH的计算:
①总体原则:若溶液为酸性,先求c(H+),再求pH=-lgc(H+);若溶液为碱性,先求c(OH-),再求
c(H+)=Kw/c(OH-),最后求pH。
②pH计算的一般思维模型:
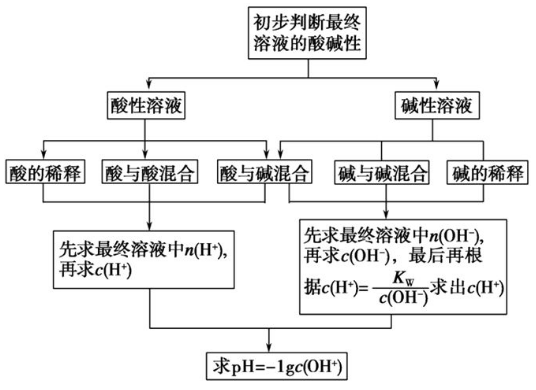
4、解答酸碱中和滴定图像三要素:
(1)酸碱中和反应要有“量”的思想,复习中着重对“两平衡、三守恒”即水解平衡、电离平衡,电荷守恒、物料守恒和质子守恒进行分析;
(2)观察图像的变化趋势;
(3)把图像中的有效信息和具体的反应结合起来,作出正确的判断。
三、盐类水解
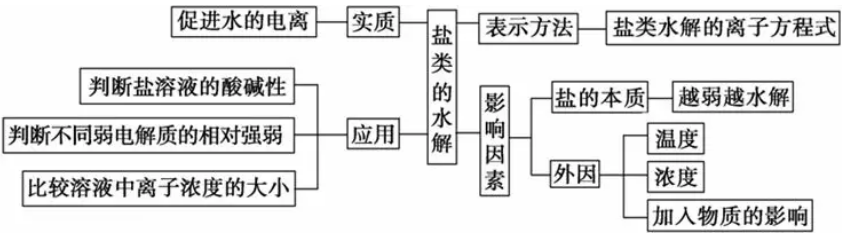
注意:
(1)强酸的酸式盐只电离,不水解,溶液显酸性。如NaHSO4在水溶液中:NaHSO4=Na++H++SO42-。
(2)弱酸的酸式盐溶液的酸碱性,取决于酸式酸根离子的电离程度和水解程度的相对大小。
①若电离程度小于水解程度,溶液呈碱性。如NaHCO3溶液中:HCO3-⇌H++CO32-(次要),HCO3-+H2O⇌H2CO3+OH-(主要)。
②若电离程度大于水解程度,溶液显酸性。如NaHSO3溶液中:HSO3-⇌H++SO32-(主要),HSO3-+H2O⇌H2SO3+OH-(次要)。
(3)相同条件下的水解程度:正盐>相应酸式盐,如CO32->HCO3-。
(4)相互促进水解的盐>单独水解的盐>水解相互抑制的盐。如NH4+的水解:(NH4)2CO3>(NH4)2SO4>(NH4)2Fe(SO4)2。
方法技巧
1、盐溶液酸、碱性的四种判断方法:
(1)强酸与弱碱生成的盐水解,溶液呈酸性。
(2)强碱与弱酸生成的盐水解,溶液呈碱性。
(3)强酸强碱盐不水解,溶液呈中性。
(4)强酸弱碱盐,其水解程度大于(1)(2)两类,有的甚至水解完全。具体有三种情况:
①生成的弱酸电离程度大于生成的弱碱的电离程度,溶液呈酸性,如NH4F;
②生成的弱酸电离程度小于生成的弱碱的电离程度,溶液呈碱性,如NH4HCO3;
③生成的弱酸和弱碱的电离程度相同,溶液呈中性,如CH3COONH4。
2、蒸干盐溶液所得物质的判断方法:
(1)先考虑分解。如NaHCO3溶液、Ca(HCO3)2溶液蒸干灼烧得Na2CO3、CaCO3;KMnO4溶液蒸干灼烧得K2MnO4和MnO2。
(2)考虑氧化还原反应。如加热蒸干Na2SO3溶液,所得固体为Na2SO4。
(3)强酸弱碱盐水解生成挥发性酸的,蒸干后得到弱碱,水解生成不挥发性酸的,得到原物质。如AlCl3溶液蒸干得氢氧化铝,再灼烧得Al2O3;Al2(SO4)3溶液蒸干得本身。
(4)弱酸强碱正盐溶液蒸干得到原物质,Na2CO3溶液蒸干得本身。
(5)NH4Cl溶液、(NH4)2S溶液蒸干、灼烧,无残留物。
(6)某些金属氯化物的结晶水合物,如MgCl2·6H2O和FeCl3·6H2O,在空气中加热时易发生水解,为得到其无水盐,通常将其结晶水合物在氯化氢气流中加热,以防止其水解。如MgCl2·6H2O=(HCl气流)=MgCl2+6H2O。
3、溶液中微粒浓度大小的比较:
(1)微粒浓度大小比较的理论依据和守恒关系:
①两个理论依据:弱电解质电离理论:电离微粒的浓度大于电离生成微粒的浓度。例如,H2CO3溶液中:c(H2CO3)>c(HCO3-)≫c(CO32-)(多元弱酸第一步电离程度远远大于第二步电离)。
②水解理论:水解离子的浓度大于水解生成微粒的浓度。例如,Na2CO3溶液中:c(CO32-)>c(HCO3-)≫c(H2CO3)(多元弱酸根离子的水解以第一步为主)。
(2)三个守恒关系:
①电荷守恒:电荷守恒是指溶液必须保持电中性,即溶液中所有阳离子的电荷总浓度等于所有阴离子的电荷总浓度。例如,NaHCO3溶液中:c(Na+)+c(H+)===c(HCO3-)+2c(CO32-)+c(OH-)。
②物料守恒:物料守恒也就是原子守恒,变化前后某种元素的原子个数守恒。例如,0.1 mol·L-1NaHCO3溶液中:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)=0.1 mol·L-1。
③质子守恒:由水电离出的c(H+)等于由水电离出的C(OH-),在碱性盐溶液中OH-守恒,在酸性盐溶液中H+守恒。例如,纯碱溶液中c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)。
(3)四种情况分析:
①多元弱酸溶液:根据多步电离分析,如:在H3PO3溶液中,c(H+)>c(H2PO4-)>c(HPO42-)>c(PO43-)。
②多元弱酸的正盐溶液:根据弱酸根的分步水解分析,如:Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)。
③不同溶液中同一离子浓度的比较:要看溶液中其他离子对其产生的影响。例如,在相同物质的量浓度的下列溶液中:①NH4NO3溶液,②CH3COONH4溶液,③NH4HSO4溶液,C(NH4+)由大到小的顺序是③>①>②。
④混合溶液中各离子浓度的比较:要进行综合分析,如电离因素、水解因素等。即:
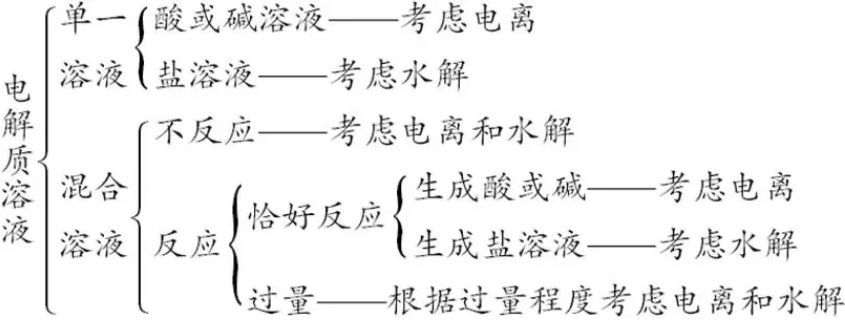
(4)离子浓度大小比较的解题思路:

(5)平衡移动原理解释问题的思维模板:
①解答此类题的思维过程:找出存在的平衡体系(即可逆反应或可逆过程);找出影响平衡的条件;判断平衡移动的方向;分析平衡移动的结果及移动结果与所解答问题的联系。
②答题模板:……存在……平衡,……(条件)……(变化),使平衡向……(方向)移动,……(结论)。
例如:把AlCl3溶液蒸干灼烧,最后得到的主要固体是什么?为什么?(用化学方程式表示并配以必要的文字说明)。
在AlCl3溶液中存在着如下平衡:AlCl3+3H2O⇌Al(OH)3+3HCl,加热时水解平衡右移,HCl浓度增大,蒸干时HCl挥发,使平衡进一步向右移动得到Al(OH)3,在灼烧时发生反应2Al(OH)3![]() Al2O3+3H2O,因此最后得到的固体是Al2O3。
Al2O3+3H2O,因此最后得到的固体是Al2O3。
四、溶解平衡:
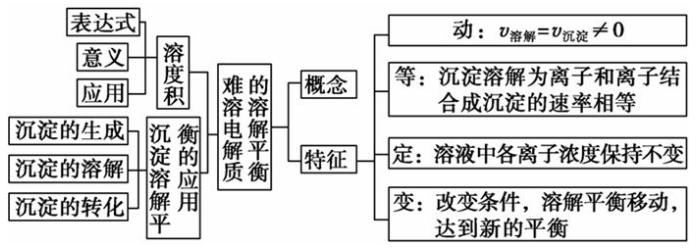
注意:
1、利用生成沉淀的方法不可能将要除去的离子全部通过沉淀除去。一般认为残留在溶液中的离子浓度小于1×10-5mol·L-1时,沉淀已经完全。
2、沉淀的转化过程中一般是溶解度大的易转化为溶解度小的,但在溶解度相差不大的情况下,溶解度小的也可以转化为溶解度大的,如BaSO4沉淀在饱和Na2CO3沉淀中可以转化为BaCO3沉淀。
方法技巧
1、溶度积与离子积的使用方法:以AmBn(s)⇌mAn+(aq)+nBm-(aq)为例:
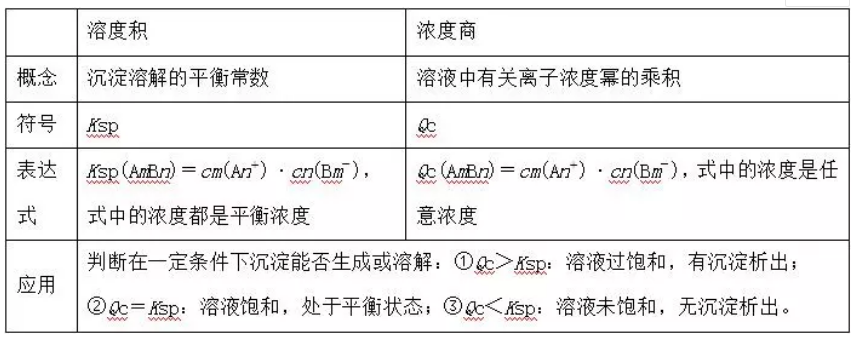
需要强调的是,若离子来源于不同溶液,则代入Q、Ksp中进行计算的离子浓度是指溶液混合后、反应前时的浓度,绝不是混合前的浓度。
2、三个强调:
(1)沉淀溶解平衡是化学平衡的一种,沉淀溶解平衡移动分析时也同样遵循勒·夏特列原理。
(2)溶度积大的难溶电解质的溶解度不一定大,只有组成相似的难溶电解质才有可比性。
(3)复分解反应总是向着某些离子浓度减小的方向进行,若生成难溶电解质,则向着生成溶度积较小的难溶电解质的方向进行。
3、电解质在水中的溶解度分类区间:20 ℃时,电解质在水中的溶解度大小的分类区间可形象的表示为:
![]()
4、Ksp的有关计算及其图像分析:
(1)溶度积的计算:
①已知溶度积求溶液中的某种离子的浓度,如Ksp=a的饱和AgCl溶液中c(Ag+)=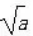 mol/L。
mol/L。
②已知溶度积、溶液中某离子的浓度,求溶液中的另一种离子的浓度,如某温度下AgCl的Ksp=a,在0.1 mol·L-1的NaCl溶液中加入过量的AgCl固体,达到平衡后c(Ag+)=10amol·L-1。
(2)图像分析:
①曲线上的任意一点,都代表指定温度下的饱和溶液,由对应的离子浓度可求Ksp。
②可通过比较、观察得出溶液是否达到饱和状态,是否有沉淀析出。处于曲线上方的点表明溶液处于过饱和状态,一定会有沉淀析出,处于曲线下方的点,则表明溶液处于未饱和状态,不会有沉淀析出。
③从图像中找到数据,根据Ksp公式计算得出Ksp的值。
④比较溶液的Qc与Ksp的大小,判断溶液中有无沉淀析出。
⑤涉及Qc的计算时,所代入的离子浓度一定是混合溶液中的离子浓度,因此计算离子浓度时,所代入的溶液体积也必须是混合液的体积。

- 全部评论(0)
