认识消毒剂及相关考点
时间:2020-03-10 14:27 来源:未知 作者:化学自习室 点击: 次 所属专题: 消毒剂
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、什么是消毒剂呢?
化学消毒剂是指用于杀灭传播媒介上病原微生物,使其达到无害化要求的制剂,不同于抗生素,它在防控中的主要作用是将病原微生物消灭于人体之外,切断传染病的传播途径,达到控制传染病的目的。
二、消毒剂有哪些种类呢?
常用的消毒剂产品按照成分可分为9种:
含氯消毒剂、过氧化物类消毒剂、醛类消毒剂、醇类消毒剂、含碘消毒剂、酚类消毒剂、环氧乙烷、双胍类消毒剂和季铵盐类消毒剂。
本内容重点讲解酒精和84消毒液。
84消毒液
84消毒液--次氯酸钠溶液
84消毒液的成分:以次氯酸钠(NaClO)为主要有效成分的消毒液,有效氯含量为 1.1%~1.3%,
84消毒液的作用:杀灭肠道致病菌、化脓性球菌和细菌芽孢。
84消毒液的适用范围:适用于一般物体表面、白色衣物、医院污染物品的消毒。
84消毒液的消毒原理:NaClO具有强氧化性,作漂白剂,其漂白原理是NaClO水解生成具有漂白性的 HClO(次氯酸)
ClO−+H2O⇌HClO+OH−,HClO具有强氧化性,能够将具有还原性的物质氧化,使其变性,因而能够起到消毒的作用。
空气中的CO2(二氧化碳)溶解于NaClO溶液中,可以与NaClO参加反应得到具有漂白性的HClO。
化学反应方程式为:NaClO+CO2+H2O=NaHCO3+HClO
次氯酸
HClO分子的结构式为H−O−Cl(氧元素位于中心位置),所以其电子式为
★弱酸性:
HClO是一种弱酸,其电离方程式为HClO⇌H++ClO−,与碳酸相比,其酸性强弱有如下关系:H2CO3>HClO。
★HClO具有强氧化性:
能与亚铁盐、碘化物、硫化物及亚硫酸盐等发生氧化还原反应,能杀菌消毒。
★HClO具有不稳定性:2HClO⇌2HCl+O2↑。
★漂白性:
能漂白有色物质,且漂白后颜色不能恢复。
84消毒液使用过程中的注意事项:
1.84消毒液有一定的刺激性与腐蚀性,必须稀释以后才能使用。
2.84消毒液的漂白作用与腐蚀性较强,最好不要用于衣物的消毒,必须使用时浓度要低,浸泡的时间不要太长。
3. 84消毒液是一种含氯消毒剂,而氯是一种挥发性的气体,因此盛消毒液的容器必须加盖盖好,否则达不到消毒的效果。
4.不要把84 消毒液与其他洗涤剂或消毒液混合使用,因为这样会加大空气中氯气的浓度而引起氯气中毒。
5.外用消毒液,不得口服,
6.本品对金属有腐蚀作用,对织物有漂白作用,慎用。
7.本品对皮肤有刺激性,使用时应戴手套,避免接触皮肤。
8。本品宜现用现配,一次性使用,勿用50°以上热水稀释。
9.使用时最好戴手套。
医用酒精
医用酒精是什么?
医用酒精是指医学上使用的酒精,医用酒精的纯度有多种,常见的为95%和75%。
酒精消毒的原理是什么?
酒精浓度越高杀菌效果越好吗?不是的。
75%的酒精之所以用于消毒。这是因为,过高浓度的酒精会在细菌表面形成一层保护膜,阻止其进入细菌体内,难以将细菌彻底杀死。若酒精浓度过低,虽可进入细菌,但不能将其体内的蛋白质凝固,同样也不能将细菌彻底杀死。
酒精分子有两个末端,一端是憎水的(−C2H5),可以破坏蛋白质内部憎水基团之间的吸引力;一端是亲水的(−OH),但它难以破坏蛋白质外部的亲水基团之间的吸引力。另一方面,水分子虽然可以松弛蛋白质亲水基团之间的吸引力,但它即使钻进细菌内部,也无法破坏其蛋白质中憎水基团之间的吸引力。
所以,纯酒精或水都不足以使细菌内的蛋白质变性,只有酒精和水共同存在,同时使保持蛋白质几何形状的各种吸引力松弛,蛋白质才会失去生理活性。因此,只有一定浓度的酒精溶液,才能达到良好的消毒杀菌目的。
乙醇和酒精什么关系?
酒精是乙醇的俗名,是一种常见有机物。
乙醇的分子式是C2H6O,结构式是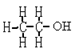 ,电子式为
,电子式为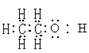 ,官能团是−OH(羟基),结构简式为C2H5OH或CH3CH2OH,乙醇是极性分子。
,官能团是−OH(羟基),结构简式为C2H5OH或CH3CH2OH,乙醇是极性分子。
球棍模型:
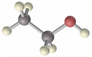 ,
,
比例模型
 。
。
工业上如何制备乙醇呢?
1.发酵法
含淀粉的农产品或含纤维素的木屑、植物茎秆等经一定的预处理后,经水解、发酵即可制得乙醇。
(1)淀粉在有催化剂存在和加热条件下发生水解反应,生成葡萄糖。
(C6H10O5)n+nH2O nC6H12O6
nC6H12O6
(2)葡萄糖在催化剂的作用下生成乙醇。
C6H12O6 2C2H5OH+2CO2↑
2C2H5OH+2CO2↑
2.乙烯水化法
(1)定义:乙烯在加热、加压和催化剂存在的条件下,跟水反应生成乙醇。(乙烯水化法)
(2)化学方程式为:CH2=CH2+H2O CH3CH2OH,属于加成反应。
CH3CH2OH,属于加成反应。
有关消毒剂考点预测
考点预测1--防病毒常识
1. 2019 年 12 月以来,我国部分地区突发的新型冠状病毒肺炎威胁着人们的身体健康。以下是人们在面对“新型冠状病毒肺炎”时的一些认识,你认为符合科学道理的是( )
A.家庭消毒时,消毒液越浓越好
B.吸烟、喝酒可以预防“新型冠状病毒”
C.应经常保持室内清洁卫生和通风
D.必须每天吃药,补充人体所需化学物质
2. 2019 年 12 月以来,我国部分地区突发的新型冠状病毒肺炎威胁着人们的身体健康。而根据国家卫健委高级别专家组成员李兰娟院士在记者会上透露:新型冠状病毒怕酒精,你认为符合科学道理的是( )
A.家庭消毒时,酒精越浓越好,最好使用纯酒精
B.家庭消毒时,酒精越稀越好
C.家庭消毒时,应该使用70%-75%的酒精
D.家庭消毒时,酒精和84消毒液可以混合用,这样消毒作用强
【答案】
1.C 2.C
考点预测2--次氯酸钠相关考点
1.2019 年 12 月以来,我国部分地区突发的新型冠状病毒肺炎威胁着人们的身体健康。已知该病毒对化学药品敏感,乙醇、高锰酸钾溶液、次氯酸钠溶液、双氧水等消毒剂可以完全灭活病毒感染性.下列有关说法正确的是( )
A.乙醇、次氯酸钠溶液的消毒原理相同
B.双氧水和次氯酸钠具有较强的腐蚀性,不能用于皮肤的消毒
C.高锰酸钾溶液和双氧水均可以将病毒氧化而达到消毒的目的
D.在次氯酸钠溶液中通入少量二氧化硫可发生反应:2NaClO+SO2+H2O=Na2SO3+HClO
【答案】C
解析
A.乙醇消毒液消毒是因为可以使蛋白质变性,而并非是将病毒氧化,而次氯酸钠溶液可以将病毒氧化而达到消毒的目的,故A错误;
B.双氧水具有较强的氧化性,能用于皮肤的消毒,故B错误;
C.高锰酸钾溶液和双氧水的消毒原理都是因为具有强氧化性,原理相同,故C正确;
D.次氯酸钠溶液中通入少量二氧化硫生成硫酸根离子和水,故D错误;
故选C.
补充练习
题1:潮湿的氯气、新制的氯水、次氯酸钠及漂粉精的水溶液均能使有色布条褪色,因为它们都含有微粒( )
A.Cl2 B.HClO C.ClO− D.HCl
题2:将一定量的氯气通入30mL浓度为10.00mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成氯化钠、次氯酸钠、氯酸钠共存体系.下列判断正确的是( )
A.与氢氧化钠反应的氯气一定为0.16mol
B.n(Na+):n(Cl−)可能为7:3
C.若反应中转移的电子为nmol,则0.15<n<0.25
D.n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1
解析:
A.由于反应后体系中没有NaOH,故氢氧化钠反应完,根据钠元素守恒n(NaOH)=n(NaCl)+n9NaClO)+n(NaClO3)=0.03L×10mol/L=0.3mol,根据氯原子守恒有2n(Cl2)=n(NaCl)+n(NaClO)+n(NaClO3)=0.3mol,故参加反应的氯气n(Cl2)=0.15mol,故A错误;
B.根据方程式Cl2+2NaOH=NaCl+NaClO+H2O、3Cl2+6NaOH=5NaCl+NaClO3+3H2O可知,氧化产物只有NaClO,n(Na+):n(Cl−)最大为2:1,当氧化产物为NaClO3,n(Na+):n(Cl−)最小为6:5,故6:5<n(Na+):n(Cl−)<2:1,7:3>2:1,故B错误;
C.根据方程式Cl2+2NaOH=NaCl+NaClO+H2O、3Cl2+6NaOH=5NaCl+NaClO3+3H2O可知,氧化产物只有NaClO,转移电子数最少,为0.3mol×0.5×1=0.15mol,氧化产物只有NaClO3,转移电子数最多,为0.3mol×5/6×1=0.25mol,则0.15<n<0.25,故C正确;
D.令n(NaCl)=11mol,n(NaClO)=2mol,n(NaClO3)=1mol,生成NaCl获得的电子为11mol×1=11mol,生成NaClO、NaClO3失去的电子为2mol×1+1mol×5=7mol,得失电子不相等,故D错误;
故选C.
题3:84消毒液(有效成分是次氯酸钠)、漂白粉(有效成分是次氯酸钙)等物质是日常生活中常用的消毒剂,广泛应用于日常生活中。根据下列要求回答相关问题:
(1)在0.1mol⋅L−1的84消毒液中滴加几滴酚酞试液,可能观察到的现象是,写出反应的离子方程式: 。
(2)某同学测定漂白粉溶液pH的操作方法:将一小块pH试纸放在表面皿上,用玻璃棒蘸取少量待测液滴在试纸上,大约半分钟后,再与标准比色卡对照。你认为他能否达到实验目的?(填′′能′′或′′否′′)。
(3)下列关于0.5mol⋅L−1NaClO溶液中各粒子浓度的关系式正确的是。
A.c(OH−) > c(H+) > c(Na+) > c(ClO−)
B. c(Na+)= c(ClO−) + c(HClO)
C.c(Na+) > c(ClO−) > c(OH−)> c(H+)
D.c(Na+) + c(H+)= c(ClO−)
解析:
1:次氯酸钠溶液具有强氧化性,次氯酸根离子水解溶液显碱性,则在0.1mol⋅L−1的84消毒液中滴加几滴酚酞试液,可能观察到的现象是溶液颜色先变红后褪色,反应的离子方程式为ClO−+H2O⇌HClO+OH−。
2:由于次氯酸钙溶液具有强氧化性,能漂白酸碱指示剂,因此不能用pH试纸测其pH。
3:A.次氯酸根离子水解溶液显碱性,则c(Na+)> c(ClO−)> c(OH−)> c(H+),A错误;B.根据物料守恒可知c(Na+)= c(ClO−)+ c(HClO),B正确;C.次氯酸根离子水解溶液显碱性,则c(Na+)> c(ClO−)> c(OH−)> c(H+),C正确;D.根据电荷守恒可知 c(Na+)+ c(H+)= c(ClO−)+ c(OH−),D错误,答案选BC。
考点预测3--乙醇
题4:下列酒类,其中酒精含量最高的是( )
A. 啤酒 B.白酒 C.葡萄酒 D.黄酒
解析:
啤酒酒精含量一般约3%,葡萄酒的一般酒精含量不过14%,黄酒的酒精度一般在14%~20%,属于低度酿造酒,白酒一般30%以上,所以其中酒精含量最高的是白酒,故选:B。
题5 :下列有关乙醇物理性质的应用中不正确的是( )
A.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中药的有效成分
B.由于乙醇能够与水以任意比例互溶,所以酒厂可以勾兑各种浓度的酒
C.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
D.由于乙醇容易挥发,所以才有“酒香不怕巷子深”的说法
解析:
A、有机物易溶于有机物,则乙醇能够溶解很多有机物和无机物,可用乙醇提取中药的有效成分,故A正确;
B、乙醇与水可形成氢键,以任意比例互溶,则酒厂可以勾兑各种浓度的酒,故B正确;
C、乙醇与水互溶,不能选分液除去乙醇中的水,故C错误;
D、乙醇易挥发,远处可闻到乙醇的香味,则才有“酒香不怕巷子深”的说法,故D正确;

- 全部评论(0)
