有机化学基础讲座:卤代烃主要性质介绍
时间:2020-12-04 08:24 来源:未知 作者:化学自习室 点击: 次 所属专题: 卤代烃
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
卤原子取代了烃分子中的氢而生成的衍生物,总称为卤代烃。 它们并不存在于自然界,而是经过合成方法制造出来的。一般说 来,卤代烃的性质比母体烃活泼,能进行多种化学反应。卤代经 分子中的卤素称为“官能团”。
第一节:卤代轻的分类
卤代烃因烃基的不同可以分为脂肪族卤代烃、脂环族卤代烃 和芳香族卤代烃,例如:
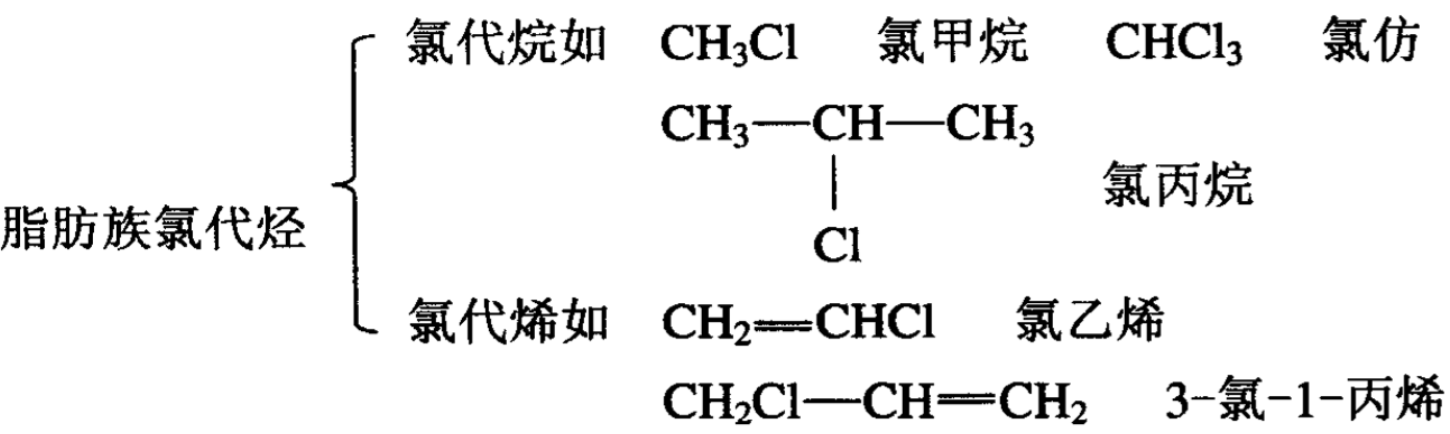
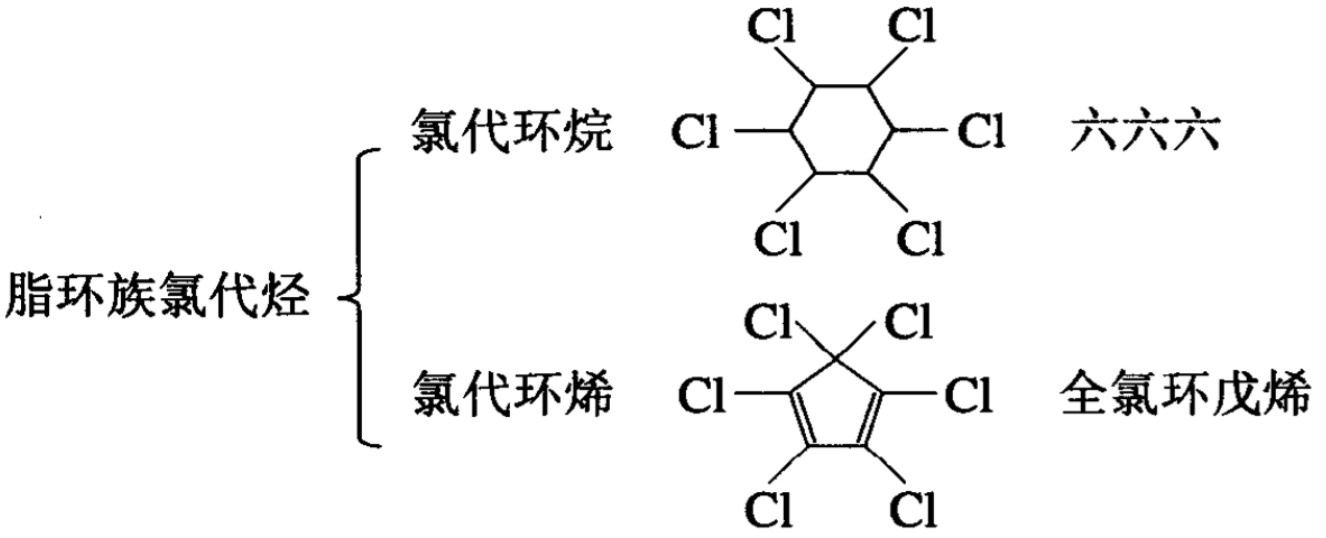
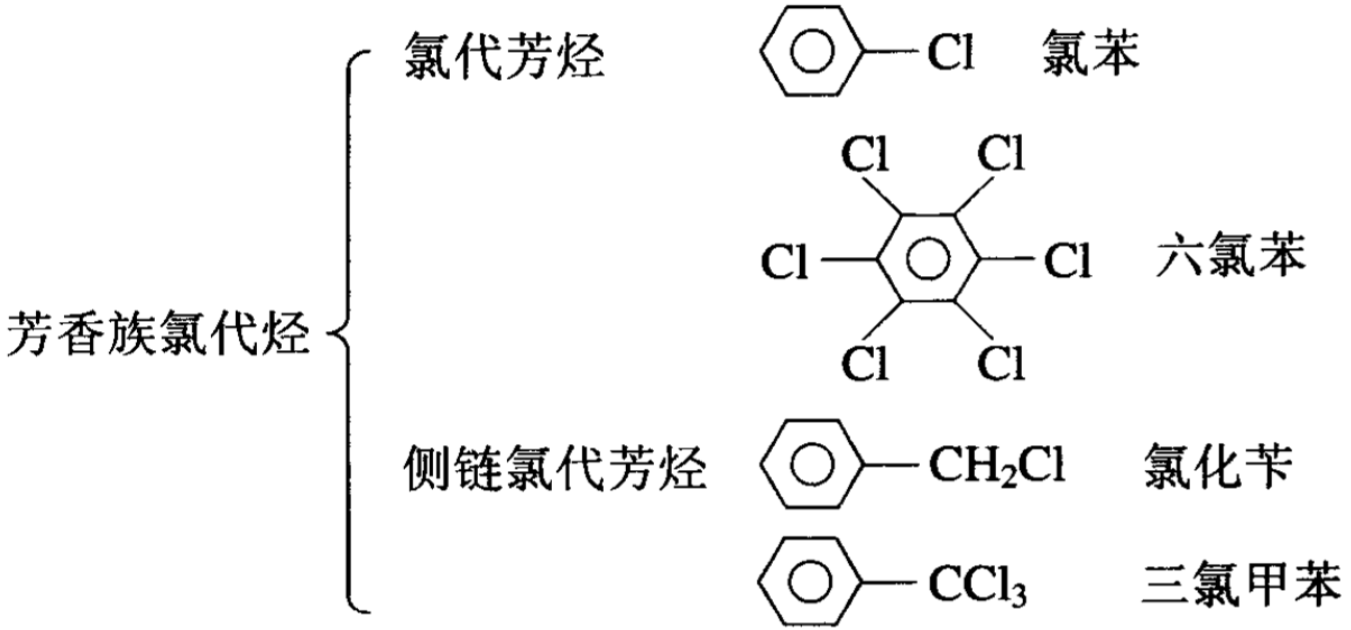
卤代烃的名称一般随母体烃。卤原子在烃分子中的地位决定 了卤素的化学活性。
第二节:氯甲烷和多氯甲烷
甲烷和氯气在光照射下发生强烈的氯代反应,并放出大量热, 比较难控制,产物中有一氯甲烷、二氯甲烷、三氯甲烷(氯仿)、 四氯化碳,还有碳。工业上釆用直接氯代方法比较困难,它的工 业化还是近年的事。少量生产氯甲烷从甲醇开始:
![]()
三氯甲烷和四氯化碳从二硫化碳开始:
![]()
四氯化碳用铁还原得氯仿:
![]()
大规模生产这些氯甲烷和多氯甲烷应以甲烷为原料。
甲烷和氯气的混合物在室温下和黑暗中可以长期保存不起反 应,其情况和氢气相似。只是在外部的引发下,例如光照和加热才能使甲烷和氯发生反应。只光照甲烷不光照氯气不能起动反应, 但是只光照氯气而不光照甲烷却仍能起反应,这说明起反应的关键是在氯。
随着分子中氯原子的增多,氯甲烷、氯仿、四氯化碳的沸点 升高,密度增大,见下表。
氯甲烷、氯仿、四氯化碳的性质
名称 | 分子式 | 沸点, | 密度,g/cm3 | 用途 |
氯甲烷 | CH3Cl | -23.7 | 0.992 | 可用作冷冻剂 |
二氯甲烷 | CH2Cl2 | 42 | 1.325 | 可作溶剂不着火 |
氯仿 | CHCl3 | 61 | 1.490 | 麻醉剂 |
四氯化碳 | CCl4 | 76 | 1.594 | 灭火剂 |
这些氯代甲烷都不溶于水,有香味,能够溶解许多有机化 合物。
第三节:氯乙烯
在乙烯分子中氯取代一个氢原子就形成氯乙烯。我国化学工 业生产氯乙烯主要是用于生产聚氯乙烯塑料。
氯乙烯的制法分两条路线,一条是以乙炔为原料,另一条是 以乙烯为原料。现在我国大多数工厂釆用的是前条路线,由于 石油裂解气能提供便宜的乙烯,因此已广泛付诸生产。
乙炔法:乙炔和氯化氢在氯化汞(附在活性炭载体上)催化 剂存在下,生成氯乙烯:
![]()
这一反应收率很好,能达95%以上,反应是放^的,所以反 应器要采用水冷夹套。出来的气体经水洗、除水和精馏后,可得 纯氯乙稀。
乙烯法:乙烯和氯在二氯乙烷溶液中以氯化铁为催化剂,发 生加成反应,得二氯乙烷,收率达90%~95%。
![]()
二氯乙烷是制氯乙烯的中间体,氯乙烷和烧碱在140°C加热脱 去氯化氢而得氯乙烯:
![]()
氯乙烯的收率几乎是理论量。这一反应叫做退减反应,退下 的氯成为氯化钠,不能再用于加成反应。
如果在少量氯和活性炭等存在下,用热解法从二氯乙烷分子 脱去氯化氢:
![]()
这部分氯化氢可以回收利用于制氯乙烯,即把这部分氯化氢与乙 炔加成,与乙炔法配合起来,充分利用氯气。这一条路线称为烯 诀法制氯乙烯。
氯乙烯虽然不容易发生置换反应(氯被其他基团所置换),但 能发生加成反应,它在适当条件下与氯化氢发生加成:
![]()
加成方向符合马氏规则,即氯原子加在含氯的碳上,氢原子 加在含氢较多的碳上。
氯乙烯在催化剂或光照作用下发生聚合,生成聚氯乙烯:

第四节:氯苯和六六六
氯苯是氯气和苯在铁等催化剂作用下的产物,氯苯是有香味 的液体,沸点132°C,比水重而不溶于水。
苯环上的氯和氯化烯一样,极不活泼。从电子理论上解释, 氯的p电子和苯环上的π键发生了共轭,p电子和π电子有交盖, 与氯乙烯中的氯和双键发生了共轭是相似的情形。在氯苯分子中 氯和碳的键长缩短了,氯和苯环结合得更牢固了,所以氯苯的性质比较不活泼。
氯是邻、对位定位基(第一类定位基),它和苯环的共轭效应 使苯环的邻、对位上电子密度相对地多于间位,所以第二个取代基进入氯的邻位或对位上。实际上在制取氯苯时,总是有第二个氯进入氯的邻位、对位,其中以对二氯苯较多:
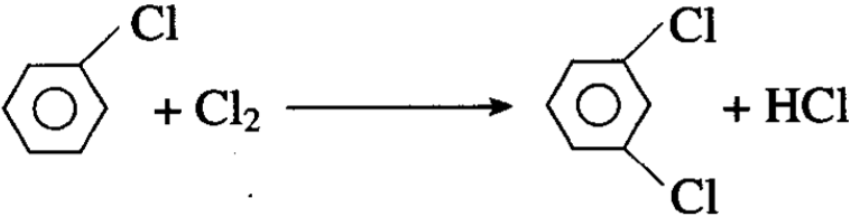
氯苯是制备二二三的工业原料,二二三又称滴滴涕,它是三氯乙醛和氯苯的缩合产物:
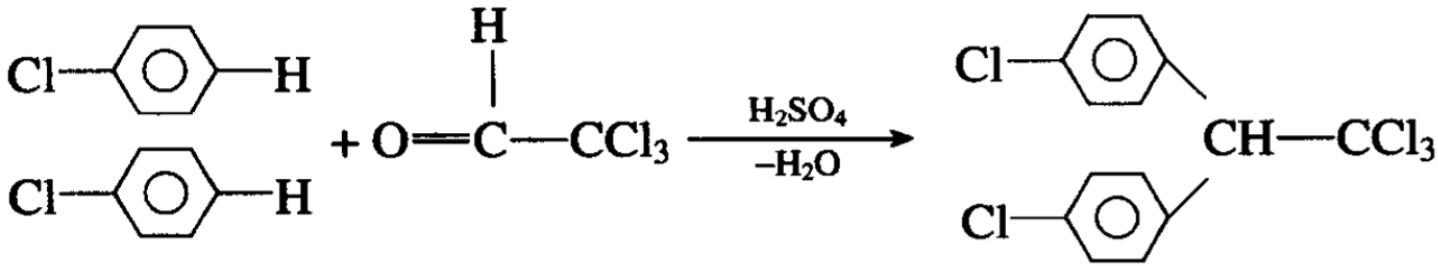
氯和苯在光照射下的加成产物称为六六六(代表六氯环己烷C6H6Cl6),也是一种常用的杀虫剂:
![]()
第五节:其他重要卤代烃
一、3-氯丙稀和氯化苯
3-氯丙烯ClCH2—CH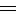 CH2(又称α-氯丙烯)和氯化苄 (
CH2(又称α-氯丙烯)和氯化苄 (![]() )是两种活泼的氯代烃,可以进行许多置换反应。3-氯丙烯的制备在工业上采用高温气相氯化法,在480~520°C将氯气 喷入过量丙烯中:
)是两种活泼的氯代烃,可以进行许多置换反应。3-氯丙烯的制备在工业上采用高温气相氯化法,在480~520°C将氯气 喷入过量丙烯中:
![]()
产物主要是α-氯代物,而极少有加成物。作为一个经验,凡 是加成反应以温度较低为宜,如果丙烯在低温溶液中加氯,有铁 等催化剂存在的话,主要发生的是加成反应。这里我们又碰到同 样的反应物在不同的条件下导致不同结果的例子。α-氯代反应的 另一例子是甲苯的氯代反应也是在加热情况下发生的:
![]()
在这里α-是指与双键或苯核相连的碳原子,这个碳原子上的氢、氯或其他官能团都是比较活泼的。α-卤素容易发生置换反应。 氯化苄和3-氯丙烯在乙醇溶液中,加硝酸银溶液,很快在溶液中沉淀出氯化银,这种情况在氯苯和氯乙烯中是不会发生的,说明 氯化苄和3-氯丙烯的化学性质非常活泼。
3-氯丙烯和氯化苄的氯能发生一系列置换反应:
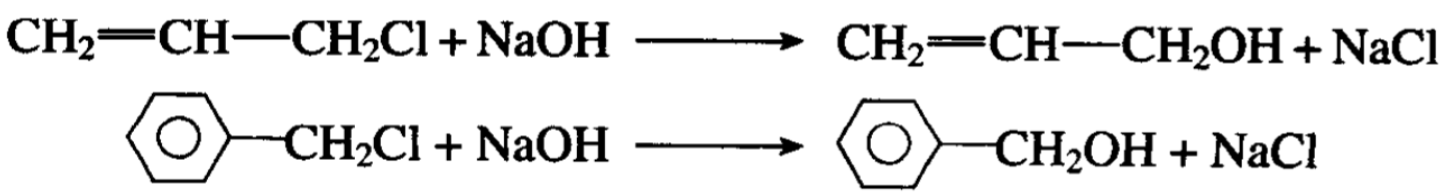
(1)氯被羟基置换。它们和氢氧化钠的水溶液发生水解作用 而得丙烯醇或苄醇:
(2)氯被氰置换。它们和氰化钠在乙醇中回流加热时,氯被 氰基置换:
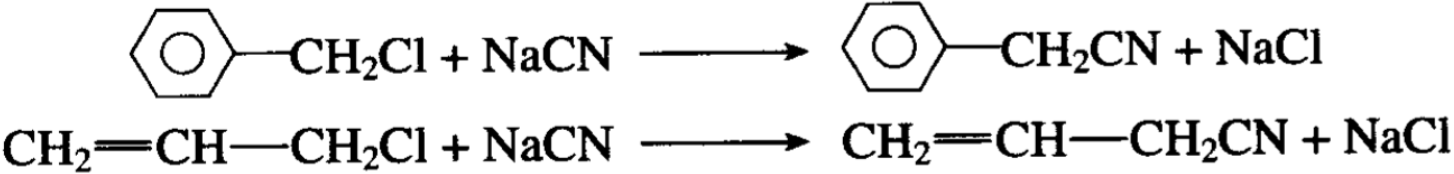
(3)氯和其他基团置换。它们和氨、碘化钠等作用,生成相 应的氨的烃基衍生物和碘化物:

由于3-氯丙烯和氯化苄的化学性质活泼,它们在工业上被用 作制造其他化学产品的原料。3-氯丙烯是制造甘油、丙烯酸和环 氧树脂的原料,氯化苄是制造苯巴比妥(一种安眠药)的原料。
二、四氟乙烯及氟利昂
四氟乙烯是乙烯四个氢全部被氟所取代的全卤代烃(“全”字 指所有的氢全部被卤素所取代):
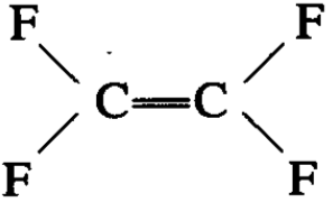
它是利用氯仿与三氟化锑和氟化氢作用,得氟利昂(二氟氯 甲烷),然后加热到800°C而制得:
![]()
四氟乙烯为气体,在氧的催化下,可以聚合成聚四氟乙烯, 为目前所知最耐热、耐腐蚀的塑料,有塑料王之称。
氯利昂是指一系列含氯含氟的甲烷和乙烷,其中二氟氯甲烷(CHC1f2)用于制四氟乙烯,代号F-22;另一种氟利昂,二氟二 氯甲烷可在五氯化锑的催化影响下由四氯化碳与三氟化锑作用 制得:
![]()
第六节:卤代轻的物理性质
卤代烃都不溶于水,在同系物中,由于碳链的增长,沸点、 熔点都随之升高。在卤代烷中除CH3Cl、CH3Br、CH3—CH2Cl为 气体外,其余都是液体或固体,溴代烷、碘代烷、多卤代烷和芳香族卤代烃的相对密度都大于1。脂肪族多卤代烃是良好的溶剂。 卤代烃的物理常数如表所列。
表卤代烃的物理常数
名称 | 结构式 | 沸点,°C | 相对密度 |
氯甲烷 | CH3Cl | -23.7 | 0.992 |
氯乙烷 | CH3CHCl | -13.7 | 0.926 |
溴甲烷 | CH3Br | 4.5 | 1/732 |
溴乙烷 | CH3CH2Br | 38.4 | 1.461 |
碘甲烷 | CH3I | 42.5 | 2.279 |
氯乙烯 | CH2—CH—Cl | -14 | 0.920 |
三氯甲烷 | CHCl3 | 61 | 1.490 |
四氯化碳 | CCl4 | 76 | 1.594 |
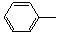
溴苯 |
| 155.5 | 1.495 |
碘苯 |
| 188.5 | 1,832 |
烷基的 名称 | 氯化物 | 溴化物 | 碘化物 | |||
沸点 | 密度 g/cm3 | 沸点 °C | 密度 g/cm3 | 沸点 °C | 密度 g/cm3 | |
甲基 | -23.7 | 0.992 | 4.5 | 1.732 | 42.5 | 2.279 |
乙基 | -13.1 | 0.926 | 38.4 | 1.461 | 72.3 | 1.936 |
乙烯基 | -14 | 0.920 | 16 | 1.517 | 56 | 2.037 |
烯丙基 | 45 | 0.938 | 70 | 1.398 | 103.4 | 1.777 |
苯基 | 132 | 1.106 | 155.5 | 1.495 | 188.5 | 1.832 |
苄基 | 179 | 1.100 | — | — | — | — |
从表中可以看到,同样的烷基卤化物的沸点为碘化物>溴 化物>氯化物,密度为碘化物>溴化物>氯化物。
在同系列中(如一氯代烷)密度随着烷基的加大而减少,沸点随着烷基的加大而升高。
第七节:卤代烷的重要化学性质
卤烷硝化银沉淀
卤烷水解被羟换
卤烷氰解增一碳
卤烷氨化被置换
退减反应能变烯
成烯强碱和卤烷
卤代烷是一类相当活泼的化合物,它的化学活泼性,是由于 分子中含有卤素原子而引起的,因此,卤代烷的主要化学反应都 发生在碳一卤链上。卤代烃的官能团为卤原子,它们有两大化学 通性,一是置换反应,另一退减反应。这两种反应有时可同时发生,视反应条件而定。
一、卤烷硝化银沉淀,卤烷水解被羟换,卤烷氰解增一碳
卤代烷的卤素比较活泼,它能和一系列无机试剂发生置换反 应。从形式上看,似乎一个负性基团置换了另一个负性基因:
![]()
但是这种置换反应完全不同于无机试剂的离子反应。卤代烷 与无机试剂进行反应不能在瞬间完成。在常温下,卤代烷与硝酸 银几乎不起作用,加热后才能产生卤化银沉淀:
![]()
卤代烷和碱性水溶液也是很慢地进行反应,只是在加热下, 卤原子才被羟基所置换:
![]()
这一反应叫做水解反应,事实上它和无机盐的水解过程是完 全不同的。
在卤代烷的水解反应中,水解速度随碱性的增大而加速。
卤代烷还能与氰化钠发生置换反应:
![]()
反应在醇溶液中进行,置换的结果生成了比原来卤代烷多一 个碳原子的腈。反应过程中,实现了新的C一C键的合成。
二、卤烷氨化被置换
卤代烷还能在加压下和氨反应,这个反应先是形成一种铵盐, 在过量碱中释出胺:
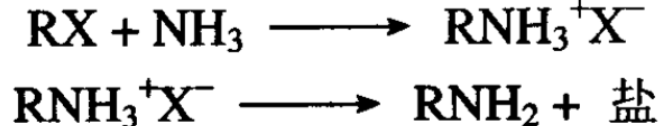
以上置换反应说明了卤原子的活性,这是烷烃所不能实现的 反应。利用卤代烷合成的胺有实用意义。
三、退减反应能变烯,成烯强碱和卤烷
卤代烷在强碱作用下,常常发生另一种反应,就是失去一分 子卤化氣,形成稀烃。这一反应叫作退减反应(或叫消除反应)。 要发生这个反应,在卤原子邻近的碳原子上必须有一个氢原子:
![]()
这个退减反应的进行程度决定于反应的温度、烷基的结构以 及碱的强度等。
先看看烷基的结构对退减反应的影响。
卤原子在碳链上不同位置对退减的难易有一定影响。以卤代丁烷的水解为例,卤代丁烷有下列几种异构体:
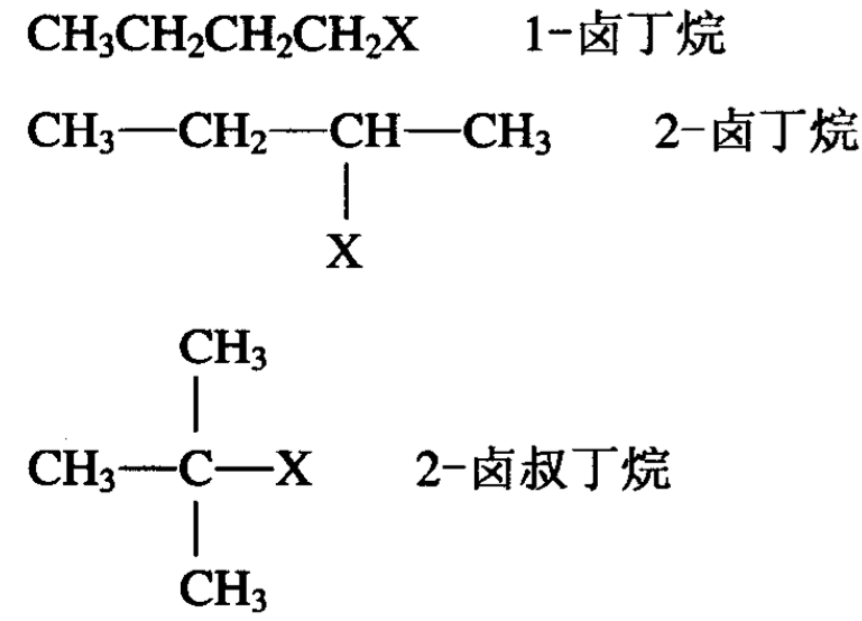
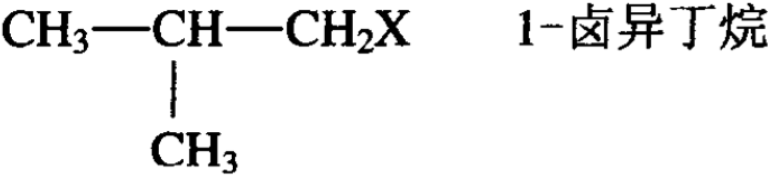
卤原子连在第一碳原子上(如1-卤丁烷,1-卤异丁烷)称为 一级卤原子,卤原子连在第二碳原子上的称为二级卤原子,卤原 子连在第三碳原子上的称为三级卤原子。一般来说,三级卤原子 最容易发生退减反应,其次是二级卤原子,再次才是一级卤原子。
在同样条件下,几种溴丁烷和乙醇钠发生退减反应,形成烯 烃。百分次序如下:
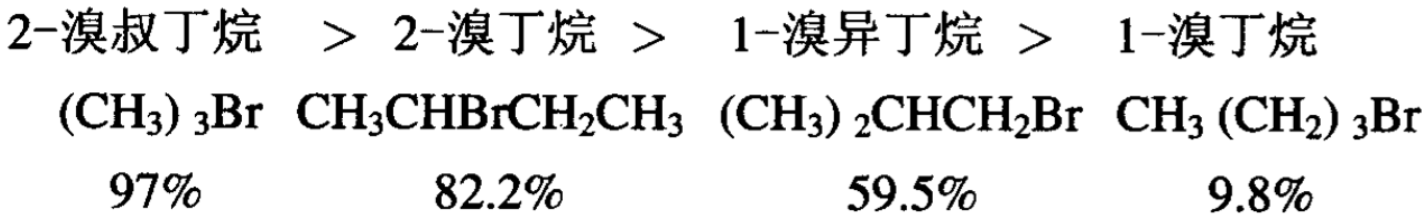
它们退减一分子HX的结果为:
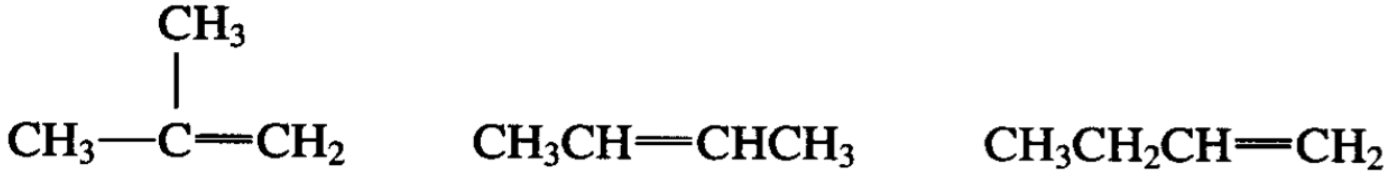
在以上四种卤代烷的退减反应中,产生了三种丁烯。值得注 意的是2-卤丁烷除去一分子HX后,理论上可以生成1-丁烯或 2-丁烯:
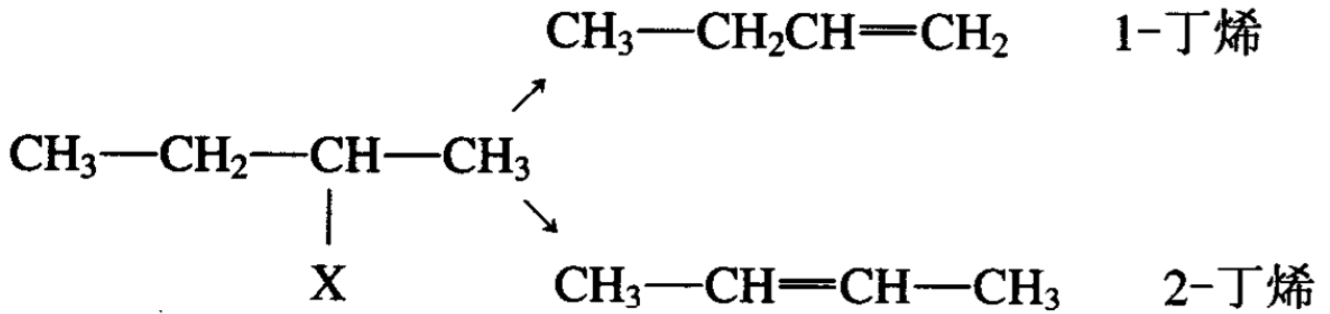
但实际实验结果为:2-卤丁烷失去HX,主要产生2-丁烯。 可以得出这样一种经验规律:卤代烷分子中,卤原子邻近有两个 或两个以上C一H键时,退减的氢发生在含氢较少的碳原子上。
再看导致退减反应的外部条件。一般提高反应温度,则有利于形成烯烃。在较强的碱溶液中,卤代烷容易发生退减反应而变成烯烃;在较弱的碱溶液中,卤代烷容易发生置换反应而变成醇:
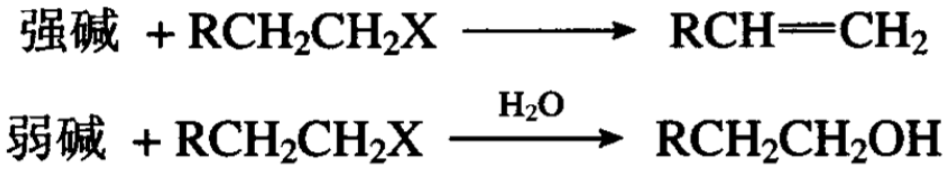
一般使卤代烷除去HX的试剂为氢氧化钾的乙醇溶液或醇钠的乙醇溶液。

- 全部评论(0)
 Br
Br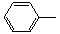 I
I