常用电离平衡常数的解题技巧
时间:2021-03-11 11:11 来源:未知 作者:化学自习室 点击: 次 所属专题: 电离平衡常数
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
电离平衡常数是高考中一个重要的必考考点,常考查电离平衡常数的计算、弱酸的相对强弱、离子浓度离子大小的比较、离子方程式的书写等,大多结合图像进行分析。解决此类问题的关键是,掌握电离常数的概念及基本的计算方法,利用平衡移动原理,认真分析图像的变化趋势,结合电荷守恒、物料守恒进行判断。
一.电离平衡常数的计算
利用图像求电离平衡常数,一定要看清楚图像中纵、横坐标表示的含义,图中曲线起点、转折点、交叉点、与纵横坐标的的含义。
案例1(2017课标Ⅱ)改变0.1mol/L 二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数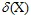 随pH的变化如图所示[已知
随pH的变化如图所示[已知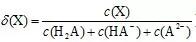 ]。
]。
下列叙述错误的是
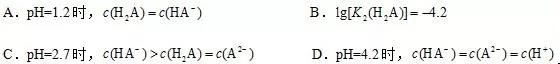
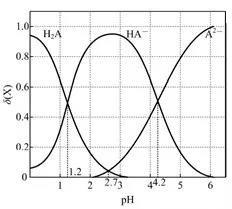
分析:该题是一道0.1mol/L 二元弱酸H2A电离平衡试题,纵坐标代表的是溶液中的H2A、HA-、A2-的物质的量分数,横坐标表示的是pH,图中有三个交点:pH =1.2,c(H2A)=c(HA-);pH =2.7,c(H2A)=c(A2-);pH=4.2时,c(A2-)=c(HA-)。
解析:A、根据图像,pH=1.2时,H2A和HA-相交,则有c(H2A)=c(HA-),故A说法正确;B、pH=4.2时,c(A2-)=c(HA-),根据第二步电离HA- H++A2-,得出:K2(H2A)=c(H+)×c(A2-)/c(HA-)= c(H+)=10-4.2,故B说法正确;C、根据图像,pH=2.7时,H2A和A2-相交,则有c(H2A)=c(A2-),故C说法正确;D、根据pH=4.2时,c(HA-)=c(A2-),且物质的量分数约为0.48,而c(H+)=10-4.2,可知c(HA-)=c(A2-)>c(H+),故D说法错误。
H++A2-,得出:K2(H2A)=c(H+)×c(A2-)/c(HA-)= c(H+)=10-4.2,故B说法正确;C、根据图像,pH=2.7时,H2A和A2-相交,则有c(H2A)=c(A2-),故C说法正确;D、根据pH=4.2时,c(HA-)=c(A2-),且物质的量分数约为0.48,而c(H+)=10-4.2,可知c(HA-)=c(A2-)>c(H+),故D说法错误。
二.根据平衡常数判断弱酸或弱碱溶液或其盐溶液的酸碱性的相对强弱
根据电离平衡常数可以判断弱酸的相对强弱,从而可以判断出其对应盐的pH大小关系。
案例2已知25℃时有关弱酸的电离平衡常数见下表:
弱酸化学式 | HA | H2B |
电离平衡常数(25℃) | Ka=1.7×10-6 | K1=1.3×10-3 K2=5.6×10-8 |
则下列有关说法正确的是
A.等物质的量浓度的各溶液pH关系为:pH(Na2B)>pH(NaHB)>pH(NaA)
B.将a mol·L-1的HA溶液与a mol·L-1的NaA溶液等体积混合,混合液中:c(Na+)>c(A-)
C.向Na2B溶液中加入足量的HA溶液发生反应的离子方程式为:B2-+2HA==2A-+H2B
D. NaHB溶液中部分微粒浓度的大小为:c(Na+)> c(HB-)> c(B2-)> c(H2B)
分析:根据电离常数可判断出酸性:H2B >HA>HB-,再根据越弱越水解,则可判断出对应盐溶液的pH(Na2B)>pH(NaA)>pH(NaHB)。
解析:A.由于酸性H2B>HA>HB-,使得水解程度HB-<A-
三.书写化学方程式
由电离常数判断出弱酸的酸性强弱,根据强酸制弱酸的原理,可以写出两种酸发生反应的化学方程式。
案例3H2CO3和H2S在25℃时的电离常数如下:
电离常数 | K1 | K2 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
H2S | 5.7×10-8 | 1.2×10-15 |
则下列反应可能发生的是()
A. NaHCO3+NaHS=Na2CO3+H2S
B. Na2S+H2O+CO2=NaHS+NaHCO3
C. H2S+2Na2CO3=Na2S+2NaHCO3
D. H2S+NaHCO3=NaHS+H2CO3
分析:由电离平衡常数可判断出弱酸的相对强弱为:H2CO3>H2S>HCO3->HS-,再根据强酸制弱酸,则可写出反应的化学方程式。
解析:根据25℃时碳酸与氢硫酸的电离常数可知,两种酸都是弱酸,电离平衡常数越大,酸性越强,所以酸性H2CO3>H2s>HCO3->HS-。A项,因为酸性H2S>HCO3-,所以违背强酸制弱酸原理,故A错误;B项,酸性H2S>HCO3->HS-,所以H2O、CO2与Na2S反应生成NaHCO3,故b正确;C项,因为酸性H2S>HCO3->HS-,所以H2S与Na2CO3反应能生成NaHS和NaHCO3,故C错误;D项,因为酸性H2CO3>H2S,所以不能由H2S和NaHCO3生成H2CO3,故D错误。综上,选B。
四.判断溶液中离子浓度的大小关系
电离平衡常数表示弱酸的相对强弱,由弱酸生成的盐就会发生水解,由越弱越水解的原理,可以判断盐溶液中离子离子浓度大小关系。
案例4表是25℃时某些弱酸的电离平衡常数,下列说法正确的是( )
化学式 | CH3COOH | HClO | H2CO3 |
Ka | 1.8×10﹣5 | 3.0×10﹣8 | Ka1=4.1×10﹣7 Ka2=5.6×10﹣11 |
A.相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是:
c(Na+)>c(ClO﹣)>c(CH3COO﹣)>c(OH﹣)>c(H+)
B.向0.1mol·L﹣1CH3COOH溶液中滴加NaOH溶液至溶液pH=5,此时:
c(CH3COOH):C(CH3COO﹣)=9:5
C.少量碳酸氢钠固体加入到新制的氯水中,c(HClO)增大
D.等体积等物质的量浓度的CH3COONa(aq)与NaClO(aq)中离子总数大小:n(前)<n(后)
分析:由电离平衡常数可判断出弱酸的酸性强弱:CH3COOH> H2CO3> HClO>HCO3-,根据越弱越水解,水解程度大小为:CO32->ClO->HCO3->CH3COO-,即可判断盐溶液中离子浓度大小顺序。
解析:A.醋酸的电离常数大于次氯酸,所以醋酸钠的水解程度小于次氯酸钠,醋酸钠和次氯酸钠都是强碱弱酸盐,其混合溶液呈碱性,所以相同物质的量浓度的CH3COONa和NaClO的混合液中,各离子浓度的大小关系是:c(Na+)>c(CH3COO-)>c(ClO-)>c(OH-)>c(H+),故A错误;B.CH3COOH的电离常数为1.8×10-5,向0.1mol•L-1CH3COOH溶液中滴加NaOH溶液至溶液pH=5,则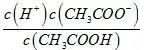 =1.8×10-5,c(CH3COOH):C(CH3COO-)=10-5:1.8×10-5=5:9,故B错误;C.氯水中存在Cl2+H2O⇌H++Cl-+HClO,少量碳酸氢钠固体加入到新制的氯水中,碳酸氢钠只与盐酸反应,则平衡正向移动,c(HClO)增大,故C正确;D.HClO酸性较弱,NaClO水解程度较大,根据电荷守恒:c(Na+)+c(H+)=c(OH-)+c(CH3COO-)、c(Na+)+c(H+)=c(OH-)+c(ClO-),由于NaClO水解程度较大,溶液中氢离子浓度较小,且两溶液钠离子浓度相等,所以CH3COONa溶液中离子总数大于NaClO溶液,即n(前)>n(后),故D错误;故选C。
=1.8×10-5,c(CH3COOH):C(CH3COO-)=10-5:1.8×10-5=5:9,故B错误;C.氯水中存在Cl2+H2O⇌H++Cl-+HClO,少量碳酸氢钠固体加入到新制的氯水中,碳酸氢钠只与盐酸反应,则平衡正向移动,c(HClO)增大,故C正确;D.HClO酸性较弱,NaClO水解程度较大,根据电荷守恒:c(Na+)+c(H+)=c(OH-)+c(CH3COO-)、c(Na+)+c(H+)=c(OH-)+c(ClO-),由于NaClO水解程度较大,溶液中氢离子浓度较小,且两溶液钠离子浓度相等,所以CH3COONa溶液中离子总数大于NaClO溶液,即n(前)>n(后),故D错误;故选C。
总之涉及电离平衡常数的题目必须先根据电离常数判断出酸的相对强弱,把酸的相对强弱由强到弱的顺序排好,然后按照题目要求进行回答,遇到图像要看清楚图像代表的含义,关键的点表达的意义要清晰。

- 全部评论(0)
