浅析离子交换膜在电化学中的运用
时间:2021-08-23 10:42 来源:未知 作者:夏时君 点击: 次 所属专题: 离子交换膜
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
离子交换膜是“具有选择透过性能的网状立体结构的高分子功能膜或分离膜”,常运用于膜电解和电渗析等离子交换膜法技术中。它具有选择透过性、分离效率高、能耗低、污染少等特点,在水处理、环保、化工、冶金等领域都有广泛应用。高中化学各版本教材中对于交换膜虽有介绍,但内容分布零碎,对结构特点及功能挖掘较少。笔者通过选取典型案例,剖析其在电化学中的重要运用。
1.离子交换膜的种类与透过原理
离子交换膜依据不 同标准有不同分类方式,其中按选择透过性可分为阳离子交换膜(下简称阳膜)、阴离子交换膜(下简称阴膜)、特殊离子交换膜三大类。根据双电层理论:阳膜含有酸性活性基团,解离出阳离子,使膜呈负电性,选择性透过阳离子;阴膜含有碱性活性基团,解离出阴离子,使膜呈正电性,选择性透过阴离子。如图1和图2所示。我们常将这种与膜所带电荷相反的离子透过膜的现象称为反离子迁移。
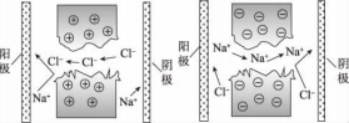
图1 阳膜选择性透过过程图2阴膜选择性透过过程
离子交换的透过性常与膜的静电作用、孔隙作用和扩散作用有关。从离子交换膜的选择性来看:它使溶液中阳、阴离子在膜上实现反离子迁移,同种离子受到阻挡。从离子相对大小来看:水合离子半径小于孔隙大小才能通过。从电场作用来看:它使溶液中阳、阴离子分别向阴极和阳极定向迁移。
2.离子交换膜在电化学中的运用
(1)构成双液原电池,闭合电路,提高放电寿命与效率
单液原电池由于活性电极材料与电解质溶液直接接触,无法避免放电的同时也发生化学腐蚀,导致能量转化效率低、放电不稳定、使用寿命短等问题。将单液原电池转换为双液原电池可减弱上述问题。解决此问题可使用盐桥或离子交换膜形成负极室和正极室。相对于盐桥,离子交换
膜表面积较大,有利于增大离子的定向移动速率,减小电阻,放电效率提高,使用寿命增长。
[案例1]某原电池装置结构如图3,电池总反应为2Ag+Cl2==2AgCl。
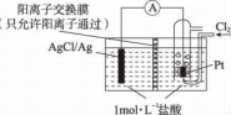
图3 银氯原电池的结构示意图
解析:该原电池装置通过阳膜形成两液原电池,分别在负极和正极形成一对氧化-还原电对:AgCl/Ag和Cl2/Cl-。负极反应:Ag-e-+Cl-==AgCl;正极反应:Cl2+2e-==2Cl-。
(2)制备提纯物质:隔离微粒,提高物质的产率与纯度
膜电解法是制备物质的重要方法,它将电解和膜分离相结合,将制备、分离和浓缩相结合。即“在通电条件下发生电解化学反应时,生成的产物能及时地从反应体系中通过离子交换膜分离出来,使反应 向生成物的方 向进行,从而提高反应效率。”其中最重要的膜电解运用于氯碱工业以及废水处理等。
①氯碱工业
氯碱工业结构示意图如图4所示,电解池构成:通过阳膜将电解室隔离为阳极室与 阴极室,两室只进行阳离子迁移;阳极室和阴极室分别加入饱和NaCl溶液和稀NaOH溶液。电极反应过程,阳极反应:2Cl--2e-==Cl2↑,同时Na+在电场作用下向阴极室定向移动,导致阳极室NaCl浓度下降;阴极反应:2H++2e-==H2↑,H+浓度下降,促 进H2O的电离平衡,产生大量OH-。由于阳膜 的阻挡,在阴极室富集NaOH,制备出烧碱。阳膜功能分析:一方面可以避免副反应发生,如H2和Cl2的反应、Cl2和NaOH的反应;另一方面能够提高烧碱的纯度与产率。若选用阴膜,则会出现OH-在阴室产生,却在阳室富集,同时与阳极电解出的Cl2与剩余NaCl混合,导致产率和纯度下降,不利于分离与提纯。
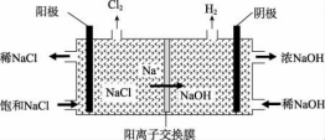
图4 氯碱工业结构示意图
同样,用上述单膜双室电解池也可制备硫酸:在阳极室、阴极室分别加入稀H2SO4和CuSO4溶液,离子交换膜选择阴膜。阳极反应:4OH--4e-==O2↑+2H2O,产生大量H+。阴极反应:Cu2++2e-==Cu,阴极室富集大量SO42-,通过阴膜迁移至阳极室与H+结合,从而完成回收金属和制备酸的目的。
②盐制备酸碱
盐电离产生的阳阴离子在电场作用下发生定向移动,借助于阴膜制备酸、阳膜制备碱,是一种很好地利用盐制备酸碱的方法,如图5所示。电解池的结构:通过阴膜和阳膜形成双膜三室电解池。从H+和OH-的产生来看:阳极是OH-放电,放出O2产生大量H+;阴极是H+放电,放出H2生成OH-。从离子定向移动来看:SO42- 向阳极移动,Na+向阴极移 动。阴膜与阳膜的选择:SO42-移向阳极与H+结合形成H2SO4,离子交换膜须保证能通过SO42-且阳极产生的H+不能通过,故靠近阳极室选择阴膜;同理Na+需通过阳膜才能向阴极迁移,与阴极产生的OH-形成NaOH,故选择阳膜,从而实现由Na2SO4溶液制备H2SO4和NaOH的目的。
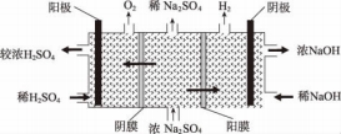
图5 电解法制备酸碱
(3)多室电渗析:交替运用阴膜阳膜,完成物质淡化与浓缩
电渗析是将阴膜与阳膜交替排列在电极之间,在直流电场作用下,以电位差为动力,离子透过选择性离子交换膜而迁移,从而使电解质离子自溶液中部分分离出来,实现溶液的浓缩与淡化,复分解反应及电解氧化还原等效能,达到提纯精制的目的。
如海水的淡化如图6,淡化室:因离子迁移而盐溶液淡化。Na+和Cl-在电场作用下,分别向右通过阳膜和向左通过阴膜,溶液脱盐得到淡水的目的,解决了用水问题,达到工业废液的零排放。浓缩室:因富集离子而浓缩物质。由于相邻两个室分别迁移了Na+和Cl-,从而富集了NaCl,实现物质分离与利用 。同样用阴膜扩散渗析可从含酸的工业废液中回收酸,用阳膜扩散渗析从含碱的工业废液中回收碱。
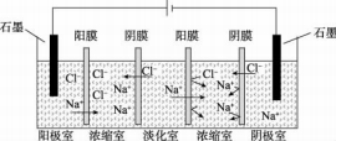
图6 电解法淡化海水
(4)废水处理:处理离子电性与物质性质间矛盾,完成试剂再生循环
用离子交换膜电解也可回收工业废水中的金属、分离稀有金属和贵金属等,回收方法包括:金属阳离子在阴极放电而沉积、调节溶液pH或加沉淀剂转化为难溶物进行处理。如从电性来看,Fe2+会向阴极定向迁移;从还原性来说,它倾向于在阳极失电子被氧化,如何解决阳离子电性引发的定向迁移与离子还原性间的矛盾?这就可以借助离子交换膜发挥透过选择性功能。
[案例2]利用化石燃料开采、加工过程产生的H2S废气制取氢气,既廉价又环保。其中电化学法制氢气过程如图7。
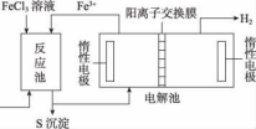
图7 H2S电化学法制H2
解析:H2S废气制取氢气处理过程分为两个部分:(1)H2S的脱硫处理:H2S通过FeCl3反应池发生2FeCl3+H2S==2FeCl2+S↓+2HCl,生成S。(2)原料FeCl3的电解再生:阳极中Fe2+放电产生Fe3+,阴极H+放电生成H2。该电解核心问题是离子交换膜的选择。若选择阴膜,阴极产生的OH-会与阳极Fe2+、Fe3+作用产生沉淀,导致循环物质再生失败。若选择阳膜,Fe2+因定向迁移而放电不完全,也会产生Cl2;阴极由于Fe2+及Fe3+向阴极定向迁移产生Fe(OH)2和Fe(OH)3。当然在阳极涉及因Fe2+放电导致浓度下降引发的由高浓度到低浓度的扩散问题(向阳极移动)和电场作用向阴极的定向迁移间 的相对大小的矛盾问题。这也是该装置在设计上有待完善的地方,修正方法是在靠近阳极处再增加一个阴膜,在阴膜与阳膜间加入电解质NaCl,既不影响阳极中Fe2+放电,也不影响FeCl3的纯度;阴极不影响H+的放电,不影响制备NaOH的纯度与产率。
可以看出,离子交换膜的广泛运用是由其结构特点决定的,我们通过阴膜与阳膜的合理配置,可挖掘其不同的功能,更好地发挥其工具性和价值性,应用于更多的领域。

- 全部评论(0)
