全文解读原子结构
时间:2022-09-16 15:11 来源:未知 作者:化学自习室 点击: 次 所属专题: 原子结构03
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
原子是构成物质的基本单元,原子结构影响原子间的结合方式,而原子间结合的方式决定了材料的种类,不同材料有着不同的性能,同一材料经过不同的加工工艺后也会有不同的性能,这些都归结于内部结构的不同,本文重讲一下原子结构(Atomic Structure)的相关知识。
一、原子结构
原子虽然为构成物质的基本单元,但原子并不是最小的微粒,具有复杂结构。原子由原子核(质子和中子)和电子构成,电子绕核做不规则运动,形成的电子云模型。原子核内有中子和质子,体积很小,却承担了原子绝大部分的质量。如图1所示为原子结构的示意图。
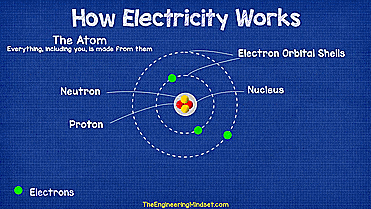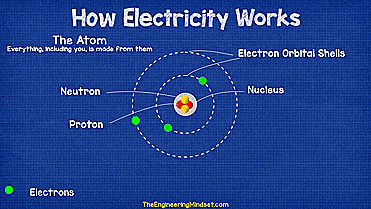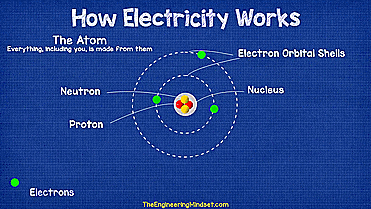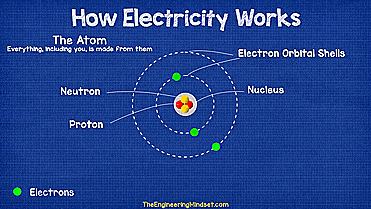
图1
原子的原子序数(Atomic numbers)表示原子核中的质子数(带正电的粒子),在中性原子中,原子序数也等于电荷云中的电子数。所有元素都是根据周期表中的电子构型分类的。
原子核的带电情况如图2所示:
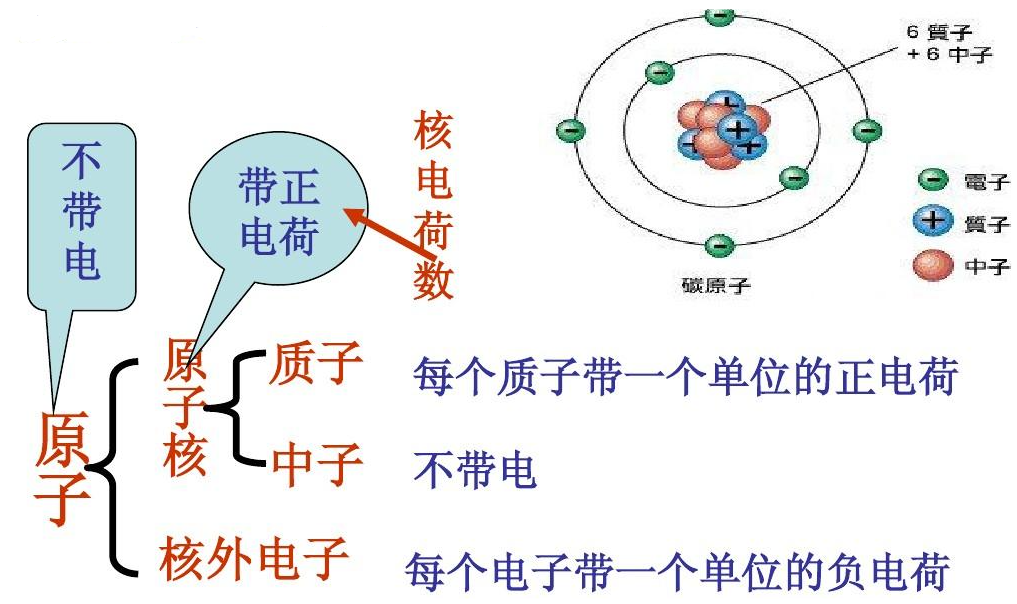
图2
质子:每个质子带一个单位的正电荷
中子:不带电,电中性
原子核(质子+中子):带正电
核外电子:每个电子带一个单位的负电荷
原子(原子核+核外电子):不带电,电中性
【注】核电荷数=质子数=核外电子数
二、原子的电子结构
(1)量子数
电子绕原子核在一定轨道上旋转,核外电子的运动状态由主量子数 n、轨道动量量子数 l、磁量子数 m、自旋量子数 ms 确定。量子数是原子中分配电子到离散能级的数。
每个电子所属的能级由四个量子数决定:
主量子数 n:K、L、M、N、O、P、Q、……
角量子数 li:s、p、d、f、……
磁量子数 m:2l + 1
自旋量子数 ms:![]()
随着主量子数n值的增加,电子层按K、L、M、N、O…的顺序排列,电子的能量逐渐升高、电子离原子核的平均距离也越来越大。如图3所示有原子核,K、L、M、N壳层。
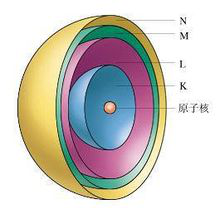
图3
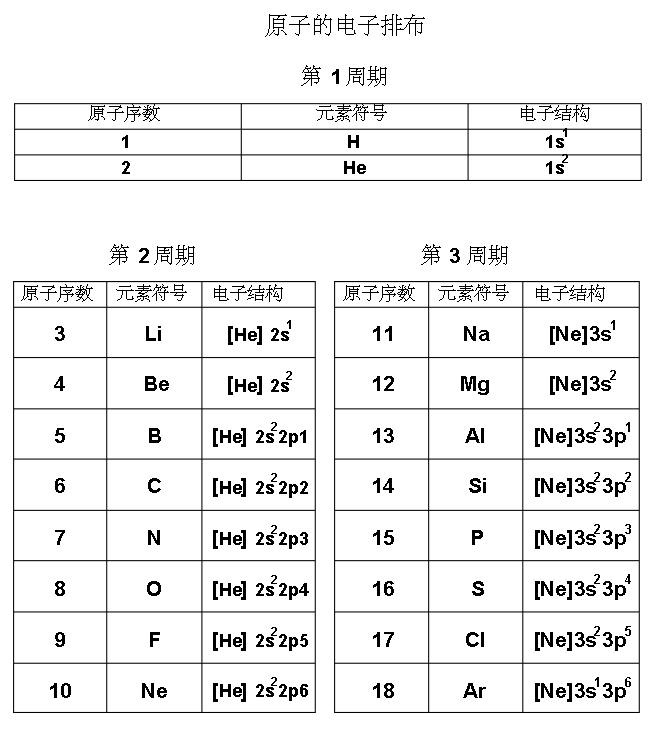
(2)电子排布
原子处于基态时,即原子的能量处于最低的状态,此时原子最稳定,必须遵循如下原则:
● 能量最低原则:电子优先占据能级较低的原子轨道,当能量低的壳层占满后,电子才会占据能量较高的层级,这使整个原子体系能量处于最低,如图4所示。

图4
1s-2s-2p-3s-3p-4s-3d-4p-5s-4d-5p
● 泡里不相容原理(Pauli’s exclusion principle):一个原子轨道最多容纳两个电子,且这两个电子自旋方向必须相反,即2n2
洪特规则(Hund's rule):在能级高低相等的轨道上,电子尽可能分占不同轨道,电子自旋平行,即全充满,半充满,全空,核外电子以这三种形式排布时比较稳定。
全满(s2、p6、d10、f14)
半满(s1、p3、d5、f7)
全空(s0、p0、d0、f0)
图5以氢原子为例,分析了电子排布,蓝点只有一个填充电子。
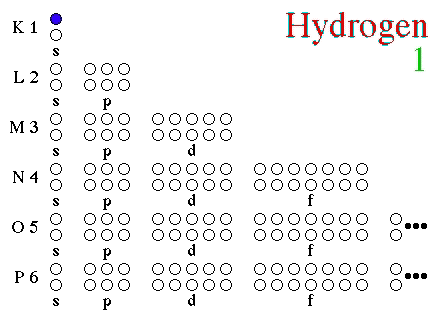
图5
第24号元素铬Cr,若按各能级填充规则,其核外电子排布式应为1s22s22p63s23p63d44s2。但依据洪特规则可知3D能级填充5个电子时较稳定,故其核外电子排布为1s22s22p63s23p63d54s1
图6为电子能量随主量子数和次量子数变化情况。
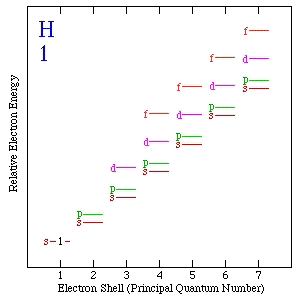
图6
三、原子质量(Atomic mass)
元素的相对原子质量是该元素的6.023×1023个原子(阿伏伽德罗数NA)的质量,单位为克。
四、原子尺寸(Atomic size)
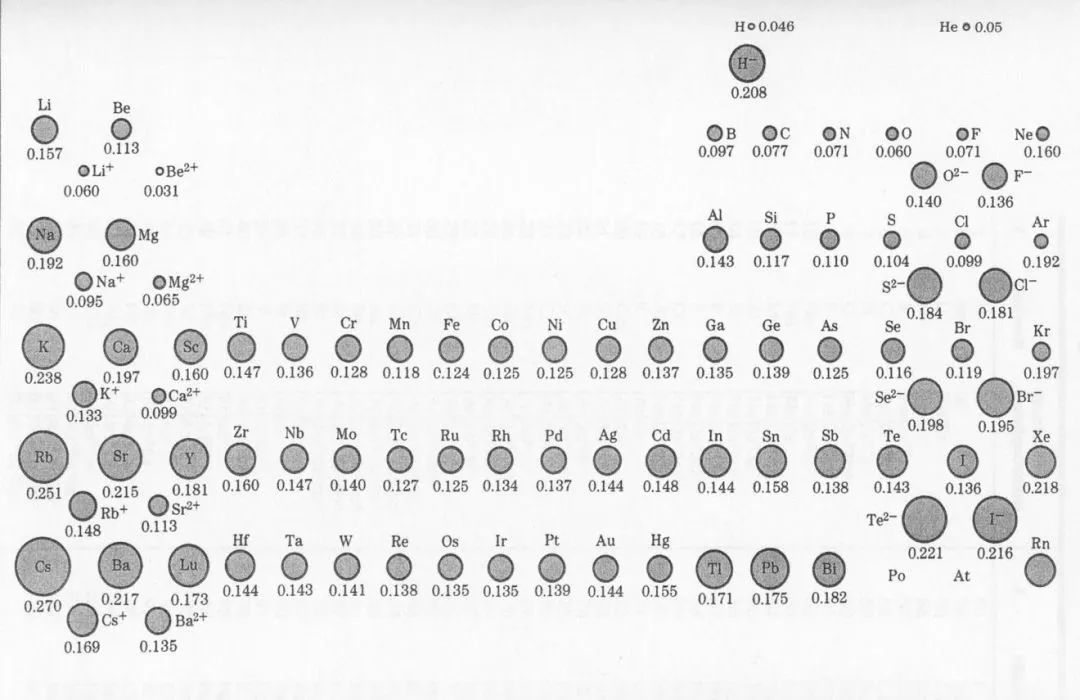
图7
原子尺寸由原子半径决定,影响原子半径的因素有三个:
一是核电荷数,核电荷数越多原子核对核外电子的引力越大(使电子向原核收缩),则原子半径越小;当电子层数相同时,其原子半径随核电荷数的增加而减小;
二是最外层电子数,最外层电子数越多半径越大;
三是电子层数(电子的分层排布与离核远近空间大小以及电子云之间的相互排斥有关),电子层越多原子半径越大。当电子层结构相同时,质子数越大,半径越小。如图7为原子及其离子的尺寸情况。
五、电负性(Electronegativity)
电负性是元素的原子在化合物中吸引电子的能力的标度。元素的电负性越大,表示其原子在化合物中吸引电子的能力越强。元素电负性数值越大,表示其原子在化合物中吸引电子的能力越强;反之,电负性数值越小,相应原子在化合物中吸引电子的能力越弱(稀有气体原子除外)。

图8
图8给出了元素周期表中不同原子的电负性,其变化情况如下
● 随着原子序号的递增,元素的电负性呈现周期性变化。
● 同一周期,从左到右元素电负性递增,同一主族,自上而下元素电负性递减。对副族而言,同族元素的电负性也大体呈现这种变化趋势。因此,电负性大的元素集中在元素周期表的右上角,电负性小的元素集中在左下角。
● 电负性越大的非金属元素越活跃,电负性越小的金属元素越活泼。氟的电负性最大(4.0),是最容易参与反应的非金属;电负性最小的元素(0.79)铯是最活泼的金属。

- 全部评论(0)
