浓差电池的本质是什么?
时间:2025-08-31 09:04 来源:未知 作者:化学自习室 点击: 次 所属专题: 浓差电池
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
【导读】浓差电池是以氧化还原为工具、以浓度差为本质的特殊电化学装置。浓差电池的原理是浓度梯度驱动的熵增过程(ΔS>0),通过电极反应将扩散能转化为电能。
微观上:电极发生氧化还原反应,正负电极上有电子转移;
宏观上:浓差电池总反应无净氧化还原,总反应无电子得失或化合价变化,仅体现出物质的转移。

一、浓差电池的本质
1.能量来源:浓度梯度而非化学反应
普通化学电池通过氧化还原反应释放化学能(如锌铜电池),而浓差电池的能量完全源于浓度差导致的熵增效应。根据热力学原理,物质从高浓度向低浓度扩散是自发过程(ΔG<0),浓差电池通过电极反应将这部分吉布斯自由能转化为电能。
离子浓差电池:Ag|Ag⁺(高浓度)||Ag⁺(低浓度)|Ag

总反应无新物质生成,仅离子迁移。
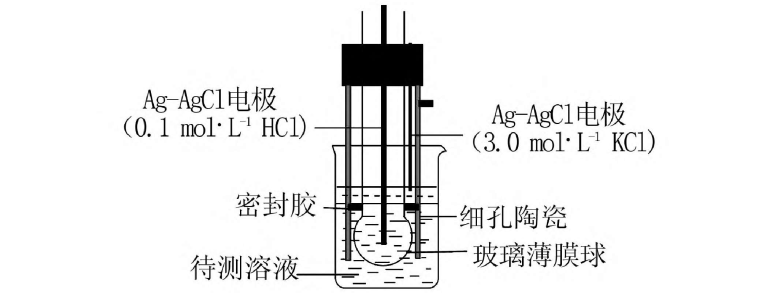
2.电极反应的“工具性”角色
虽然电极上发生氧化还原反应,但其作用是辅助浓度平衡。
如上述浓差电池的负极(低浓度侧):物质失去电子被氧化(Ag=Ag⁺+E⁻),增加局部浓度。正极(高浓度侧):物质获得电子被还原(Ag⁺+E⁻=Ag),降低局部浓度。电极反应本身不改变系统总组成,仅推动离子定向迁移。
3.浓差电池的“死亡”特性
当两侧浓度相等时,电势差归零,电池失效。这与普通电池活性物质耗尽相似,但本质是浓度梯度消失。
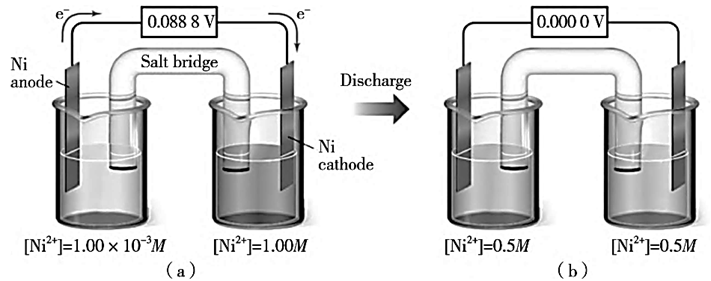
二、浓差电池是否属于氧化还原反应?
1.微观层面:每个电极均发生电子转移,涉及氧化还原反应。
负极:氧化反应(失电子)
Ag-e⁻=Ag⁺(低浓)
H₂(高压)-2e⁻=2H⁺
正极:还原反应(得电子)
Ag⁺(高浓)+e⁻=Ag
2H⁺+2e⁻=H₂(低压)
由此可见浓差电池的电极反应符合氧化还原反应的基本定义。
2.宏观层面:电池总反应无电子得失或化合价变化,仅体现物质转移,无净氧化还原反应。
Ag⁺(高浓)=Ag⁺(低)
H₂(高压)=H₂(低压)
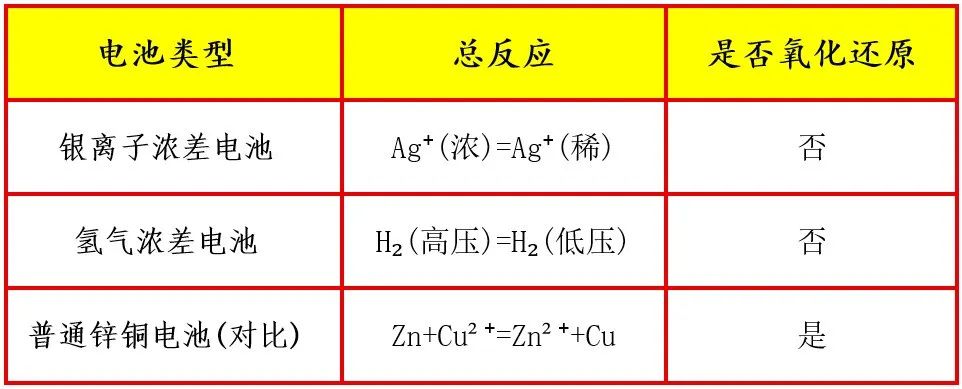
3.与普通电池的区别:
浓差电池的ΔG完全由浓度差驱动(ΔG=−nfE),而标准氧化还原电位(E∘=0)。
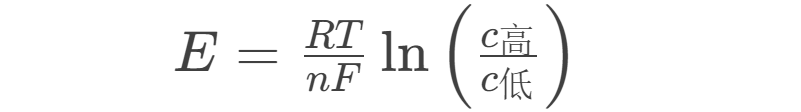
三、浓差电池典例简析
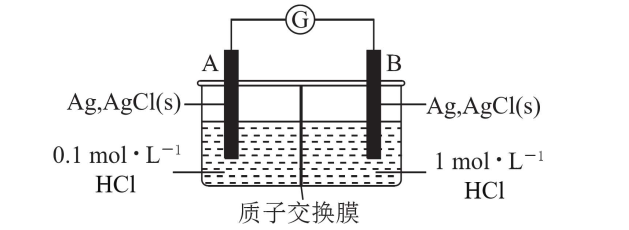
1.电解质浓差电池(双液型)
装置:
Ag|AgNO₃(低浓度)||AgNO₃(高浓度)|Ag
负极:Ag-e⁻=Ag⁺(低浓) (氧化)
正极:Ag⁺(高浓)+e⁻=Ag(还原)
总反应:Ag⁺(高浓)=Ag⁺(低)
电压公式:
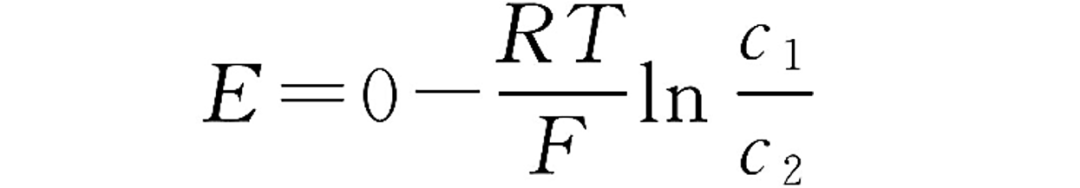
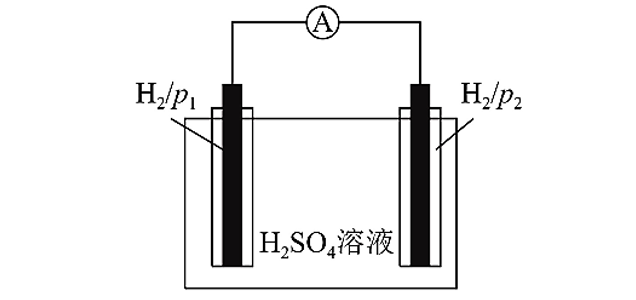
2.电极浓差电池(单液型)
氢气浓差电池:
Pt|H₂(P₁)|H⁺|H₂(P₂)|Pt (P₁>P₂)
负极:H₂(P₁)-2e⁻=2H⁺
正极:2H⁺+2e⁻=H₂(P₂)
总反应:H₂(P₁)=H₂(P₂)



- 全部评论(0)
