原电池的负极就是阳极吗?为什么叫“牺牲阳极法”,而不叫“保护
时间:2025-10-11 07:46 来源:未知 作者:化学自习室 点击: 次 所属专题: 正负与阴阳
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
【导读】“正/负”看电势,按照电势高低,高正低负,绝不互换;“阴/阳”看反应,装置不同则对应关系不同。
在原电池中,负极是阳极,正极是阴极,但不可以通用替换;在电解池中,阳极接正极,阴极接负极。阳极永远是发生氧化反应的地方,不管它带正电还是负电;反之阴极是发生还原反应的地方。
“牺牲阳极法”中的‘阳极’指的是那个被牺牲的金属(如锌、镁),发生的是氧化反应,阳极不是指被保护的钢铁。钢铁是阴极,被保护;锌是阳极,被牺牲。

一、阳极/阴极与正极/负极是两个不同的命名体系

二、在原电池中,负极就是阳极,正极就是阴极!
阳极/阴极的定义是按反应类型来的,不是按电势高低。阳极氧化,阴极还原,不管正负只看反应!
典例:锌铜原电池
负极(锌)失去电子,发生氧化是阳极;正极(铜)得到电子,发生还原阴极。
锌电极:Zn=Zn²⁺+2e⁻→氧化反应→阳极,是负极。
铜电极:Cu²⁺+2e⁻=Cu→还原反应→阴极,是正极。
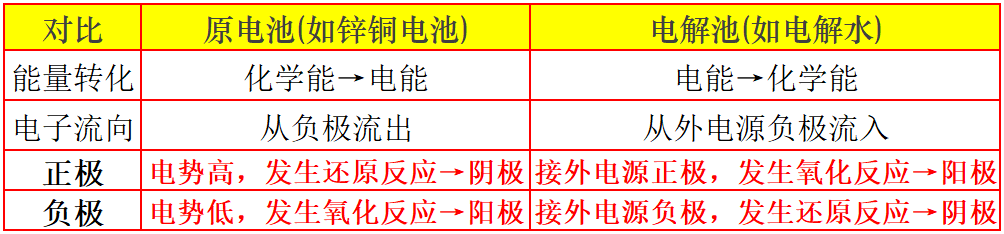
三、正/负极与阳/阴极可否相互通用替换?
不可以。
正/负极:按电子流向(或电势高低)命名,是物理概念,用于描述电路特性。
阴/阳极:按反应类型命名,是化学概念,用于描述化学反应,氧化为阳极,还原为阴极。
在原电池中,这两套身份是重合的:负极就是阳极,正极就是阴极。但这不等于可以“通用替换”,使用时需根据讨论的侧重点(物理电势还是化学反应)来选择术语。
在电解池中,这两套身份是分离、交叉的:阳极连接电源正极,阴极连接电源负极,绝对不可以通用。
一个电极的身份,必须同时用两套系统来描述,但它们不能交叉替换。这就好比描述定义一个人,你可以说“他是斐戈(姓名),他是教师(职业)”,但你不能说“他的名字就是教师”,具体要根据所处的场景、扮演的角色和需要强调突出说明的特性。
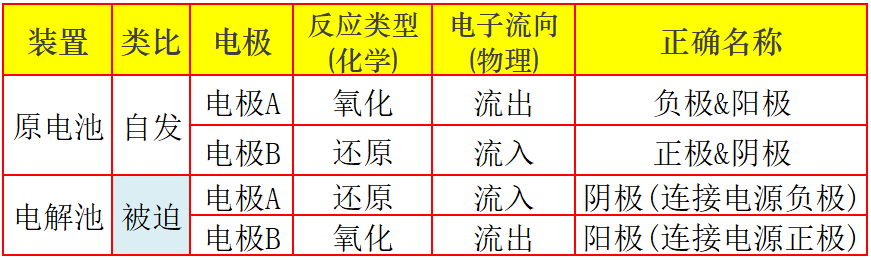
由以上对比分析可知:原电池的正极≠电解池的阳极;原电池的负极≠电解池的阴极;接外电源负极≠本身是负极。交叉称呼就会把氧化、还原搞反。

四、原电池原理防腐为什么叫“牺牲阳极法”,不叫“保护阴极法”?
“牺牲阳极法”这个名字强调的是牺牲的是阳极,而不是说被保护的是阳极。这个名字是从牺牲的角度出发的,而不是从被保护对象出发的。
从电化学原电池的角度理解:阳极=发生氧化反应=被腐蚀=锌块;阴极=发生还原反应=被保护=钢铁。
五、为什么把发生氧化反应的电极叫阳极,把发生还原反应的电极叫阴极?
人为定义,历史和语言综合因素。
Anion=ana-(向上)+ion(行走者)=走向阳极(氧化反应)的离子。
Cation=kata-(向下)+ion(行走者)=走向阴极(还原反应)的离子。
“阴离子”和“阳离子”这两个词本身,也正是从“阳极”和“阴极”派生出来的。


- 全部评论(0)
