常压蒸馏、减压蒸馏、水蒸气蒸馏、分馏介绍与比较
时间:2026-01-07 18:06 来源:未知 作者:化学自习室 点击: 次 所属专题: 分馏 蒸馏 减压蒸馏 水蒸气蒸馏
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、蒸馏概述
蒸馏的定义:通过加热气化液体物质,冷凝其蒸汽并加以收集来实现液体物质的分离和纯化的一种实验方法。
蒸馏的用途:分离具有不同挥发度的液体混合物;提纯液体物质,去除其中不挥发性的杂质;提纯液体产物,去除其中挥发性的溶剂。
蒸馏的种类:蒸馏分为简单蒸馏(常压蒸馏)、减压蒸馏、水蒸气蒸馏和分馏等。
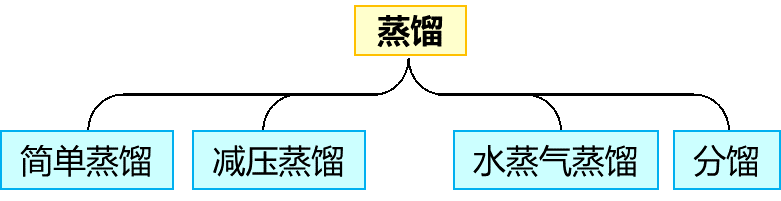
各类蒸馏方法比较:
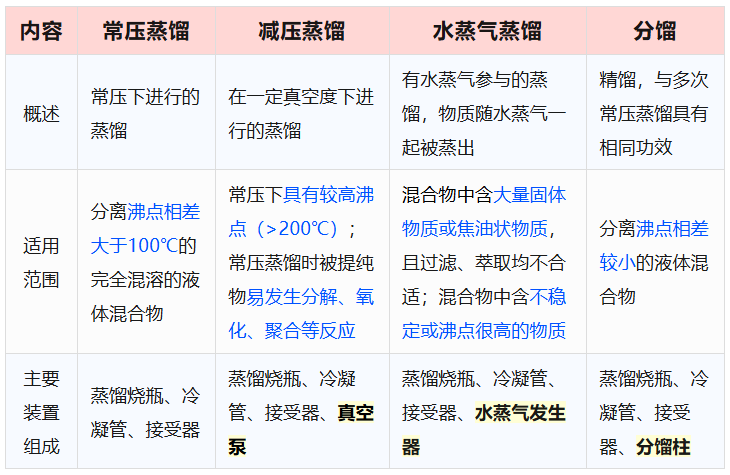
二、常压蒸馏
常压蒸馏又称普通蒸馏或简单蒸馏,是在常压下进行的蒸馏。
适用范围:应用简单蒸馏可分离沸点相差大于100℃的两种液体。低沸点的组分在较低恒定温度下被蒸出,随后,蒸气温度上升并再次保持恒定,高沸点的组分在此温度下被蒸出,这样具有较大沸点差的两种液体得到了很好的分离。
实验装置:常用的简单蒸馏装置包含蒸馏烧瓶、温度计、直形冷凝管、接引管和接收瓶等仪器。
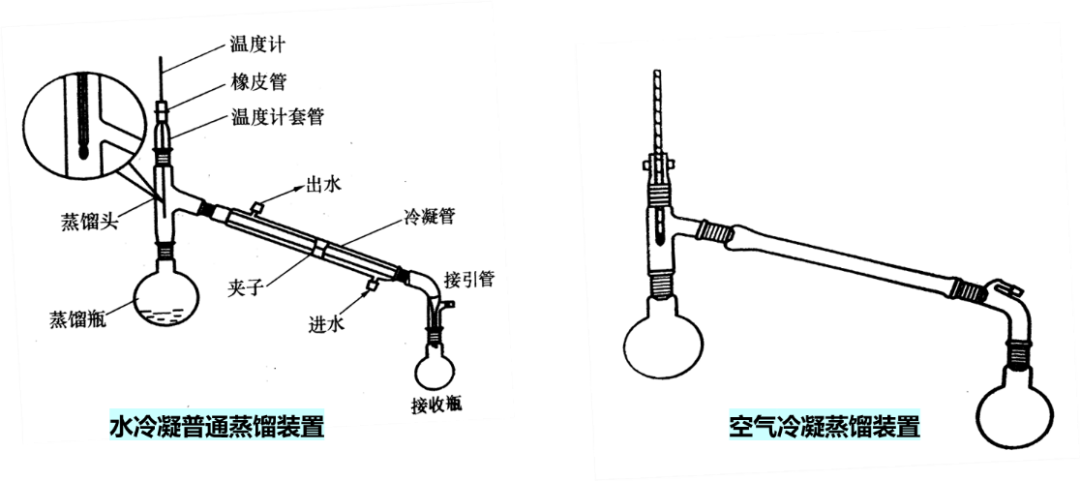
蒸馏烧瓶的选择:
蒸馏烧瓶由蒸馏头和圆底烧瓶(不可用平底烧瓶代替,以防蒸馏过程中受热不均匀而破裂)组成。蒸馏烧瓶的大小要选择适宜,其选择根据所蒸馏的液体体积来确定,液体体积一般不少于圆底烧瓶容积的1/3,不超过2/3。
如果圆底烧瓶太大,液体量太少,相对会有较多液体残留在瓶内,损失较多;如果圆底烧瓶太小,液体量太多,沸腾时液体可能从瓶中冲出,影响蒸馏效果。
冷凝管的选择:
冷凝管的种类有直形冷凝管、空气冷凝管、蛇形冷凝管等。需根据具体的蒸馏液体进行选择。
被蒸馏液体的沸点(bp)在140℃以下用水冷凝,使用直形冷凝管。
被蒸馏液体的沸点在140℃以上时用空气冷凝管,因高沸点化合物用空气冷凝管即可达到冷却的目的,而且可防止用水冷凝温差太大而引起冷凝管接头处破裂。
被蒸馏液体的沸点如果很低,可以使用蛇形冷凝管。
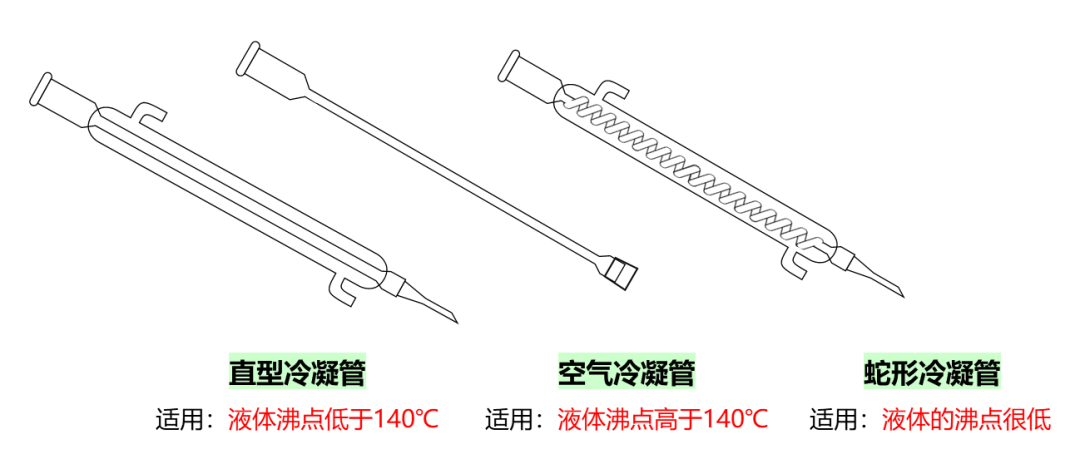
热源的选择:
水浴加热:沸点低于80℃的液体
油浴或沙浴加热:沸点高于80℃的液体
火直接加热:沸点更高的液体
三、减压蒸馏
减压蒸馏也叫真空蒸馏,是分离、提纯有机化合物的重要方法之一,它特别适用于那些在常压下蒸馏时未达到沸点温度就受热分解或氧化、聚合的物质。有时候也因为被蒸馏物质沸点太高,而考虑采用减压蒸馏。
减压蒸馏原理:
液体的沸点是指它的蒸气压等于外界大气压时的温度,所以液体沸腾的温度随外界压力的降低而降低。因而使用真空泵连接盛有液体的容器,使液体表面的压力降低,即可降低液体的沸点,这种在较低压力下进行蒸馏的操作称为减压蒸馏。
许多有机化合物的沸点在压力降到1.3-2.0kPa(10-15mmHg)时,可比其常压下沸点降低80-100℃。
实验装置:
进行减压蒸馏时,预先了解被蒸馏物质在一定真空度下的沸点对减压蒸馏的具体操作具有一定参考价值,比如热源的选择、冷凝管的选择以及减压泵的选择等。
物质在一定压力下的沸点可通过查阅相关文献得知,也可利用公式lnp=A+B/T(式中P为蒸气压,T为沸点;A、B为常数)估算得出。
常用的减压蒸馏装置一般由克氏蒸馏烧瓶(也即圆底烧瓶+克氏蒸馏头组合)、冷凝管、接受器和减压系统四个部分组成。下图为常用的减压装置,根据各部分的用途,可分为蒸馏部分、减压部分、保护和测压部分。
常用减压蒸馏装置
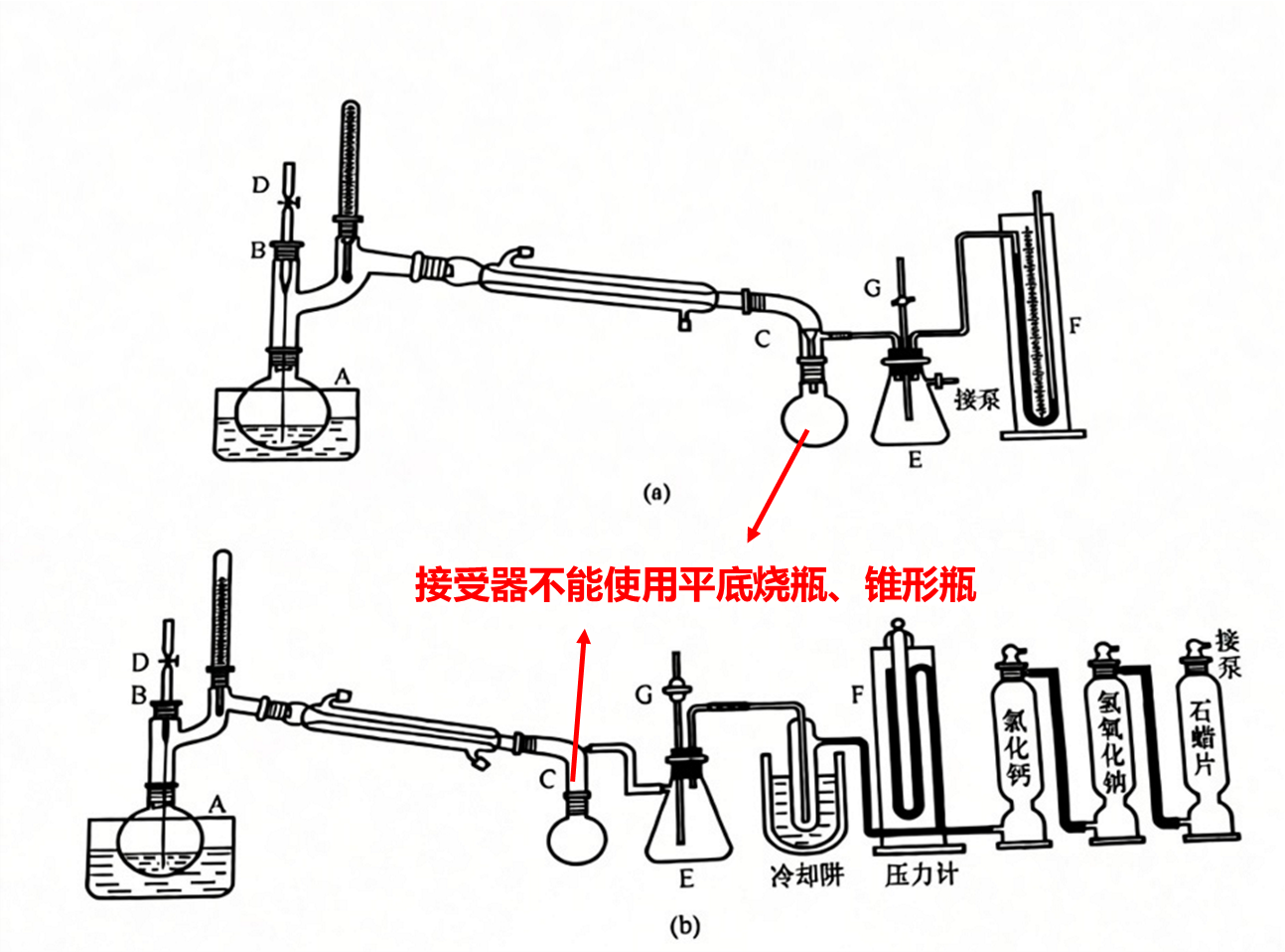
与常压蒸馏装置相比,减压蒸馏装置不仅多了减压系统,所用蒸馏烧瓶有所不同,对接收器的要求也不同。
由于减压蒸馏时,整套装置都要承受一定压力,所以接受器(上图中的C)不能使用锥形瓶或瓶底烧瓶之类的薄壁或有棱角的容器(因不耐压,减压时易破裂),而且各个连接处的橡胶管均应是厚壁型的,以免真空下被压瘪。
四、水蒸汽蒸馏
定义:许多不溶于水或微溶于水的有机化合物,无论是固体还是液体,只要在100℃左右具有一定的蒸气压,即有一定的挥发性,若与水一起加热就能与水同时蒸馏出来,这种蒸馏方式称为水蒸气蒸馏。
适用范围:可将某些化合物与其他挥发性更低的物质分开而达到分离提纯的目的,也是从动植物中提取芳香油等天然产物最常用的方法之一。特别适用于分离那些在其沸点附近易分解的物质;适用于分离含有不挥发性杂质或大量树脂状杂质的物质;也适用于从较多固体反应混合物中分离被吸附的液体,其分离效果较常压蒸馏或重结晶好。
水蒸汽蒸馏法分离提纯有机化合物的要求:
①不溶或微溶于水,这是满足水蒸气蒸馏的先决条件;
②长时间与水共沸不发生化学反应;
③在100℃左右,有一定的蒸气压,一般不小于1.33kPa(10mmHg)。
水蒸气蒸馏的基本原理:
根据道尔顿分压定律,整个体系的蒸气压等于体系内各组分的蒸气压之和。对于不混溶混合物,混合物中每一组分是独立蒸发的,每一组分在一定温度下的分压等于其纯物质在同一温度下的蒸气压,所以不混溶混合物在一定温度下的总蒸气压等于各个纯组分在同一温度下的蒸气压之和。当不混溶混合物的蒸气压等于外界大气压时,混合物就开始沸腾,因此不混溶混合物的沸点比各个组分单独存在时的沸点都低。
对于水蒸气蒸馏,水蒸气充当了不混溶混合物的组分之一,不混溶混合物在一定温度下的总蒸气压等于该温度下水的蒸气压与被提纯物质在同一温度下的蒸气压之和。常压下水的沸点为100℃,因此被提纯物质可在低于100℃的温度下随同水蒸气被蒸馏出来。由于被提纯物质不溶或难溶于水,所以馏出液一旦冷却,被提纯物质即从水中分层析出,再通过简单萃取即可完成分离纯化。
实验装置:
常用的水蒸气蒸馏装置由水蒸气发生器、蒸馏部分、冷凝部分和接受器组成。与简单蒸馏实验装置相比,多了一个水蒸气发生器。
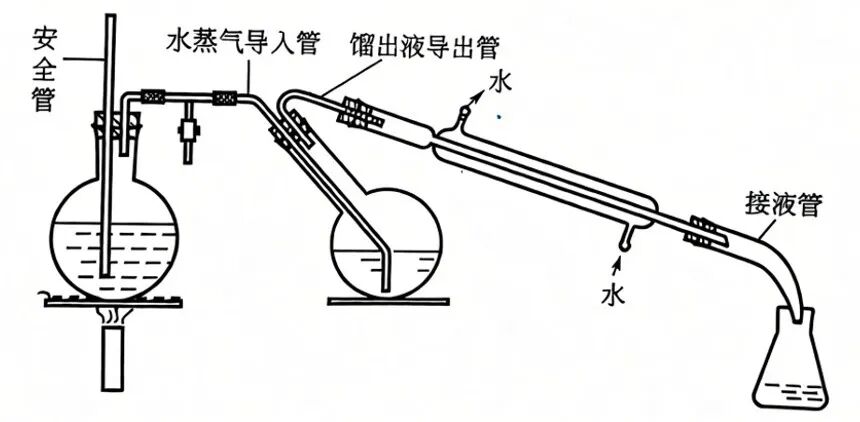
水蒸气蒸馏装置
五、分馏
什么情况考虑采用分馏法
利用常压蒸馏可分离沸点相差较大(>100℃)的完全混溶的液体混合物,对于沸点相差较小的液体混合物,常压蒸馏只能达到部分分离,分离效果不佳。要获得比较好的分离效果,必须进行多次常压蒸馏。这样繁琐费时,损耗又大,实际中很少采用,常常采用分馏法。
分馏也叫精馏,它能实现混合物的多次气化和冷凝,与多次常压蒸馏具有相同功效。
实验装置:
实验室常用的分馏装置主要由蒸馏烧瓶、分馏柱、蒸馏头、冷凝管和接受器组成。与常压蒸馏装置相比,多了一个分馏柱。分馏柱是分馏装置中的核心部件,混合物的多次气化和冷凝都是在其中完成的。
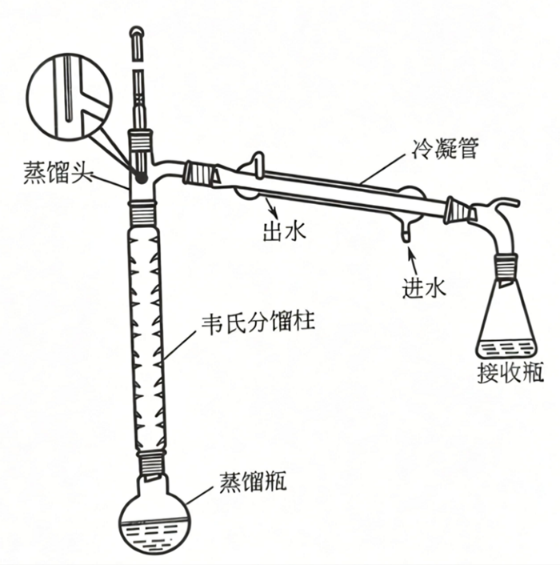
分馏实验装置
连续蒸馏是如何在分馏柱中实现的?
当混合物蒸气进入分馏柱时,因沸点较高的组分易被冷凝,冷凝液中就会含有较多高沸点的物质,而蒸气中低沸点的成分就相对地增多。冷凝液向下流动时又与上升的蒸气接触,二者之间进行热量交换,即上升的蒸气中高沸点的物质被冷凝下来,低沸点的物质仍呈蒸气状上升;而在冷凝液中低沸点的物质则受热汽化,高沸点的仍呈液态。
如此经多次反复的液相与气相的热交换,使得低沸点的物质不断上升,最后被蒸馏出来,高沸点的物质则不断流回加热的容器中,从而将沸点不同的物质分离。
分馏时柱内不同高度的各段组分是不同的:相距越远,组分的差别就越大。也即,在柱的动态平衡情况下,沿着分馏柱存在着组分梯度,越接近柱顶沸点低的组分越多。

- 全部评论(0)
