高中化学取代反应类型判断及考点
时间:2026-03-30 17:17 来源:未知 作者:鲁志超 点击: 次 所属专题: 取代反应,有机反应类型
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、什么是取代反应?
一句话:有机物里某个原子/原子团,被别的原子/原子团换掉。 判断口诀:
1.有进有出(区别加成“只进不出”、消去“只出不进”)
2.饱和度不变
3.一般无化合价大幅变化
二、这两个绝对不是取代!(高频坑点)
1. 硝基变为氨基 → 还原反应
很多同学误以为“2个O换成2个H”就是取代,其实是官能团被还原,不属于取代。
2. 两分子乙炔二聚成乙烯基乙炔 → 加成反应
2HC≡CH → HC≡C−CH=CH₂ 只有键的合并,没有原子团“换掉”,不是取代。
三、高中全部取代反应(按类别记)
1. 烷烃的卤代
CH₄ + Cl₂  CH₃Cl + HCl 继续取代: CH₃Cl → CH₂Cl₂ → CHCl₃ → CCl₄
CH₃Cl + HCl 继续取代: CH₃Cl → CH₂Cl₂ → CHCl₃ → CCl₄
条件:光照
易错:不能用 FeBr₃、FeCl₃ 催化;不能用卤化氢
2. 烯烃 α‑H 卤代(双键邻位饱和碳上的氢)
烯烃与卤素在室温发生双键亲电加成,但在高温(500~600℃,气相)时,优先在双键的 α 位发生自由基取代:
以丙烯为例:
加成(室温):CH₃CH=CH₂ + Cl₂  CH₃CHClCH₂Cl
CH₃CHClCH₂Cl
取代(高温):CH₃CH=CH₂ + Cl₂  ClCH₂CH=CH₂ + HCl
ClCH₂CH=CH₂ + HCl
核心区别:
室温 + 有机溶剂(如 CCl₄)→ 加成(双键断裂,加两个 Cl)
高温(500~600℃)+ 气相 → α‑H 取代(双键保留,仅 α 位 H 被 Cl 替换)
本质:高温下 Cl₂ 均裂为 Cl·自由基,进攻 α‑H,属于自由基取代反应
3. 苯及其同系物的取代
(1)苯的卤代

溴代:FeBr₃
氯代:FeCl₃
(2)苯的硝化

(3)苯的磺化(可逆)

4. 卤代烃水解(取代)
CH₃CH₂Br + NaOH  CH₃CH₂OH + NaBr
CH₃CH₂OH + NaBr
条件:NaOH 水溶液、加热
易错:NaOH 醇溶液 = 消去反应
5. 醇的取代(新教材条件已修正)
(1)醇与卤化氢反应
乙醇 + HBr: CH₃CH₂OH + HBr  CH₃CH₂Br + H₂O
CH₃CH₂Br + H₂O
乙醇 + HCl: CH₃CH₂OH + HCl![]() CH₃CH₂Cl + H₂O
CH₃CH₂Cl + H₂O
乙醇 + HI: CH₃CH₂OH + HI  CH₃CH₂I + H₂O
CH₃CH₂I + H₂O
(2)醇分子间脱水
2CH₃CH₂OH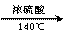 CH₃CH₂OCH₂CH₃ + H₂O
CH₃CH₂OCH₂CH₃ + H₂O
易错:140℃取代;170℃消去
6. 酯化与酯的水解(都是取代)
(1)酯化(可逆)
CH₃COOH + CH₃CH₂OH CH₃COOCH₂CH₃ + H₂O
CH₃COOCH₂CH₃ + H₂O
(2)酯的水解
酸性水解:酯 + H₂O 羧酸 + 醇
羧酸 + 醇
碱性水解:酯 + NaOH  羧酸钠 + 醇(不可逆)
羧酸钠 + 醇(不可逆)
四、取代反应条件对照表
反应类型 | 反应物 | 规范条件 | 易错提醒 |
|---|---|---|---|
烷烃卤代 | 烷烃 + 卤素单质 | 光照 | 不能用催化剂、不用卤化氢 |
烯烃 α‑H 卤代 | 烯烃 + 卤素单质 | 500~600℃,气相 | 室温为加成,高温才是取代;双键保留 |
苯环卤代 | 苯 + Br₂/Cl₂ | FeBr₃/FeCl₃ | 光照为加成,不是取代 |
苯的硝化 | 苯 + 浓硝酸 | 浓H₂SO₄、50~60℃ | 产物是硝基苯,非氨基苯 |
卤代烃水解 | 卤代烃 + NaOH | 水溶液、加热 | 醇溶液为消去反应 |
醇与HBr取代 | 乙醇 + HBr | 浓硫酸、加热 | 新教材标准条件 |
醇与HCl取代 | 乙醇 + HCl | ZnCl₂、加热 | 催化剂必须写ZnCl₂ |
醇与HI取代 | 乙醇 + HI | 加热 | 无需催化剂 |
醇分子间脱水 | 乙醇 + 乙醇 | 浓H₂SO₄、140℃ | 170℃为消去反应 |
酯化反应 | 羧酸 + 醇 | 浓H₂SO₄、加热 | 酸脱羟基醇脱氢,可逆 |
五、3秒判断技巧
1.看进出:有进有出=取代
2.看饱和度:不变=可能取代
3.看条件:光照+卤素→烷烃取代
FeBr₃/FeCl₃+卤素→苯环取代
500~600℃+气相卤素→烯烃 α‑H 取代
室温+有机溶剂卤素→烯烃加成(不是取代)
最终总结
硝基→氨基:还原反应,不是取代
乙炔二聚:加成反应,不是取代
卤代条件:光照(烷烃)、500~600℃气相(α‑H)、FeBr₃/FeCl₃(苯环)
醇+卤化氢:HBr(浓硫酸)、HCl(ZnCl₂)、HI(仅加热)
烯烃与卤素:室温加成,高温α‑H取代,条件不同产物完全不同

- 全部评论(0)
