等电子体原理全面解读
时间:2026-03-10 16:48 来源:未知 作者:化学自习室 点击: 次 所属专题: 等电子体
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!

(欧文·朗缪尔1881年1月31日—1957年8月16日)
这一原理由美国化学家欧文·朗缪尔(Irving l Angmuir)气体裹钨丝,科学照人间:欧文·朗缪尔的一生于1919年提出,它揭示了分子或离子的结构与其电子排布之间的内在联系,成为预测和理解物质性质的重要工具。简单来说,若两种微粒具有相同的通式(AXm)且价电子总数相等,它们便属于“等电子体”,通常表现出相似的立体结构和化学键特征。
一、等电子体的定义与核心特征
等电子体的核心在于“通式相同”和“价电子总数相等”两个条件。通式AXm,A代表中心原子,X代表配位原子,M为配位原子的个数。例如,CO2均符合AX2通式,且价电子总数均为16,因此它们互为等电子体。
等电子体的结构相似性主要体现在以下三个方面:
1.立体构型一致:如CO2、N3-均为直线形分子,键角为180°;
2.杂化方式相同:中心原子的轨道杂化类型由价层电子对数决定,等电子体的电子对排布一致,故杂化方式相同。例如,CO32-、SO32-为sp2化,呈平面三角形;
3.化学键类型相似:等电子体常含有相同类型的大π键。例如,CO2均含有两套p-pπ键,而SO2、NO2-均含有一套三中心四电子的大π键( )。
)。
二、等电子体的典型实例解析
(1) 通式:AX2,价电子数:16
例子:CO2)、NO2+(亚硝酰阳离子)、N3-(叠氮根)。
结构特征:几何构型:直线形;杂化方式:中心原子无孤对电子,采取 sp杂化;键角:180°;化学键:含有两套p-pπ键大π键( )。
)。
(2) 通式:AX3,价电子数:24
例子:CO32-碳酸根)、NO3-硝酸根)、SO3三氧化硫)。
结构特征:几何构型:平面三角形;杂化方式:中心原子无孤对电子,采取 sp2杂化;化学键:含有一套p-pπ键大π键( )。
)。
(3) 通式:AX2,价电子数:18
例子:SO2二氧化硫)、O3臭氧)、NO2-亚硝酸根)。
结构特征:VSEPR模型:平面三角形(理想模型);孤对电子:中心原子上有1对孤对电子(位于分子平面上);实际构型:V形(或角形、折线形)。
化学键:含有一套p-pπ键大π键(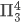 )。
)。
对比注意:ClO2-虽然也是 AX2但价电子数为20,结构不同(中心原子有2对孤对电子,采取 sp3杂化,键角更小)。
(4) 通式:AX4 ,价电子数:32
例子:ClO4-高氯酸根)、SO42-硫酸根)、PO43-磷酸根)。
结构特征:几何构型:正四面体;杂化方式:sp3杂化;化学键注意:这些离子中不存在 p-pπ键(因为中心原子的 p轨道已全用于杂化)。路易斯结构式中的双键实际上是d-p大π键(由中心原子的 D轨道和配位原子的 P轨道形成)。
(5) 通式:AX3,价电子数:26
例子:SO32-(亚硫酸根)、ClO3-氯酸根)。
结构特征:VSEPR模型:四面体;电子排布:中心原子有4个σ轨道(3个成键,1对孤对电子占据);实际构型:三角锥体(不计孤对电子时);杂化方式:sp3杂化。
对比注意:对比 SO3和 SO32-虽然通式看似相同,但 SO3价电子数为24(平面三角形),而 SO32-价电子数为26(三角锥体),因此结构特征不同。
三、等电子体原理的应用与局限
等电子体原理在化学研究中具有广泛的应用价值:
预测分子结构:对于未知结构的分子,可通过寻找已知结构的等电子体进行类比推断。例如,ClO3-SO32-为等电子体(价电子数均为26),因此可预测ClO3-三角锥形结构。
理解化学键本质:通过等电子体的键型对比,可深入理解离域π键、共振结构等概念。例如,苯(C6H6)与吡啶(C5H5N)虽原子组成不同,但因价电子总数相同(30个),均具有芳香性,体现了等电子体原理在有机化学中的延伸。
指导新材料设计:在无机合成中,利用等电子体原理可设计具有特定结构和功能的新化合物。例如,石墨烯的等电子体——氮化硼(BN)纳米片,具有与石墨烯相似的二维结构,但表现出不同的电学性质。
然而,等电子体原理也存在一定的局限性:
键角差异:虽然等电子体的构型相同,但键角不一定完全相等。例如,SO2键角为119.5°,而O3116.8°,这是由于中心原子的电负性差异导致的。
过渡金属化合物的复杂性:对于含有D轨道参与成键的过渡金属配合物,等电子体原理的适用性会受到限制,需结合晶体场理论或分子轨道理论进行综合分析。

- 全部评论(0)
