dz�������ܽ���̵������仯
ʱ��:2016-03-10 18:20 ��Դ:δ֪ ����:���ظ� ���:�� ����ר�⣺ �����ܽ����
��Ȩ��������������Ϊ����ѧ��ϰ�ҡ�����ζ��δ����ϵ��ԭ���ߣ���ԭ���߿�����������ϵ�����䣺79248376@qq.com����
���л�ѧ�α��н����ܽ���̵���ЧӦʱд�������������������ܽ�ʱ���е����ȣ����еķ����أ�������Ϊ�������ܽ���ˮ�ͨ���������ֹ��̣�һ�������� �ķ��ӣ������ӣ�����ɢ���̣����ֹ����������������������̣���һ�������ʵķ��� (������ �� ��ˮ�������ã��γ�ˮ�Ϸ��ӣ���ˮ�����ӡ��Ĺ��̣����ֹ��̷ų������� �ǻ�ѧ���̡������ܽ��ʱ����Һ���¶��������ǽ��ͣ�Ҫ���������ֹ�����Ƿų��������������յ��������������յ��������ڷų��������������������¼�ơ��� ������
����Ϊ���α�����������������������������ͬ�������֡�
�����ܽ�ʱ�����ʵķ��ӻ�����Ҫ�˷��˴˼��������������ӻ���Ӿ���Ȼ����ɢ�������ȥ�����α����н�����ɢ�����������Dz�ȫ��ģ������ܽ�ʱ�����ʵķ��ӻ� ����Ҫ�˴˷��룬�ܼ��ķ���ҲҪ���룬�����������ʷ��ӻ����ӵĿ�Ѩ���ⶼҪ���� ���������α����н�����������ɢ�����������������棬Ҳ��Ƿ�ġ�
���������α��ڶ����ڽ������˶�ʱд��������ͬ�������ڻ���Ӵ�ʱ�� �˴˽���Է����������ɢ������������ɢ�����������ܼ�С���Է����̣�����ЧӦ��ֵ һ���С�����˷�����������������������ֵһ��ϴ������Ӿ������������ֵһ ��Ϊ����ǧ��•ÿĦ���������������� '
�����Ӿ�������±����Ϊ�������ܽ���������仯��������ѭ����ʾ��
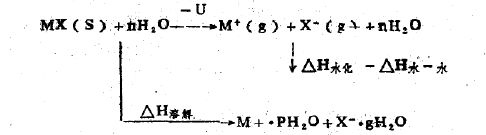
U��ʾ���Ӿ���ľ����ܣ���ָ���ɵ���̬�����������γ�1Ħ�����Ӿ������ų� �������������±����ľ�����һ��Ϊ������һǧ��ǧ��•ÿĦ����
��Hˮ����ʾ�����ε�ˮ���ȣ�P��Q�ֱ������������ӵ�ˮ������ˮ������ָ1Ħ����̬�������Ӻ�1Ħ����̬�����ӷֱ���ˮ�������ų�������֮�ͣ���ֵһ����Ϊ������һǧ��ǧ��•ÿĦ������Hˮ-ˮ��ʾˮ���ӿ˷��˴˾�������(�ر���������γ��������ʷ��ӻ����ӵĿ�Ѩ�����������������ʵ����ʼ���ˮ��ϵ������ͷ�ʽ�й�,���Ʋ⣬��ֵԼΪ100��300ǧ��•ÿĦ��,�й��鼮�н��������һ��,��Ϊˮ����,��ô����������ʵ����Ϊ������ˮ���ȿ˷���Hˮ-ˮ�ų���������
��H�ܽ�Ϊ�����ε��ܽ��ȣ�����ָ����1Ħ������������ˮ�γ�����ϡ����Һ����ЧӦ��
������ѭ�����ɵã�
��H�ܽ�=��Hˮ��һUһ��H ˮһˮ
�ɴ˿ɼ����������ܽ�ʱ���ƻ�������Ҫ����������ʹ�ܼ����ӱ˴˷���ҲҪ��������������ˮ����ų��������ܽ��Ⱦ�������������֮���ˮ���ȴ��ھ����ܼ� ��Hˮ-ˮ֮��ʱ���ܽ���ȣ���Һ�¶����룻 ��֮���ȣ���Һ�ضȽ��͡�
�����±���ᄃ��ľ�����U���Hˮ-ˮ֮����ˮ����ֵ����൱�����ܽ���һ �㶼�Dz������ֵ��ֵ����ˮ������ǿ�Ҷ����������С�ߣ�������������NaOH�� ��֮��������������NH4NO3
Һ�����ʣ���ŨH2SO4����ˮ�ų������ȣ�������H��������SO42�����ӷֱ���ˮ���÷ų������ϴ������ڿ˷�H2SO4���Ӽ�����H��������SO42�����Ӽ�������������֮�ʡ���һ���ͣ�ͬ��Ҳ�����������������ˮ�е��ܽ⡣
ͬ�����ǵ�����������ܽ���ˮ���˷�����Ӽ�������ˮ���Ӽ�����Ҫ�����ȣ�������ˮ���ӷ���ˮ��������ų�һ���������ܽ���Ҳ������������֮�
�ܽ��������ʡ��ܼ������ʣ��¶ȡ�Ũ�ȵ������йأ��������ʵĽṹ��ͬ��������ܽ�ʱ����������ЧӦ��һ����
��ˣ��ܽ���̵���ЧӦӦ�������ͣ�
���ʵ��ܽ���̾������ʵķ��ӻ��������ܼ����ӣ���ˮ���ӣ��������£��˷��˴����������ܼ�����ɢ�Ĺ��̡��������ܽ�ʱ�����ʵķ��ӻ�����Ҫ�˴˷��룬�ܼ��ķ���ҲҪ�˴˷��룬�ⶼҪ�����������ʵķ��ӻ��������ܼ���������ã������ܼ������ӣ���ˮ�Ϸ��ӣ������ӣ���ˮ�����ӣ��ų��������ܽ��Ⱦ�������������֮��ܽ�������Ǹ�ֵ���ܽ�ʱ���ȣ���Һ�¶����ߣ��ܽ����������ֵ���ܽ�ʱ�� �ȣ���Һ�¶Ƚ��͡�

- ȫ�����ۣ�0��
