为什么氯气、氨气容易液化?
时间:2017-04-30 17:53 来源:未知 作者:黄瑞 点击: 次 所属专题: 氨气 氯气
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
各种气态物质分子间的作用力不同,它们液化的难易也不一样,水在101KPa下低于100℃时就能液化,而要使氯气在室温下液化就必须加压才行。氢气和氧气则在室温下无论加多大压力都不能使它们液化。须将温度分别降到-239.8℃和-119℃时它们才能液化。
每种气体都有一个特定的温度,在这个温度以上,不论加多么大的压力都不能使其液化,这个特定温度就叫气体的临界温度。在临界温度时,使气体液化所需的最低压力叫临界压力。
下表列出某些气体的临界温度和临界压力。
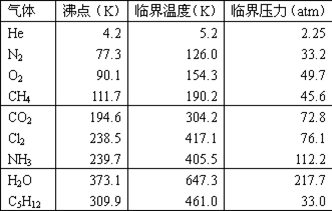
从表中数据可以看出,气体沸点越低,其临界温度也越低,它就越难液化。氦气是最难液化的气体。在室温下不能加压液化的He、N2、O2、CH4等称为“永久气体”。沸点低而临界温度高于室温的CO2、Cl2、NH3等在室温下加压就能液化,它们称为“可凝聚气体”。沸点和临界温度均高于室温的C5H12和H2O等,在常温常压下就是液体了。
为什么在临界温度以上无论加怎样大的压力都不能使气体液化呢?这是因为气体分子热运动引起的扩散膨胀因素只决定于温度,而与压力无关。温度高,分子热运动快,由热运动引起的扩散膨胀因素也明显,此时尽管加压可使分子间距离缩小,吸引力增大,但这种缩小不是无限制的。如加压使分子间距离缩到最小产生的引力尚不足以克服分子运动引起的扩散膨胀,那么气体仍不能液化,只有降温和加压同时采用,液化才有可能。
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
(604521673) 评论 href="/plus/view.php?aid=16282">为什么氯气、氨气容:三个sb,真的服了
曲氏半坡人(2900141694) 评论 href="/plus/view.php?aid=16282">为什么氯气、氨气容:哈哈哈哈哈哈
曲氏半坡人(2900141694) 评论 href="/plus/view.php?aid=16282">为什么氯气、氨气容:哈哈哈哈哈哈
曲氏半坡人(2900141694) 评论 href="/plus/view.php?aid=16282">为什么氯气、氨气容:哈哈哈哈哈
苍松(2900141679) 评论 href="/plus/view.php?aid=16282">为什么氯气、氨气容:一直以来都会很、、我是、
央视财经评论(123456789) 评论 href="/plus/view.php?aid=16282">为什么氯气、氨气容:我们的,我们都是一个我
还没有评论,快来抢沙发吧!
