甲烷的取代反应规律
时间:2022-08-07 08:10 来源:未知 作者:化学自习室 点击: 次 所属专题: 甲烷卤代
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
1.反应条件和反应物
反应条件为光照,反应物为卤素单质。例如甲烷与氯水、溴水不反应,但可与氯气、溴蒸气发生取代反应。
2.反应产物
虽然反应物的比例、反应的时间长短等因素会造成各种产物的比例不同,但甲烷与氯气反应的产物都是CH3Cl、CH2Cl2、CHCl3和CCl4四种有机物与氯化氢形成的混合物。

3.物质的量的关系
CH4与Cl2发生取代反应时,每1 mol H原子被取代,消耗1 mol Cl2分子,同时生成1 mol 的HCl分子。
4.注意事项
(1)有机反应比较复杂,常伴随很多副反应发生,因此有机反应方程式常用“→”。
(2)CH4与Cl2的反应逐步进行,应分步书写。
(3)当n(CH4)∶N(Cl2)=1∶1时,反应并不只发生CH4+Cl2 CH3Cl+HCl,其他反应仍发生。
CH3Cl+HCl,其他反应仍发生。
5.取代反应与置换反应的比较
取代反应 | 置换反应 |
可与化合物发生取代,生成物中不一定有单质 | 反应物、生成物中一定都有单质 |
反应能否顺利进行受催化剂、温度、光照等外界条件的影响较大。 | 在水溶液中进行的置换反应遵循金属或非金属活动性顺序 |
分步取代,很多反应是可逆的 | 反应一般是单向进行 |
深化理解
1.甲烷的卤代反应的产物是混合物,而不是纯净物。
2.甲烷等有机物与氯气发生取代反应时,取代的位置和个数是难以控制的,因此制备卤代烃一般不采用取代反应。
典型例题
例1将1 mol 甲烷与一定量的氯气混合于一量筒中,倒立于盛有饱和食盐水的水槽(如图所示),对于此反应,有关叙述不正确的是( )

A.该反应属于取代反应
B.该反应的条件是光照
C.该反应的生成物只有四种
D.该反应现象有量筒内气体颜色变浅,器壁上有油状液滴
答案C
【分析】CH4与Cl2在光照条件下发生取代反应,该反应的生成物有一氯甲烷、二氯甲烷、三氯甲烷、四氯甲烷、氯化氢五种产物,据此分析作答。
【详解】A.将1 mol 甲烷与一定量的氯气混合于一量筒中,甲烷与氯气发生取代反应,A项正确;
B.该取代反应需要光照条件,B项正确;
C.该反应的生成物有一氯甲烷、二氯甲烷、三氯甲烷、四氯甲烷、氯化氢五种产物,C项错误;
D.氯气参与反应,生成了液态有机物二氯甲烷、三氯甲烷、四氯甲烷,则量筒内气体颜色变浅,器壁上有油状液滴,D项正确;
答案选C。
例2(2020·四川省高一期中)若甲烷与氯气以物质的量之比1:3混合于试管中进行如下实验(如图),下列对于试管内发生的反应及现象的说法正确的是()

A.反应完全后,向饱和食盐水中加入紫色石蕊试液无变化
B.甲烷和Cl2反应后的产物只有CHCl3和HCl两种产物
C.反应过程中试管内黄绿色逐渐消失,试管壁上有油珠产生
D.CH4和Cl2完全反应后液面上升,液体充满试管
答案C
解析甲烷和Cl2在光照条件下发生取代反应,生成一氯甲烷、二氯甲烷、三氯甲烷、四氯甲烷和氯化氢,其中一氯甲烷和氯化氢是气体,二氯甲烷、三氯甲烷、四氯甲烷是油状液体。
A.反应生成氯化氢气体,氯化氢气体极易溶于水,反应完全后,向饱和食盐水中加入紫色石蕊试液,溶液会变红,A错误;
B.甲烷和Cl2在光照条件下发生取代反应是连锁反应,该反应可得到一氯甲烷、二氯甲烷、三氯甲烷、四氯甲烷以及氯化氢气体,B错误;
C.生成二氯甲烷、三氯甲烷、四氯甲烷都是难溶于水的油状液体,因此反应过程中试管内黄绿色逐渐消失,试管壁上有油珠产生,C正确;
D.反应生成的一氯甲烷、二氯甲烷、三氯甲烷、四氯甲烷都难溶于水,一氯甲烷呈气态,二氯甲烷、三氯甲烷、四氯甲烷是油状液体,氯化氢极易溶于水,因此完全反应后液面上升,液体不会充满试管,D错误;故答案为:C。
【点睛】高中化学常用的酸碱指示剂有甲基橙、石蕊和酚酞:
①甲基橙的变色范围为3.1~4.4,小于3.1为红色,在3.1~4.4之间为橙色,大于4.4为黄色;
②石蕊溶液变色范围为5.0~8.0,小于5.0为红色,在5.0~8.0之间为紫色,大于8.0为蓝色;
③酚酞试液变色范围为8.2~10.0,小于8.2为无色,在8.2~10.0之间为浅红色,大于10.0为红色。
变式强化
(2020·宜宾市叙州区第一中学校高一月考)利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下:

(1)B装置有三种功能:①控制气流速度;②均匀混合气体;③_______________。
(2)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x≧___________。
(3)D装置的石棉中均匀混有KI粉末,其作用是_________________________________。
(4)写出C装置中CH4与Cl2生成一氯代物的化学反应方程式:___________________.。
(5)①E装置中除盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为______。
A.分液法 B.蒸馏法 C.萃取分液法 D.结晶法
②该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为_______。
A.CH4 B.CH3Cl C.CH2Cl2 D.CHCl3
答案
(1)干燥混合气体(或吸水)
(2)4
(3)吸收过量的氯气
(4)CH4+Cl2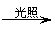 CH3Cl+HCl
CH3Cl+HCl
(5)AB
【分析】
在加热条件下,实验室用浓盐酸和二氧化锰反应制取氯气,在光照条件下,甲烷和氯气发生取代反应生成氯代烃和氯化氢,生成的黑色小颗粒为碳单质,氯气具有强氧化性,能将碘离子氧化生成碘单质,最后生成的氯化氢溶于水得到盐酸,互不相溶的液体采用分液的方法分离,一氯甲烷是气体,还可能有过量的甲烷,据此答题。
【详解】
在加热条件下,实验室用浓盐酸和二氧化锰反应制取氯气,在光照条件下,甲烷和氯气发生取代反应生成氯代烃和氯化氢,生成的黑色小颗粒为碳单质,氯气具有强氧化性,能将碘离子氧化生成碘单质,最后生成的氯化氢溶于水得到盐酸,互不相溶的液体采用分液的方法分离,一氯甲烷是气体,还可能有过量的甲烷;
(1)在加热条件下,二氧化锰和浓盐酸反应生成氯气,同时生成的氯气中还含有水分,浓硫酸具有吸水性、脱水性和强氧化性,所以b装置除了控制气流速度、均匀混合气体外,还有干燥作用;
(2)氯气与甲烷发生取代反应,反应特点是1mol 氯气可取代1mol H原子生成1mol HCl,设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则应保证甲烷被完全取代,x应大于或等于4;
(3)氯气具有强氧化性,能将碘离子氧化生成碘单质,所以D装置的石棉中均匀混有KI粉末,其作用是吸收过量的氯气;
(4)甲烷和氯气在光照条件下生成一氯甲烷和氯化氢,发生反应的化学方程式为CH4+Cl2 CH3Cl+HCl;
CH3Cl+HCl;
(5)①盐酸和有机物不能互溶,所以可以采用水洗分液的方法分离,故选A;
②反应生成的二氯甲烷、三氯甲烷、四氯化碳均是油状的液体,只有一氯甲烷是气体,即尾气中含有一氯甲烷,故答案为B。

- 全部评论(0)
