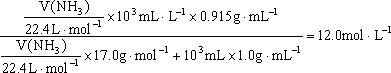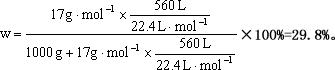物质的量浓度计算“七注意”
时间:2007-10-29 14:22 来源: 作者:王辉 点击: 次 所属专题: 物质的量浓度计算
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
物质的量浓度是关于溶液组成的一个重要物理量,是高中化学溶液有关计算的重要内容。物质的量浓度概念及表达式虽然比较简单,但不注意理解其内涵、不注意问题的特点,应用起来常常会容易出错。一般说来,要注意以下几方面的问题:
一、注意溶质是什么
溶液中的溶质是什么,是运用物质的量浓度表达式进行计算时首先要考虑的,对有些特殊情况,如![]()
![]() 等溶于水后所得溶质及氨水中溶质是什么等,要注意辨别。
等溶于水后所得溶质及氨水中溶质是什么等,要注意辨别。
例1:标准状况下,用一定量的水吸收氨气后制得物质的量浓度为![]() 、密度为
、密度为![]() 的氨水。试计算1体积水吸收多少体积的氨气可制得上述氨水。(本题中氨的相对分子质量为17.0,水的密度为
的氨水。试计算1体积水吸收多少体积的氨气可制得上述氨水。(本题中氨的相对分子质量为17.0,水的密度为![]() )
)
解析:很多同学认为氨水中的溶质为![]() ,导致计算出错。其实,我们习惯认为氨水中的溶质为
,导致计算出错。其实,我们习惯认为氨水中的溶质为![]() 。设水的体积为
。设水的体积为
二、注意溶液的体积
主要注意两点:一是不能用水的体积代替溶液的体积;二是当题设未给出溶液的密度时,可将各溶液(一般为稀溶液)的体积相加(如溶液混合、稀释),认为其和为溶液的总体积;当给出密度后则需通过密度进行换算求溶液的体积。
例2:在![]() 为、密度为
为、密度为![]() 的浓硫酸中加入一定量的水稀释成
的浓硫酸中加入一定量的水稀释成![]() 的硫酸,则加入水的体积( )
的硫酸,则加入水的体积( )
A. 小于100mL B. 等于100mL
解析:一些同学未考虑浓硫酸加水稀释后,溶液的密度会发生变化(减小),而直接将溶液和水的质量加和求体积。设加入水的体积为x mL,则![]() ,解得x=100,导致错选B项。
,解得x=100,导致错选B项。
三、注意单位运算
在概念理解及应用中,要注意各物理量的单位,一是各物理量的单位要相互匹配;二是注意从单位运算入手,能简化解题思路,快捷求解。
例3:标准状况下,1体积水大约溶解560体积氨。求:(1)所得氨水中溶质的质量分数?(2)若测得上述氨水的密度为![]() ,则此氨水的物质的量浓度为多少?(3)取此氨水10mL,加水稀释到
,则此氨水的物质的量浓度为多少?(3)取此氨水10mL,加水稀释到
解析:(1)注意单位量及比例关系。设取用水的体积为
(2)可用不同公式解答:
四、注意溶解度的影响
第一,物质的量浓度适合于表示不饱和及饱和溶液中溶质与溶剂的关系,不适合于过饱和溶液(溶质未溶解完全);第二,注意一些典型问题,如![]() 的溶解度情况及气体物质在溶液中的溶解问题等。
的溶解度情况及气体物质在溶液中的溶解问题等。
例4:将![]() 的硫酸中以制取
的硫酸中以制取![]() 气体,反应完全后,若溶液中+4价硫元素的物质的量浓度为
气体,反应完全后,若溶液中+4价硫元素的物质的量浓度为![]() ,假定溶液的体积不变,忽略溶液及导管中的气体体积。求:(1)溶液中硫元素的质量。(2)收集到
,假定溶液的体积不变,忽略溶液及导管中的气体体积。求:(1)溶液中硫元素的质量。(2)收集到![]() 气体的体积。(3)溶液中Na+和H+的物质的量浓度(不考虑弱电解质的电离)。
气体的体积。(3)溶液中Na+和H+的物质的量浓度(不考虑弱电解质的电离)。
解析:本题涉及![]() 气体在溶液中的溶解问题,只有
气体在溶液中的溶解问题,只有![]() 在水中溶解量达到饱和后,才有气体逸出,因此,在计算收集到的气体体积时要减除溶解量。根据题意有以下关系量:
在水中溶解量达到饱和后,才有气体逸出,因此,在计算收集到的气体体积时要减除溶解量。根据题意有以下关系量:
0.1mol 0.8mol(过量) 0.02mol(溶解量)
五、注意密度变化规律
在溶液混合和溶液稀释等问题中,在注意溶液体积变化的同时,还要考虑溶液密度的变化对溶液物质的量浓度的影响。如强酸、强碱、盐等溶液的密度随浓度增大而增大;氨水、乙醇等溶液的密度随浓度增大而减小。
例5:若以![]()
![]()
A. ![]()
![]()
C. ![]()
![]()
解析:设溶液的体积为VL,密度为![]() ,溶质的摩尔质量为M g·
,溶质的摩尔质量为M g·![]() ,质量分数为
,质量分数为![]() ,物质的量浓度为
,物质的量浓度为![]() 。根据溶液物质的量浓度的表达方式不同,但其溶质的量不变,有V L×103 mL·
。根据溶液物质的量浓度的表达方式不同,但其溶质的量不变,有V L×103 mL·![]() ,即
,即![]() 。依题意有
。依题意有![]() ,因
,因![]() ,又由于氨水的密度比纯水小,且浓度越大,密度越小,即
,又由于氨水的密度比纯水小,且浓度越大,密度越小,即![]() ,代入上式
,代入上式![]() 。故答案为C项。
。故答案为C项。
六、注意实验情景
在计算溶液配制或溶液稀释等问题中溶液物质的量浓度时,一要注意不能把水的体积当作溶液的体积;二是在配制溶液时,要注意容量瓶规格与实际配制溶液体积的关系。
例6:实验室需用480mL ![]() 的硫酸铜溶液,现选取500mL容量瓶进行配制,以下操作正确的是( )
的硫酸铜溶液,现选取500mL容量瓶进行配制,以下操作正确的是( )
A. 称取
B. 称取
C. 称取
D. 称取
![]() ,选A项;也有一些同学选C项,这里包含两个错误:一是用500mL容量瓶进行配制时,溶质的质量应满足500mL容量瓶的需求;二是错把溶剂的体积当作溶液的体积,正确情况应该是“称取
,选A项;也有一些同学选C项,这里包含两个错误:一是用500mL容量瓶进行配制时,溶质的质量应满足500mL容量瓶的需求;二是错把溶剂的体积当作溶液的体积,正确情况应该是“称取
七、注意物质与其组成微粒的关系
物质与其组成微粒的物质的量、物质的量浓度之间的关系可以通过电离方程式进行分析。组成微粒的某量=对应物质的某量×物质组成中该微粒的数目。此类问题在近几年高考中出现频率较高,需引起注意。
例7:今有300mL ![]() 溶液、
溶液、![]() 溶液和
溶液和 ![]() 溶液,这三种溶液中
溶液,这三种溶液中![]() 的浓度之比为( )
的浓度之比为( )
A. 1:1:1 B. 3:2:
解析:本题易错选A项或C项,错选A项是对物质与其组成微粒的关系把握不准造成的;错选C项是因为审题不仔细,有些同学看到浓度、体积就想到求物质的量,将题设数据分别相乘,再比较得到C项,而未细看题目要求。本题是要计算![]() 的浓度之比,审题仔细后,很容易得到答案为D项。
的浓度之比,审题仔细后,很容易得到答案为D项。

- 全部评论(0)