何谓同离子效应?
时间:2021-09-23 09:16 来源: 作者:朱照鹰 点击: 次 所属专题: 同离子效应
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
由于加入含相同离子的强电解质,使弱电解质电离度减小或使难溶盐溶解度降低的效应,叫同离子效应。分别说明如下:
①使弱电解质电离度减小
例如,在醋酸溶液中加入醋酸钠,由于醋酸钠是强电解质,在水中全部电离成Na+和 Ac-,溶液中Ac-浓度增大,大量的 Ac-同H+结合成醋酸分子,使醋酸的电离平衡向左移动:
HAc![]() H++Ac-
H++Ac-
因此,醋酸的电离度减小,溶液中H+浓度降低。在弱碱溶液中加入弱碱盐,例如,在氨水中加入氯化铵,也存在同离子效应。有同离子效应时计算氢离子浓度的一般公式为:
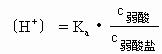
式中Ka为弱酸的电离常数,c为浓度。同理可得:
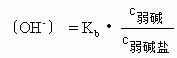
式中Kb为弱碱的电离常数。
②使难溶盐溶解度降低
例如,硫酸钡饱和溶液中,存在如下平衡:
![]()
在上述饱和溶液中加入氯化钡,由于氯化钡完全电离,溶液中[Ba2+]突然增大,[Ba2+][SO42-]>Ksp,原来的平衡遭到破坏,平衡向左移动,析出BaSO4沉淀。当溶液中再次建立新的平衡,即〔Ba2+〕[SO42-]=Ksp时,[Ba2+]大于BaSO4溶解在纯水中的钡离子浓度,而[SO42-]则小于BaSO4溶解在纯水中的硫酸根浓度,硫酸钡的溶解度可用新的平衡状态下的[SO42-]来量度,因此,BaSO4在BaCl2溶液中的溶解度比在纯水中要小。即加入含相同离子的强电解质BaCl2使难溶盐BaSO4的溶解度降低。同离子效应也可以降低易溶电解质的溶解度。例如,在饱和的NaCl溶液中加入浓盐酸或通入氯化氢气体,也可以使NaCl晶体析出。
(责任编辑:)

说点什么吧
- 全部评论(0)
还没有评论,快来抢沙发吧!
