同离子效应与盐效应
时间:2013-04-11 10:34 来源:未知 作者:翟娜 点击: 次 所属专题: 同离子效应 盐效应
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
若在难溶电解质溶液中,加入一种与难溶电解质无共同离子的电解质,将使难溶电解质的溶解度增大。这种由于加入了易溶的强电解质而增大难溶电解质溶解度的现象称作盐效应。例如BaSO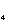 在KNO
在KNO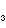 溶液中的溶解度就比在纯水中稍大,并且KNO
溶液中的溶解度就比在纯水中稍大,并且KNO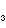 浓度越大,BaSO
浓度越大,BaSO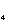 的溶解度也变得越大。这是因为KNO
的溶解度也变得越大。这是因为KNO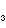 的加入使溶液中的离子强度大大增加,溶液中离子的有效浓度(即活度а)降低,使原来已达平衡时J
的加入使溶液中的离子强度大大增加,溶液中离子的有效浓度(即活度а)降低,使原来已达平衡时J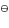 =
=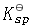 的情况变为J
的情况变为J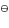 <
<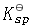 ,必须多溶解一些BaSO
,必须多溶解一些BaSO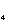 沉淀。增加溶液中相应的离子浓度才能达到新的平衡。使得溶液中BaSO
沉淀。增加溶液中相应的离子浓度才能达到新的平衡。使得溶液中BaSO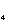 沉淀减少。因此BaSO
沉淀减少。因此BaSO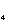 沉淀在KNO
沉淀在KNO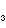 溶液中,Ba
溶液中,Ba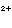 和SO
和SO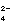 离子浓度比在纯水中大。
离子浓度比在纯水中大。
在难溶电解质的饱和溶液中,加入一种与难溶电解质含有相同离子的强电解质,难溶电解质的沉淀平衡将发生移动,其结果可使难溶电解质的溶解度降低。这种因加入含有共同离子的电解质而使沉淀溶解度降低的效应叫做沉淀溶解平衡中的同离子效应。例如在难溶电解质BaSO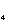 饱和溶液中,加入含有相同离子的强电解质Na
饱和溶液中,加入含有相同离子的强电解质Na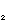 SO
SO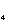 溶液,使BaSO
溶液,使BaSO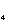 的溶解度降低。
的溶解度降低。
BaSO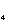 (s)
(s) Ba
Ba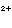 (aq) + SO
(aq) + SO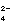 (aq)
(aq)
Na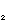 SO
SO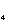 → 2Na
→ 2Na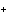 (aq) + SO
(aq) + SO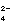 (aq)
(aq)
这是因为一定温度下,在BaSO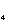 饱和溶液中,J
饱和溶液中,J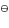 =[Ba
=[Ba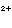 ][SO
][SO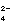 ]=
]=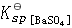 ,加入Na
,加入Na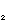 SO
SO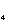 后,Na
后,Na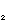 SO
SO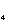 在水中完全离解使溶液中SO
在水中完全离解使溶液中SO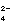 离子浓度增大。此时J
离子浓度增大。此时J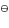 = c(Ba
= c(Ba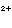 )·c(SO
)·c(SO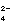 )>
)>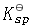 ,平衡遭到破坏,反应向着生成沉淀方向移动,将析出更多的BaSO
,平衡遭到破坏,反应向着生成沉淀方向移动,将析出更多的BaSO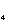 ,直至再次建立平衡 (J
,直至再次建立平衡 (J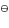 =
=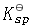 )为止。
)为止。
盐效应和同离子效应是影响沉淀完全度的两个主要因素,同离子效应可以降低难溶电解质的溶解度,盐效应可以增大难溶电解质的溶解度。
在难溶电解质的饱和溶液中,加入一种与难溶电解质含有相同离子的强电解质,难溶电解质的沉淀平衡将发生移动,其结果可使难溶电解质的溶解度降低。这种因加入含有共同离子的电解质而使沉淀溶解度降低的效应叫做沉淀溶解平衡中的同离子效应。例如在难溶电解质BaSO
BaSO
Na
这是因为一定温度下,在BaSO
盐效应和同离子效应是影响沉淀完全度的两个主要因素,同离子效应可以降低难溶电解质的溶解度,盐效应可以增大难溶电解质的溶解度。
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
还没有评论,快来抢沙发吧!
