相对原子质量和相对分子质量及摩尔质量的比较
时间:2007-12-25 12:41 来源: 作者:单莹 点击: 次 所属专题: 摩尔质量 分子量 原子量
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、相对原子质量:
1、相对原子质量:

2、几个有关相对原子质量的概念的区别:
(1)同位素的质量数是同位素原子中质子和中子相对质量的整数部分之和,它是个正整数。由于质子和中子的相对质量都近似等于1,所以质量数在数值上等于原子中质子数和中子数之和。但质量数不只是微粒个数,它是一个属于质量范畴的数值。质量数是对某种同位素而言的,如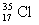 的质量数是35。对于一种元素来说,没有一种质量数跟它相对应,因此讲氯元素的质量数是35是错误的。
的质量数是35。对于一种元素来说,没有一种质量数跟它相对应,因此讲氯元素的质量数是35是错误的。
(2)同位素的相对原子质量是把该同位素原子质量与作为相对原子质量标准的碳原子质量的1/12的比值,通常它不是整数。由于一种元素通常有几种同位素,这几种同位素原子由于其核内中子数目不同而有着不同的质量,与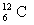 的1/12的比值也不相同。如氯元素的两种同位素
的1/12的比值也不相同。如氯元素的两种同位素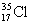 和
和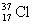 ,它们的相对原子质量分别是34.969和36.966。
,它们的相对原子质量分别是34.969和36.966。
(3)元素的相对原子质量是按该元素的各种天然同位素的相对原子质量和所占的原子的物质的量分数(或称丰度)算出来的平均值(注意此处用的是原子的物质的量分数而不是质量分数),即元素的相对原子质量=MA·a%+MB·b%+MC·c%+…(MA,MB,MC…是各同位素的相对原子质量,a%,b%,c%…是各同位素原子的物质的量分数)。《国际原子量表》中列出的相对原子质量,就是各元素的平均相对原子质量。如天然氢是由两种同位素1H和2H组成,它们的同位素相对质量分别是1.00782和2.0140,同位素丰度分别是99.985%和0.015%,所以氢元素的相对原子质量=1.00782×99.985%+2.0140×0.015%=1.00794。
(4)元素的近似相对原子质量是按该元素的各种天然同位素的质量数和所占的原子的物质的量分数(或称丰度)计算出来的平均值。计算公式与元素的相对原子质量相同,只是式中MA,MB,MC…表示各同位素的质量数。
(2)同位素的相对原子质量是把该同位素原子质量与作为相对原子质量标准的碳原子质量的1/12的比值,通常它不是整数。由于一种元素通常有几种同位素,这几种同位素原子由于其核内中子数目不同而有着不同的质量,与
(3)元素的相对原子质量是按该元素的各种天然同位素的相对原子质量和所占的原子的物质的量分数(或称丰度)算出来的平均值(注意此处用的是原子的物质的量分数而不是质量分数),即元素的相对原子质量=MA·a%+MB·b%+MC·c%+…(MA,MB,MC…是各同位素的相对原子质量,a%,b%,c%…是各同位素原子的物质的量分数)。《国际原子量表》中列出的相对原子质量,就是各元素的平均相对原子质量。如天然氢是由两种同位素1H和2H组成,它们的同位素相对质量分别是1.00782和2.0140,同位素丰度分别是99.985%和0.015%,所以氢元素的相对原子质量=1.00782×99.985%+2.0140×0.015%=1.00794。
(4)元素的近似相对原子质量是按该元素的各种天然同位素的质量数和所占的原子的物质的量分数(或称丰度)计算出来的平均值。计算公式与元素的相对原子质量相同,只是式中MA,MB,MC…表示各同位素的质量数。
例1:下表是氯元素的两种同位素的相对原子质量和各同位素原子的丰度数据: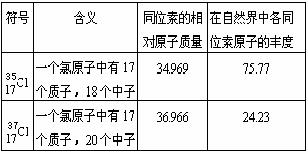

氯元素的相对原子质量是:各同位素的相对原子质量与其丰度的乘积之和,即:34.969×75.77%+36.966×24.23%=35.453。
氯元素的近似相对原子质量是:各天然同位素的质量数(近似相对原子质量)与其丰度的乘积之和,即: 35×75.77%+37×24.23%=35.485。
例2:自然界中硼有两种同位素:10B和11B,又测得硼的相对原子量为10.8,试求10B和11B的原子个数比。
[提示]应用求平均相对原子质量的公式,也可用十字交叉法
解:设自然界中硼的原子总数为100,其中含10B为X,则11B为100-x
解得:x=20(10B)故11B含量为80
10B:11B=20∶80=1∶4
二、相对分子质量:
1、 相对分子质量:
分子是由原子构成的,把构成分子的每一种原子的相对原子质量(还要乘上分子中原子的个数)相加,得出的数值即为相对分子质量。单位也是“1”,一般不写出。
H2O的相对分子质量=2×1+16×1=18
H2SO4 的相对分子质量=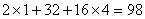
2、 平均相对分子质量:
平均相对分子质量适用于混合物,常用于混合气体。
平均相对分子质量相当于把混合物看作一个“单一组分”,这一“单一组分”的相对分子质量就是平均相对分子质量。(相关的计算见平均摩尔质量部分)
三、摩尔质量
1、 定义:单位物质的量的物质所具有的质量叫做摩尔质量。即含阿伏加德罗常数个粒子的总质量。
2、单位:g/mol或kg/mol。
3、摩尔质量与相对原子质量、相对分子质量的关系。 区别:摩尔质量是由物质质量除以物质的量得到的,单位是g · mol-1;物质的相对原子质量或相对分子质量,是以12C原子质量的1/12为标准,其他原子或分子的质量与它相比较而得到的,这是一个相对比值,单位为1,一般不写出。 联系:摩尔质量以g/mol为单位时,在数值上等于该物质的相对原子质量或相对分子质量。
即:①1mol任何粒子或物质的质量,②任何物质的摩尔质量,③该物质的相对分子(原子)质量三者数值相等,单位各不相同。
3、摩尔质量与相对原子质量、相对分子质量的关系。 区别:摩尔质量是由物质质量除以物质的量得到的,单位是g · mol-1;物质的相对原子质量或相对分子质量,是以12C原子质量的1/12为标准,其他原子或分子的质量与它相比较而得到的,这是一个相对比值,单位为1,一般不写出。 联系:摩尔质量以g/mol为单位时,在数值上等于该物质的相对原子质量或相对分子质量。
即:①1mol任何粒子或物质的质量,②任何物质的摩尔质量,③该物质的相对分子(原子)质量三者数值相等,单位各不相同。
三者关系具体表示实例: ①原子或简单离子 例如:O的相对原子质量为16,则1molO的质量为16g,O的摩尔质量为16g/mol;Na+的相对原子质量为23,则1mol Na+的质量为23g,Na+的摩尔质量为23g/mol。 ②分子 例如:H2O的相对分子质量为18,则1mol H2O的质量为18g,H2O的摩尔质量为18g/mol。
③较复杂的离子,如原子团 例如:NH4+式量为18,则1molNH4+的质量为18g,NH4+的摩尔质量为18g/mol。
③较复杂的离子,如原子团 例如:NH4+式量为18,则1molNH4+的质量为18g,NH4+的摩尔质量为18g/mol。
例1、下列关于摩尔质量的论述正确的是:
A.氢的摩尔质量是1g/mol B.1个氮分子的摩尔质量为28g
C.水的摩尔质量为18g D.NO3-的摩尔质量为62g/mol
A.氢的摩尔质量是1g/mol B.1个氮分子的摩尔质量为28g
C.水的摩尔质量为18g D.NO3-的摩尔质量为62g/mol
[分析]A选项没有指明是氢分子还是氢原子,故为无效答案; B选项有两点错误: 一是单位,摩尔质量的单位为g/mol,不是g; 二是摩尔质量与微粒种类有关,即与个数无关,N2的摩尔质量使用时总为28g·mol-1; C选项单位不正确。故正确答案为D。
例2:一个碳-12原子的质量为mg,某元素一个原子的质量为ng,则该元素原子的相对原子质量为:
A.m/ 12n B.12n/m C.n/ 12m D.nNA (NA代表阿佛伽德罗常数)
[分析]根据相对原子质量的概念,该元素原子的相对原子质量为:
ng/(mg/ 12)= 12n/m,所以答案B正确。
A.m/ 12n B.12n/m C.n/ 12m D.nNA (NA代表阿佛伽德罗常数)
[分析]根据相对原子质量的概念,该元素原子的相对原子质量为:
ng/(mg/ 12)= 12n/m,所以答案B正确。
根据摩尔质量的概念,该元素原子的相对原子质量为:
M=ng·NA mol-1=nNA g · mol-1, 所以答案D正确。
4、摩尔质量与平均摩尔质量: 摩尔质量通常是针对单一组分而言,若涉及的是多组分的混合物,则混合物用平均摩尔质量。(与相对分子质量求法相同,只是单位不同)
有三种计算方法:
(1)根据混合物中各组分在混合物中所占的物质的量分数(对气体而言,也就等于体积分数)来计算,其数学表达式为:
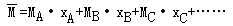 (MA,MB,MC…是A、B、C的相对原子质量,XA,XB,XC…是A、B、C的物质的量分数))
(MA,MB,MC…是A、B、C的相对原子质量,XA,XB,XC…是A、B、C的物质的量分数))
(2)根据摩尔质量的概念来确定
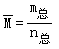
m总和n总分别为混合物的总质量和总的物质的量
(3)根据密度计算
①在标准状况下: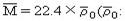 标况下混合气体密度)
标况下混合气体密度)
(2)根据摩尔质量的概念来确定
m总和n总分别为混合物的总质量和总的物质的量
(3)根据密度计算
①在标准状况下:
②根据相对密度计算:设混合气体对某气体(相对分子质量为M)的相对密度为d,则混合气体的平均相对分子质量为: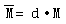
例 1、某混合气体的质量分数:H2为72%,N2为28%,计算该混合气体的平均相对分子质量。
一般可设总质量为100g,则H2为72g,N2为28g。
方法一:依据物质的量分数计算(而不是质量分数!)
n(H2)=72/2=36(mol) n(N2)=28/28=1(mol)
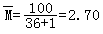
方法二:依据摩尔质量概念计算
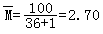
例 1、某混合气体的质量分数:H2为72%,N2为28%,计算该混合气体的平均相对分子质量。
一般可设总质量为100g,则H2为72g,N2为28g。
方法一:依据物质的量分数计算(而不是质量分数!)
n(H2)=72/2=36(mol) n(N2)=28/28=1(mol)
方法二:依据摩尔质量概念计算
例2、实验测得乙烯与氧气混合气体密度是H2的14.5倍,可知其中乙烯的物质的量分数为:
A.25.0% B.27.0% C.72.4% D.75.0%
[提示]可用公式法,也可用十字交叉法
解:先求出混合气体平均相对分子质量=14.5×2=29,可用十字交叉法求出乙烯与氧气的物质的量比
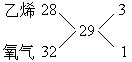
物质的质量比C2H4∶O2=3∶1 故选D
例3、某固体仅由一种元素组成,其密度为5g/cm3,用射线研究该固体的结果表明:在棱长为1×10-7cm的立方体中含有20个原子,则此元素的相对原子质量接近: A.32 B.65 C.120 D.150 [分析]要求该元素的相对原子质量,亦即先求1mol该元素原子的质量,即6.02×1023个该原子的质量。由题意,20个原子的质量m=ρV=5g·cm-3×(1×10-7cm)3=5×10-21g,故1mol该原子约为6.02×1023×5×10-21g/20=150g,所以该元素的摩尔质量约为150g/mol,此元素的相对原子质量接近于150。 答案为:D。
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
笔名 评论 href="/plus/view.php?aid=5600">相对原子质量和相对:多谢您的教导
还没有评论,快来抢沙发吧!
