浅析羧酸的还原性
时间:2021-12-20 11:13 来源:未知 作者:黄蒲山 点击: 次 所属专题: 羧酸
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
在进行烃的衍生物教学时,都会对醇、醛、酸 三者之间总结出如下的一个关系:

在这个关系中,醛会还原生成醇,但缺少了羧酸还原成醛的反应,由此很多人都认为羧酸不能还原成醛,那么羧酸能不能还原生成醛呢?
事实上,羧酸并不是不能被还原,而是由于羧酸分子中羧基具有较强的稳定性,一般条件下难于还原生成醛。另外从分子组成上来看,羧酸分子加氢后与醛的分子组成并不相同,这样使人易 产生误解,认为羧酸不能被还原。下面就有关羧基的还原问题谈点认识。
一、羧基的稳定性
羧酸中,羧基碳原子以sp2杂化的形式形成 三个杂化轨道,这三个杂化轨道一个与氧原子成 键,一个与羟基氧成键,一个与氢或烃基成键。三 个轨道在一个平面上,键角大约为120°。另外碳 原子剩余的一个p轨道与氧原子上的一个p轨道 形成一个π键,从而使碳氧原子间形成了双键,因此羧基具有下列结构:
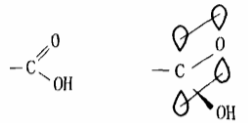
与醛不同,羧基中碳原子除了与氧原子形成 碳氧双键以外,还与一个羟基氧原子相连,羟基氧 原子上的孤对电子能与碳氧双键共扼,也正是由 于这种共扼作用,一方面增加了羧基中C =O间 的稳定性,其结果使得羧基中C=O比醛基中的 C=O难以发生加氢还原;另一方面也增加了碳原 子与羟基氧原子之间的稳定性,使得羟基上的氢 原子更容易电离为氢离子而使羧酸显酸性。
二、羧酸的还原反应
由于羧基C=O因羟基氧原子的共轭作用变得稳定,羧酸很难用催化加氢(H2/Ni)进行还原,但氢化锂铝能顺利地把羧酸先还原为醛,并继续还原为一级醇,例如:
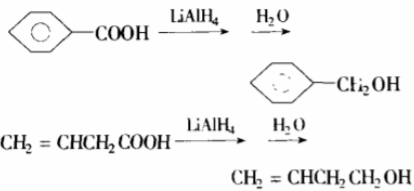
用氢化锂铝还原时,常用的溶剂是无水乙醚、四氢呋喃等,反应时首先形成羧酸锂盐:
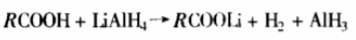
AlH3与羧酸锂接近,与羰基氧形成复合物,然后将负氢离子从铝转移到羰基碳上,再消除成醛:

醛可以继续与氢化锂铝反应,然后用稀酸水解最终生成一级醇。
由此可以看到,羧酸是可以被还原的,但还原时需要有适宜的还原剂,在总结醇、醛、酸三者的关系时,空缺了酸与醛间的还原关系,我们只能理解为这是超出中学化学范围的一个问题,但必须对此有一个正确的认识。
三、其它
中学化学教学中,所涉及的有机还原反应主要有不饱和的烯、炔、芳香烃加氢还原以及含氧衍生物中醛的加氢还原,在有机化学中,常用的还原剂有H2/Ni、NaBH4、LiAlH4等下面按照还原剂的类型对一些还原反应做一小结。
1.H2/Ni(催化加氢)
催化加氢一般适用于碳碳双键加氢,室温下可发生,例如:
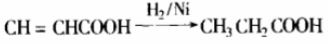
升高温度时可以还原羰基、氰基,但不能还原羧基。酯基需特殊催化剂才能加氢还原,苯环加氢需高温高压,故分子中有苯环的其它官能团加氢,一般不影响苯环,例如:
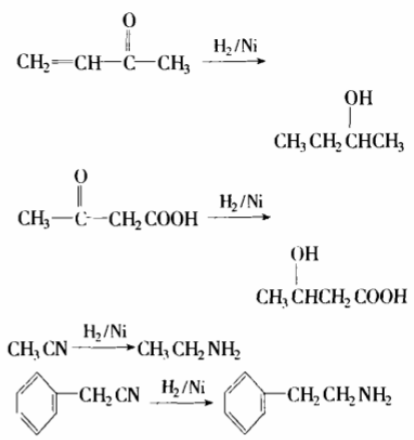
2.NaBH4
这是一种可以在水溶液中使用的还原剂,但仅能把醛、酮还原成醇,对其它任何官能团无影响,例如:
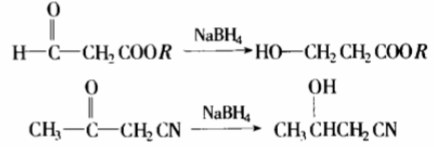
3. LiAlH4
这是一种还原能力很强的还原剂,只能在乙醚中使用,遇水爆炸,空气中可以自燃。它能把醛、酮、羧基、酯还原成醇,把氰基还原成胺,但不与碳碳双键及苯环作用,如:
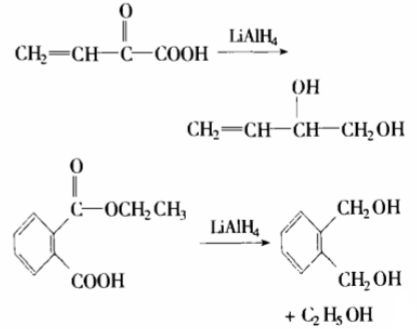
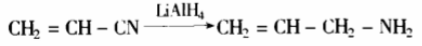
在有机化学中使用的还原剂还有很多,能发生还原反应的有机物也还有很多,限于篇幅不再一一赘述。

- 全部评论(0)
(1198896436) 评论 href="/plus/view.php?aid=15931">浅析羧酸的还原性:????????????????????????????
