溶解度较小的难溶电解质能否转化为溶解度较大的难溶电解质?
时间:2020-03-09 13:58 来源:未知 作者:蔡惠君 点击: 次 所属专题: 溶度积计算 沉淀转化
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
以BaSO4 沉淀转化为BaCO3 沉淀为例。
Ksp(BaSO4)=1.07×10-10,Ksp(BaCO3)=2.58×10-9。
溶度积:Ksp(BaSO4) <Ksp(BaCO3 ),但相差不大,工业上能实现BaSO4 沉淀转化为BaCO3 沉淀,具体做法是把BaSO4 置于一定量的饱和Na2CO3 溶液中浸泡,再充分搅拌,弃去上层清液;如此处理多次,可使绝大部分BaSO4 转化为BaCO3。
沉淀转化的原理如下:在Na2CO3 的饱和溶液中,加入BaSO4 后,少量溶解的Ba2+和CO32- 结合生成BaCO3 沉淀,使溶液中c (Ba2+) 降低,BaSO4 沉淀溶解平衡向溶解方向移动,BaSO4 逐渐溶解,直到建立新的平衡,此过程可表示如下:
BaSO4 Ba2++SO42-
Ba2++SO42-
Na2CO3=CO32-+2Na+
Ba2++CO32-=BaCO3 ↓
总反应:BaSO4(s)+CO32-  BaCO3(s)+SO42-
BaCO3(s)+SO42-
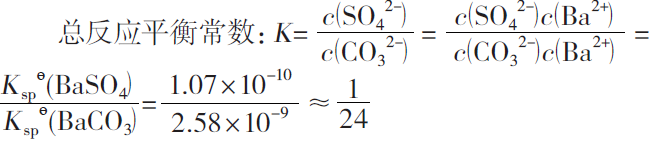
根据平衡移动原理,当溶液中

淀方向转化,由于总反应平衡常数 K= 不是很小,因而当CO32- 浓度足够大时,反应是可以向右进行的,实现BaSO4 沉淀转化为BaCO3 沉淀。
[ 结论] 一般来讲,溶解度较大的难溶电解质容易转化为溶解度较小的难溶电解质。但是欲将溶解度较小的难溶电解质转化为溶解度较大的难溶电解质就比较困难,如果溶解度相差不大,转化可能实现;如果溶解度相差太大,则转化实际上不能实现。
(责任编辑:)

说点什么吧
- 全部评论(0)
还没有评论,快来抢沙发吧!
