常见物质推断题突破口
时间:2020-03-30 21:44 来源: 作者:邵磊 点击: 次 所属专题: 无机推断突破口
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
方法一:根据物质的特殊颜色推断
知识准备:物质颜色
1.有色固体:白色:Fe(OH)2、CaCO3、BaSO4、AgCl、BaSO3、铵盐,白色或黄色腊状固体:白磷
淡黄色或黄色:S 黄或浅黄、FeS2 黄、AgI 黄、Au 黄、Na2O2 浅黄、AgBr 浅黄、Ag3PO4浅黄等。
红色或红棕色:Cu 紫红、 Cu2O 红、Fe2O3 红、Fe(OH)3红褐色
黑色:C、CuS、Cu2S 、FeS 、MnO2、FeO、Fe3O4(磁性物质)、CuO、PbS 、Ag2O棕黑
紫黑色:I2 紫黑、KMnO4 紫黑
2.有色溶液: Cu2+蓝、 MnO4-紫红、Fe2+ 浅绿、Fe3+ 棕黄、Fe(SCN)3 血红、NO2-浅黄。
氯水浅黄绿色、溴水橙黄色、碘水棕黄色、溴的有机溶液 橙红—红棕、I2的有机溶液 紫红
3.有色气体:Cl2(黄绿色)、Br2(g)(红棕色)、NO2、(红棕色)、I2(紫色)O3(淡蓝色)
4.物质的状态、气味硬度等:
呈液态的金属单质:Hg 呈液态的非金属单质:Br2
常温呈气态的单质:H2、O2、Cl2、N2、F2、稀有气体等。
刺激性气味的气体: SO2、NH3、HCl、Cl2、臭鸡蛋气味的气体:H2S
地壳中元素的含量:O、Si、A、Fe、硬度最大的单质:C(金刚石)
形成化合物种类最多的元素: C
方法二、根据特征反应现象推断
知识准备:特征反应现象
1.焰色反应:Na+(黄色)、K+(紫色)
2.能使品红溶液褪色的气体可能是:加热恢复原颜色的是SO2,不恢复的是Cl2、NaClO、Ca(ClO)2等次氯酸盐、氯水、过氧化钠、过氧化氢、活性碳等
3.![]() (由白色→灰绿→红褐色)
(由白色→灰绿→红褐色)
4.能在空气中自燃:P4
5.在空气中变为红棕色:NO
6.能使石灰水变浑浊:CO2、O2
7.通CO2变浑浊:石灰水(过量变清)、Na2SiO3、饱和Na2CO3、浓苯酚钠、NaAlO2
8.气体燃烧呈苍白色:H2在Cl2中燃烧;在空气中点燃呈蓝色:CO、H2、CH4
9.遇酚酞显红色或湿润红色石蕊试纸变蓝的气体:NH3(碱性气体)
10.使湿润的淀粉碘化钾试纸变蓝:Cl2、Br2、FeCl3、碘水等。
11.加苯酚显紫色或加SCN-显血红色或加碱产生红褐色沉淀,必有Fe3+
12.遇BaCl2生成不溶于硝酸的白色沉淀,可能是:SO42—、Ag+、 SO32—
13.遇HCl生成沉淀,可能是: Ag+、 SiO32—、AlO2—、S2O32—
14.遇H2SO4生成沉淀,可能是:Ba2+、Ca2+、S2O32—、SiO32—、AlO2—
15.与H2S反应生成淡黄色沉淀的气体有Cl2、O2、SO2、NO2
16.电解时阳极产生的气体一般是:Cl2、O2,阴极产生的气体是:H2
17.两种气体通入水中有沉淀的是2H2S+SO2=3S+2H2O
同一元素的气态氢化物和最高价氧化物对应的水化物生成盐的元素一定是氮(NH4NO3)
18.两种溶液混合生成沉淀和气体,这两种溶液的溶质可能是
①Ba(OH)2与(NH4)2SO4或(NH4)2CO3或(NH4)2SO3
②强烈双水解
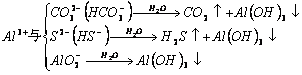 |
③可溶性铁盐与可溶性碳酸盐或碳酸氢盐
④Na2S2O3溶液与强酸
19.能使溴水褪色的物质:H2S和SO2及它们相对应的盐、活泼金属、不饱和烃、醛、酚、碱
20.两物质反应先沉淀后溶解的有:CO2与Ca(OH)2或Ba(OH)2、NaOH与铝盐、氨水与AgNO3、强酸与偏铝酸盐
知识准备:依据特征结构
1.正四面体型分子:CH4、SiH4、CCl4、SiCl4、P4等。
2.直线型分子:乙炔、二氧化碳、二硫化碳等。
3.平面型分子: 苯、乙烯等。
4.含有非极性共价键的离子化合物:过氧化钠(Na2O2)、二硫化亚铁(FeS2)等。
5.含有10个电子的粒子:离子:O2— 、F—、Ne、Na+、Mg2+、Al3+、NH4+、H3O+、OH—、NH2—
分子:CH4、NH3、H2O、HF
6.电子总数为18的粒子:分子:Ar、F2、SiH4、PH3、H2S、HCl、H2O2、C2H6、CH3OH、CH3NH2、CH3F、 NH2 OH、 NH2—NH2 等;离子:K+、Ca2+、HS—、S2—、Cl—、O22—
7.9个电子的粒子:—OH、—CH3、—NH2、F
方法三、根据特殊反应条件推断
知识准备:熟悉具有特殊反应条件的反应,多数是重要工业生产反应
1、高温条件
C+H2O![]() H2+CO,C+2H2O
H2+CO,C+2H2O![]() CO2+2H2,3Fe+4H2O
CO2+2H2,3Fe+4H2O![]() Fe3O4+4H2,CaCO3
Fe3O4+4H2,CaCO3![]() CaO+CO2,SiO2+CaCO3
CaO+CO2,SiO2+CaCO3![]() CaSiO3+CO2,SiO2+2C
CaSiO3+CO2,SiO2+2C![]() Si+2CO↑,SiO2+CaO
Si+2CO↑,SiO2+CaO![]() CaSiO3,4FeS2+11O2
CaSiO3,4FeS2+11O2![]() 2Fe2O3+8SO2,SiO2+Na2CO3
2Fe2O3+8SO2,SiO2+Na2CO3![]() Na2SiO3+CO2
Na2SiO3+CO2
2、高温高压催化剂:N2+3H2![]() 2NH3
2NH3
3、催化剂、加热: 4NH3+5O2![]() 4NO+6H2O 2SO2+O2
4NO+6H2O 2SO2+O2![]() 2SO3 2KClO3
2SO3 2KClO3![]() 2KCl+3O2
2KCl+3O2
4、放电:N2+O2![]() 2NO 3O2
2NO 3O2![]() 2O3
2O3
5、电解: 2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑ 2H2O
2NaOH+H2↑+Cl2↑ 2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
方法四、根据特征转化关系推断
知识准备:1、一般思路是找出特别的变化关系,用可能的几种情况试探,得出合理答案.2、掌握一些特别的连续变化关系
(1)![]()
①![]()
②![]()
③![]()
④![]()
(2)A—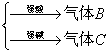
A为弱酸的铵盐:(NH4)2CO3或NH4HCO3;(NH4)2S或NH4HS;(NH4)2SO3、NH4HSO3
(3)形如![]() 的反应,中学化学里常见的有:
的反应,中学化学里常见的有:
![]()
3、注意几个典型转化关系
三角转化:
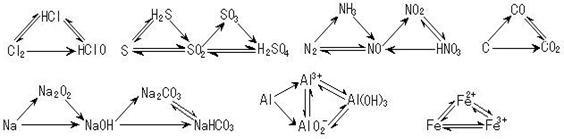
4、置换反应:
(1)金属→金属

(2)金属→非金属
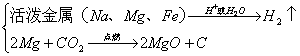
(3)非金属→非金属
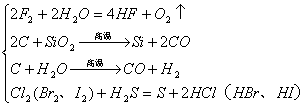
(4)非金属→金属
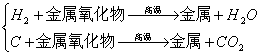
5、与碱反应产生气体
⑴
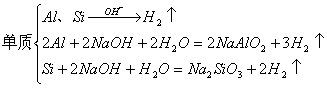
⑵铵盐:![]()
6、与酸反应产生气体
 ⑴
⑴
 ⑵
⑵
7、既能酸反应,又能与碱反应
Al、Al2O3、Al(OH)3、弱酸的酸式盐(NaHCO3、NaHSO3、NaHS等) 、弱酸的氨盐[NH4HCO3、(NH4)2CO3、NH4HSO3、 (NH4)2SO3、 (NH4)2S、NH4HS等]、氨基酸等;
8、与水反应产生气体
(1)单质
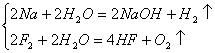
(2)化合物
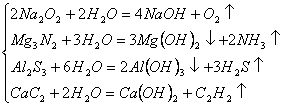
9、气体反应特征
(1)苍白色:H2在Cl2中燃烧; (2)蓝色:CO在空气中燃烧;
(3)淡蓝色:H2S、H2、CH4、CH3CH2OH、S等在空气中燃烧;
(4)明亮的蓝紫色:S在纯氧中燃烧; (5)金属的焰色反应
烟、雾
(1)在空气中形成白雾的:HCl、HBr、HI、NH3等气体及浓盐酸、浓硝酸;
(2) 相遇形成白烟或固体的:NH3+HCl、NH3+HBr、NH3+HNO3、H2S+SO2、H2S+Cl2;
(3) 燃烧时出现白色烟雾的:(P+Cl2);
(4) 燃烧时出现棕黄色烟的:(CuCl2)。
10、受热分解产生2种或3种气体的反应:
(1)铵盐
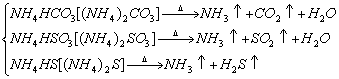
(2)硝酸盐
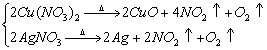
(3)硝酸:4HNO3==2H2O+4NO2↑+O2↑
(4)碱式碳酸铜:Cu(OH)2(CO3)2== CuO + 2CO2↑ + H2O
(5)碳酸氢盐:2NaHCO3![]() Na2CO3+H2O+CO2;Ca(HCO3)2
Na2CO3+H2O+CO2;Ca(HCO3)2![]() CaO+H2O+2CO2
CaO+H2O+2CO2
方法五、根据特殊工业生产推断
知识准备:重要工业生产反应
1、煅烧石灰石2、煅烧黄铁矿3、二氧化硫的催化氧化4、氨的催化氧化5、合成氨6、电解饱和食盐水7、工业制盐酸8、高炉炼铁9、工业制取漂粉精10、工业制水煤气11、硅酸盐工业
方法六、根据特征数据推断
知识准备:近两年计算型推断题成为高考热点之一,解这类题时要善于抓住物质转化时相对分子质量的变化(例CO→CO2,NO → NO2,SO2→SO3转化时分子中都增加1个氧原子,相对分子质量变化均为16);放出气体的体积或生成沉淀的量;化合物中各元素的含量;气体的相对密度;相对分子质量;离子化合物中离子个数比;反应物之间的物质的量比;电子总数;质子总数等重要数据。

- 全部评论(0)
