常见气体实验室制取装置
时间:2012-03-26 22:28 来源:未知 作者:陈功健 点击: 次 所属专题: 气体制备 实验室制取
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一. 三种典型的气体发生装置
根据制取气体的反应原理及反应条件,常见的三种典型装置有制取氧气、氢气、氯气的装置:
1. “固+固![]() 气体”型装置(如图1所示):凡是利用固体加热制取气体均可使用该套装置,如制取O2、NH3、CH4等。
气体”型装置(如图1所示):凡是利用固体加热制取气体均可使用该套装置,如制取O2、NH3、CH4等。
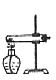
图1
(1)所需仪器:铁架台、铁夹、酒精灯、大试管、单孔橡胶塞、导气管等。
(2)注意事项:①试管口应略向下倾斜,以防止产生的水蒸气在管口冷凝后倒流而引起试管炸裂;②铁夹应夹在距试管口1/3管长处;③固体药品要在试管底部平铺开,加热时首先均匀预热,后集中加热药品部位,并逐步前移;④胶塞上的导管伸入不能过长,否则会妨碍气体的导出;⑤如用排水法收集气体,当停止制取气体时,应先从水槽中撤出导管,再熄灭酒精灯,以防止倒吸。
2. “固或液+液![]() 气体”型装置(如图2所示):凡是利用固体与液体或液体与液体加热制取气体均可使用该套装置,如制取Cl2、HCl、NO、CO等。
气体”型装置(如图2所示):凡是利用固体与液体或液体与液体加热制取气体均可使用该套装置,如制取Cl2、HCl、NO、CO等。
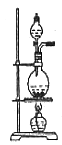
图2
(1)所需仪器:铁圈、铁架台、铁夹、酒精灯、石棉网、烧瓶、分液漏斗、双孔橡胶塞、导气管等。
(2)注意事项:①烧瓶应固定在铁架台上;②先把固体药品放入烧瓶中,然后再慢慢加入液体;③分液漏斗应盖上盖,注意盖上的小槽要对准分液漏斗颈上的小孔;④对烧瓶加热时要垫上石棉网。
3. “固+液→气体”型装置(如图3所示):凡是利用固体与液体反应不需加热制取气体均可使用该套装置,如制取H2、CO2、SO2、NO2、H2S、HF等。
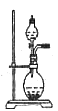
图3
(1)所需仪器:铁架台、铁夹、大试管、长颈漏斗、双孔橡胶塞、导气管等,或启普发生器(这类装置使用方便,随时使反应发生或停止)。
(2)注意事项:①在简易装置中长颈漏斗颈的下口应伸入液面以下,以防止生成的气体从长颈漏斗逸出;②加入的固体药品块状大小要适宜,如果太碎会落入底部的反应液中使反应无法停止,造成容器内压力过大导致长颈漏斗中的液体溢出;③加入反应液要适量;④最初使用时应待容器内原有的空气排净后再收集气体;⑤在导管口点燃H2等可燃性气体前,要先检验纯度。
二. 两种典型的气体收集装置
根据气体的水溶性和对空气的相对密度可选择排液法或排空气法收集:

图4
(1)排液法:其装置如图4所示。若气体难溶于水且不与水反应,则可用排水法收集(如H2、O2、No、CO等);若气体可溶于水但溶解度不大或与水能缓慢反应,则可用排饱和溶液法收集(如CO2可用排饱和NaHCO3溶液法收集,SO2可用排饱和NaHSO3溶液法收集,H2S可用排饱和NaHS溶液法收集,Cl2可用排饱和食盐水法收集等)。
(2)排空气法:凡不与空气反应且密度与空气相差较大的气体,均可用排空气法收集。若气体密度大于空气的密度,则用向上排空气法(装置如图5所示,可收集O2、Cl2、HCl、CO2、SO2、NO2、H2S等);若气体密度小于空气的密度,则用向下排空气法(装置如图6所示,可收集H2、NH3、CH4等)。用排空气法收集气体产物时,应在集气瓶口遮盖玻片或塞一团棉花,以防止被收集的气体在空气中扩散。
![]()
![]()
图5 图6
三. 一种常见的“一瓶多用”装置
如图7、8所示的装置有以下多种用途:
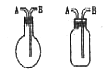
图7 图8
(1)用作排空气法收集气体:从A口进气可收集H2、NH3、CH4等密度比空气小的气体;从B口进气可收集O2、CO2、NO2、SO2等密度比空气大的气体。
(2)用作排液法收集气体:将瓶内充满水或合适的饱和溶液,从A口进气,B口排液,可收集H2、O2、CO2、SO2、H2S、Cl2等气体。
(3)用作洗气装置:在瓶内盛吸收液,从B口进气,A口出气,可用来净化或干燥气体。
(4)用作储气瓶:将瓶内充满水或合适的饱和溶液,气体从A口通入而储存;取用气体时,将B管接上自来水,使烧瓶中的气体从A管输出。
(5)用作量气装置:在B管后加一量筒,将瓶内充满水或合适的饱和溶液,从A口通入气体,便可测量气体体积。
(6)用作气体的反应容器:从A处通入密度较大的气体(如HCl),从B处通入密度较小的气体(如NH3),即成为反应器,可观察到有趣的现象。

- 全部评论(0)
