最全减压知识点总结
时间:2025-12-26 17:04 来源:未知 作者:化学自习室 点击: 次 所属专题: 减压蒸馏 减压过滤 实验与压强
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、减压蒸馏(减压蒸发)
在密闭的容器内,抽真空使液体处于一个大气压下的环境,从而降低水的沸腾温度,以此进行蒸发浓缩。
2.优点
①由于压力降低,溶液的沸点降低,能防止或减少热敏性物质的分解;
②增大传热温度差,强化蒸发操作;
③不断地排除溶剂蒸气,有利于蒸发顺利进行;
3.装置
旋转蒸发仪

4.高考实例
【例1】ClO2又称百毒净,可用于水的净化和纸张、纺织品的漂白。用如图所示装置(夹持装置和加热装置省略)制备ClO2并探究ClO2的某些性质。
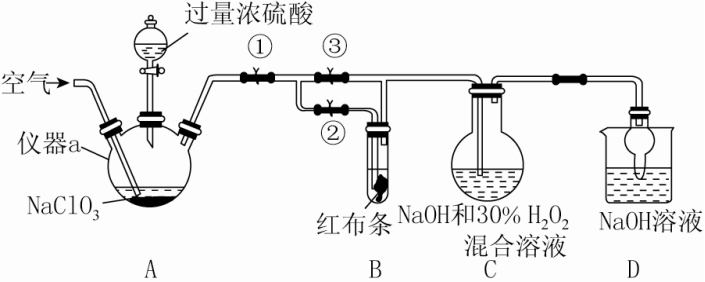
已知:①高氯酸:沸点90℃,浓度低于60%比较稳定,浓度高于60%遇含碳化合物易爆炸。
②饱和NaClO2溶液随温度变化情况:
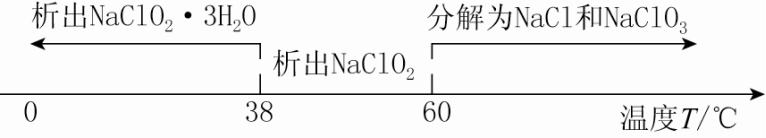
从装置C反应后的溶液中获得NaClO2晶体,需控温在38~60℃范围内进行减压蒸发结晶,采用减压蒸发的原因是减压可降低沸点,在较低温度下蒸发,避免晶体高温分解
二、减压蒸馏
1.原理
液体的沸点是指它的蒸气压等于外界大气压时的温度。所以液体沸腾的温度是随外界压力的变化而变化的。因而如用真空泵连接盛有液体的容器使液体表面上的压力降低,即可降低液体的沸点。这种在较低压力下进行蒸馏的操作称为减压蒸馏。
2.装置
减压蒸馏和常压蒸馏相比增加了减压系统,但并不仅是常压蒸馏加减压系统那么简单。
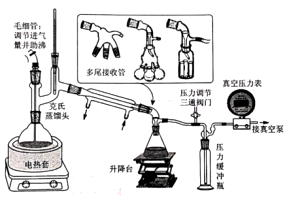
①采用克氏蒸馏头:真空状态下蒸馏,液体更容易发生液泛或暴沸,采用克氏蒸馏头可降低其发生的风险和后果。将毛细管插入蒸馏液体可调节进气量,一方面可控制调节真空度,另一方面可助沸(微量气体从液体里冒出微小的气泡,形成许多气化中心)。
加热与冷却:需根据低压下馏分的沸点进行选择。若馏分沸点很高,或为低熔点固体,可不用冷凝管,将蒸馏头支管直接与接收瓶相连。
②馏分的接收:低压状态下多个馏分的接收不易中断,应采用多尾接收管。
③玻璃器要耐真空,装置的密闭性良好。
④减压系统要有压力缓冲瓶,并配备三通阀门,以便与大气相通,防止泵液倒吸。
3.注意事项
结束减压蒸馏时先停热,待烧瓶冷却后再解除真空。解除真空时要先与大气相通,再关闭减压泵,防止发生倒吸现象。减压下与大气相通时要缓慢,突然通气会因压力猛烈而对蒸馏系统产生冲击造成事故。烧瓶未冷却时也不能突然放入大量空气,否则会使某些易于氧化的化合物突然接触大量氧气而发生爆炸事故。
4.优点
①降低物质的沸点,避免温度过高导致馏分被氧化
②在较低温度下蒸馏出产品,可以避免产品分解
③不需要高温加热,节省能源
④容器不需要耐高温
5.高考实例
【例2】(2020·江苏)实验室用氧化锌作催化剂、以乙二醇和碳酸氢钠为复合解聚剂常压下快速、彻底解聚聚对苯二甲酸乙二醇酯,同时回收对苯二甲酸和乙二醇。反应原理如下:
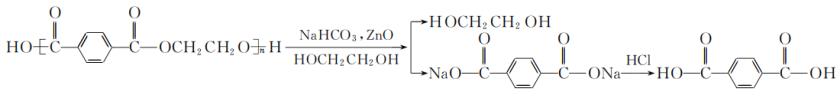
实验步骤如下:
步骤1:在题图1所示装置的四颈烧瓶内依次加入洗净的矿泉水瓶碎片、氧化锌、碳酸氢钠和乙二醇,缓慢搅拌,油浴加热至180 ℃,反应0.5 H。
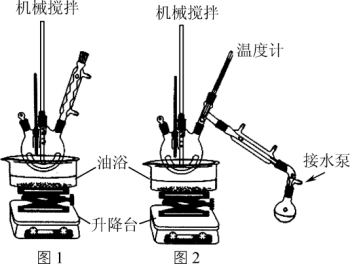
步骤2:降下油浴,冷却至160 ℃,将搅拌回流装置改为图2所示的搅拌蒸馏装置,水泵减压,油浴加热蒸馏。
步骤3:蒸馏完毕,向四颈烧瓶内加入沸水,搅拌。维持温度在60 ℃左右,抽滤。
步骤4:将滤液转移至烧杯中加热煮沸后,趁热边搅拌边加入盐酸酸化至pH为1~2。用砂芯漏斗抽滤,洗涤滤饼数次直至洗涤滤液pH=6,将滤饼摊开置于微波炉中微波干燥。
请回答下列问题:
步骤2中减压蒸馏的目的是降低蒸馏温度,防止引起副反应,蒸馏出的物质是乙二醇。
三、减压过滤(吸滤或抽滤)
1.原理与装置
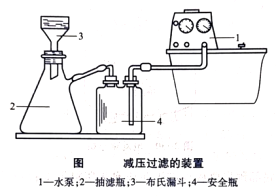
减压过装置如下图所示,利用水泵的负压原理将空气带走,从而使抽滤瓶内压力减小,在布氏漏斗内的液面与抽滤瓶内造成一个压力差提高了过滤的速度。
在连接水泵的橡胶管和抽滤瓶之间安装一个安全瓶,用以防止因关闭水阀或水泵后水流速度的改变引起水倒吸进入抽滤瓶将滤液沾污并冲稀。也正因为如此,在停止过滤时,应先从抽滤瓶上拔掉橡胶管然后才关闭水泵。
2.注意事项
①滤纸在减压下容易被抽破,因此必要时需要加厚;
②它不适用于胶状沉淀和颗粒太细的沉淀的过滤,胶状沉淀会透过滤纸,太细小的沉淀会板结在滤纸上。
3.优点
①固体和液体分离的比较完全,易分离
②滤出的固体容易干燥
③过滤和洗涤速度快
4.高考实例
【例3】利用氯碱工业中的固体废物盐泥[主要成分为Mg(OH)2、CaCO3、BaSO4,还含有少量NaCl、Al(OH)3、Fe(OH)3、Mn(OH)2等]与废稀硫酸反应制备七水硫酸镁,既处理了三废,又有经济效益。其工艺流程如图1所示:
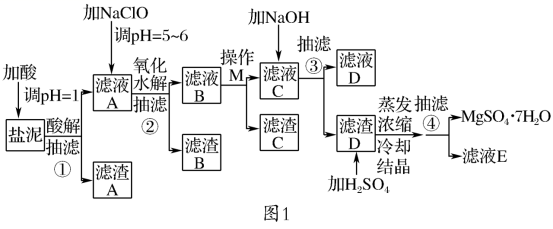
已知:
I)部分阳离子以氢氧化物形式完全沉淀时溶液的pH如表所示。
沉淀物 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
pH(完全沉淀) | 10.02 | 8.96 | 3.20 | 4.70 | 11.12 |
II)两种盐的溶解度随温度的变化(单位为g/100 g 水)如图2所示。
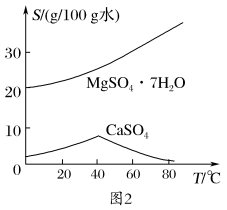
本工艺流程多次用到抽滤操作,优点是过滤速度快、;滤渣更干燥。
抽滤①所得滤渣A的成分为BaSO4和CaSO4;
抽滤②所得滤渣B的成分为MnO2、Fe(OH)3和Al(OH)3;
抽滤③所得滤液D中主要阳离子的检验方法是焰色反应。
四、真空干燥
1.真空干燥器原理
真空干燥器如下图,干燥器顶部装有带旋塞开关的出气口,由此处抽气后,可使干燥器内压力降低并趋于真空因而可以提高干燥效率。
2.装置

3.真空恒温干燥箱原理
对于一些在烘箱或一般干燥器中干燥都未能满足要求的样品,可用真空恒温干燥箱(下图)干燥。其优点是干燥效率高,能除去晶体中的结晶水或结晶醇,同时由于装置内抽真空,几乎没有氧气的存在,因为也可以防止物质被氧化。经过纯化准备进行分析鉴定(元素定量、波谱鉴定等)的样品均需在真空恒温干燥器中真空干燥2H以上,彻底除去样品中可能存在的有机溶剂结晶水或结晶醇。
4.优点
可以隔绝空气防止物质与空气中某些气体发生化学反应而破坏物质
5.高考实例
【例4】(2019·湖北省黄冈中学适应性考试)氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末,微溶于水不溶于乙醇及稀硫酸。以铜矿粉(含Cu2S、Cu2O、CuS及少量
FeS等)为原料制取的工艺流程如下:
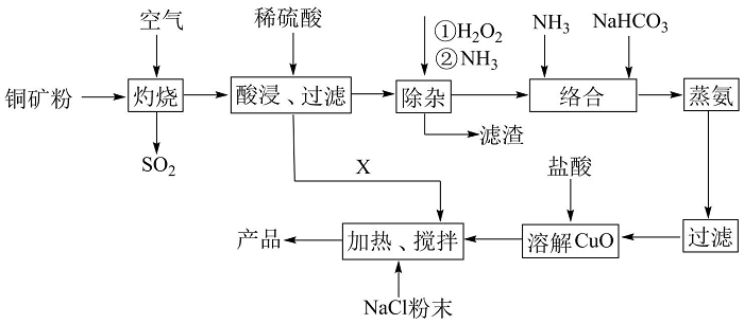
已知:FeS高温条件下与氧气生成FeO;Cu2S高温条件下与氧气生成Cu2O;Cu2O在酸性条件下会发生歧化反应。回答下列问题:
洗涤CuCl晶体后并在真空干燥机内于70℃干燥2小时,冷却,密封包装。于70℃真空干燥的目的是加快乙醇和水的挥发,防止CuCl被空气氧化。

- 全部评论(0)
