电解质的强弱是如何划分的?
时间:2012-05-16 08:39 来源:未知 作者:爱莉 点击: 次 所属专题: 弱电解质判断
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
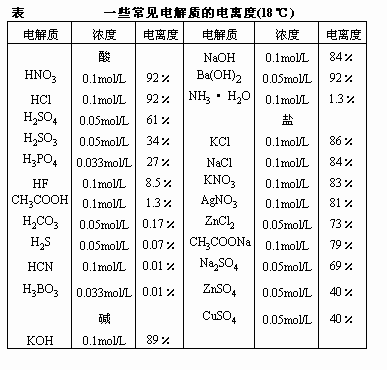
电解质的强弱没有绝对的严格的标准,一般是按电离度的大小来划分的。浓度0.1mol/L的溶液,电离度在30%以上的算做强电解质,如强酸、强碱和大多数的盐。电离度在5%以下的为弱电解质,如弱酸、弱碱。电离度在5~30%的为中强电解质,如中等强度的酸和碱。这种划分只是相对的粗略的。
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
还没有评论,快来抢沙发吧!
