怎样分析竞争反应的先后?
时间:2015-01-28 16:04 来源:未知 作者:张瀚 点击: 次 所属专题: 反应先后
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
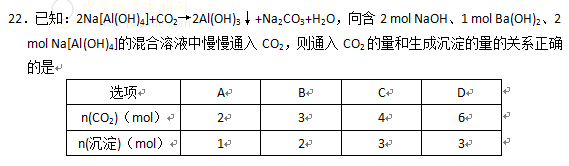
答案:反应顺序为:先碳酸钡,再碳酸钠;再氢氧化铝;再碳酸氢钠,再碳酸氢钡。
解析:氢氧根和二氧化碳先反应,生成碳酸根的同时就和钡离子反应了,这个反应总起来就相当于和氢氧化钡反应了,至于是谁的氢氧根无所谓了。
总结:同性质的物质之间的竞争反应,一般存在的规律是:谁强谁先反应(反应物角度分析);谁弱谁先生成(生成物角度分析)。
像这种竞争反应的先后问题,理科的思路很简单,就是尝试法。比如你的问题是三种物质中谁先与酸反应,你可以随意选择一种物质与盐酸反应,反应的产物与其它物质能否共存,能共存说明你选择对了,不共存说明你选择错了,重新选择就对了。
再如:Mg(OH)2、AlO2-溶液中滴入盐酸,氢离子为什么先与AlO2-反应?若先与 Mg(OH)2反应,则生成的Mg2+又可与AlO2-发生双水解,所以只能先与后者反应。
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
还没有评论,快来抢沙发吧!
