铝元素重要图象剖析
时间:2016-01-18 22:53 来源: 作者:杨董 点击: 次 所属专题: 铝反应图像
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
现将与铝元素相关的重要图象分析如下,供参考。
1. 向AlCl3溶液中滴加NaOH溶液直至过量
原理:![]() (先)
(先)
![]() (后)
(后)
现象:先沉淀后溶解。
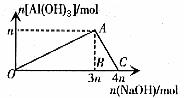
图1
图象1的特点:图象通过坐标原点,且横坐标上的比值为“3:
2. 向NaOH溶液中滴加AlCl3溶液直至过量
原理:![]() (先)
(先)
![]() (后)
(后)
现象:开始没有沉淀产生,中间产生沉淀,且最终沉淀不溶解。
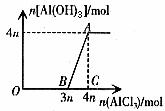
图2
图象2的特点:横坐标上的比值为“3:
3. 向NaAlO2溶液中滴加HCl溶液直至过量
原理:![]() (先)
(先)
![]() (后)
(后)
现象:先沉淀后溶解。
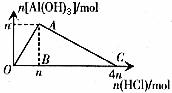
图3
图象3的特点:图象通过坐标原点,横坐标上的比值为“1:
4. 向盐酸溶液中滴加NaAlO2溶液直至过量
原理:![]() (先)
(先)
![]() (后)
(后)
现象:首先没有沉淀,中间产生沉淀,且最终沉淀不溶解。
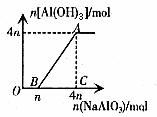
图4
图象4的特点:
横坐标上的比值为“1:
5. 向NaAlO2溶液中通入CO2气体至过量
原理:![]() (少量)
(少量)![]()
![]() (足量)
(足量)![]()
现象:产生的沉淀逐渐增多,且最终沉淀不溶解。
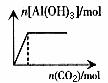
图5
图象5的特点:图象通过坐标原点,先上升后平行(平行于横坐标)。
6. 向AlCl3溶液中滴加氨水
原理:![]()
现象:产生沉淀逐渐增多,达到最大值后保持不变。
图象6的特点:图象通过坐标原点,先上升后水平(平行于横坐标),A点坐标为(3n,n)。
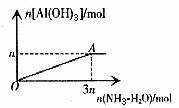
图6
7. 向AlCl3和MgCl2溶液中滴加NaOH溶液
原理:![]() ;
;
![]() (先)
(先)
![]() (后)
(后)
现象:产生沉淀至最大值后,沉淀部分溶解,最终还有沉淀存在。
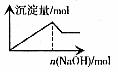
图7
图象7的特点:图象通过坐标原点,且图象中间有2个转折点。
8. 向AlCl3溶液中滴加NaAlO2溶液
原理:![]()
现象:产生沉淀至最大值后沉淀不溶解。
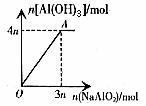
图8
图象8的特点:图象通过坐标原点,且A点坐标为(3n,4n)
9. 向NaAlO2溶液中滴加AlCl3溶液
原理:![]()
现象:产生沉淀至最大值后沉淀不溶解。
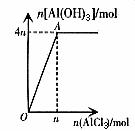
图9
图象9的特点:图象通过坐标原点,且A点坐标为(n,4n)。
10. 向含![]() 混合液滴加NaOH溶液直至过量
混合液滴加NaOH溶液直至过量
原理:![]() :
:![]()
B→A:![]()
A→D:![]()
现象:开始没有沉淀,中间产生沉淀,最后沉淀完全溶解。
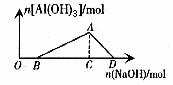
图10
图象10的特点:OB的长短由![]() 来决定。线段长度BC:CD:AC=3:1:1。
来决定。线段长度BC:CD:AC=3:1:1。
11. 向含OH-和AlO2-混合溶液中滴加盐酸直至过量
原理:O→B:![]()
B→A:![]()
A→D:![]()
现象:开始没有沉淀,后来产生沉淀,最后沉淀完全溶解。
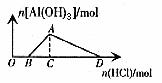
图11
图象11的特点:线段长度BC:CD:AC=1:3:1。OB的长短由![]() 决定。
决定。
12. 向含H+、Mg2+、Al3+的混合溶液中加入NaOH溶液至过量
原理:O→B:![]()
B→A:![]()
![]()
A→E:![]()
现象:开始没有沉淀,中间产生沉淀,最后沉淀部分溶解。
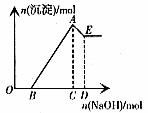
图12
图象12的特点:OB的长短由![]() 来决定,CD的长短由
来决定,CD的长短由![]() 来决定。
来决定。
13. 向OH-、AlO2-、Mg(OH)2混合物中滴加盐酸至过量
原理:O→B:![]()
B→C:![]()
C→D:![]()
![]()
现象:开始就存在沉淀且不变,中间沉淀增加,最后沉淀完全溶解。
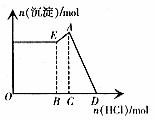
图13
图象13的特点:OB的长短由![]() 来决定,BC的长短由
来决定,BC的长短由![]() 来决定。
来决定。

- 全部评论(0)
