在以盐桥搭建的Cu-Zn原电池中,Zn不与ZnSO4反应,什么会失电子?
时间:2017-04-26 09:51 来源:未知 作者:张红 点击: 次 所属专题: 盐桥 双液电池
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
盐桥搭建的Cu-Zn原电池如下:
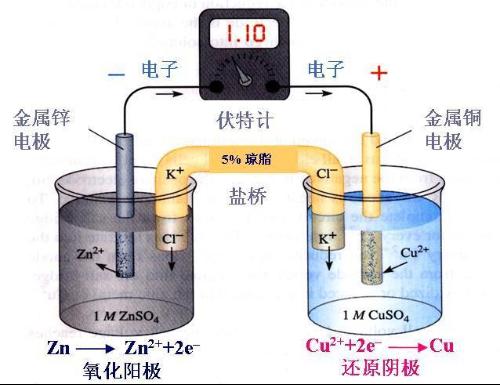
盐桥铜锌原电池
组成原电池的三个条件为:
1.电极材料由两种金属活动性不同的金属或由金属与其他导电的材料(非金属或某些氧化物等)组成。
2.两电极必须浸泡在电解质溶液中,并形成闭合回路。
3.还要有一个自发形成的氧化还原反应。
(以上三点有时候也分成四点)
在以上的三个条件影响下,对照上面用盐桥搭建的Cu-Zn原电池装置图,学生都不解了。Zn极与它浸泡的电解液ZnsO4不反应,Cu极与它浸泡的CuSO4也不反应,也就是说没有一个自发形成的氧化还原反应了,也就没有满足构成原电池的三个条件了。
课本的解释只是说利用盐桥使得两边的电解液保持电中性,从而保证电子可以源源不断地从Zn极流向Cu极。但学生更不解了,Zn极与它浸泡的电解液ZnsO4不反应,Zn就不会因为失电子而成为Zn2+了,那就不会使ZnsO4溶液中因为Zn2+的增多而带电性;同理,Zn不失电子,Cu极中CuSO4中的Cu2+也不会因为从Cu极上得到电子析出,而使CuSO4溶液因为Cu2+减少而带负电。
对于学生这样的疑惑,我非常理解。但按照高中阶段的要求,还是只能从电池的总反应:Zn + Cu2+= Zn2++ Cu 这个自发的氧化还原反应去理解,而盐桥,则是导致Zn、Cu2+这两个不在一个溶液体系环境中的物质(把Cu2+也说成是物质可能不太恰当)发生反应的原因。
如果真要解释得切底点,那就必须从大学的电极电势去解释了。
原电池中,电极不一定要和电解质溶液反应(也就是说,原电池的这个自发形成的氧化还原反应,不一定是电极和电解质反应。),只要作为两极的材料具有电势差即可。
因为锌是金属晶体,内部每时每刻都在进行着自由电子离开原子核与靠近原子核的过程。该过程是可逆的,每时每刻都有电子靠近、远离原子核。如果把锌板插入硫酸锌、铜板插入硫酸铜,电子远离锌原子核后,由于铜原子核得电子能力更强,所以电子由锌板通过导线到达铜板与硫酸铜中的铜离子结合,成为单质铜。实际上是锌与硫酸铜反应!这也是常说的电极电势差而导致电子的转移。

- 全部评论(0)
(123456789) 评论 href="/plus/view.php?aid=13215">在以盐桥搭建的Cu-Z:真的解决了我的燃眉之急,谢谢
(2461199682) 评论 href="/plus/view.php?aid=13215">在以盐桥搭建的Cu-Z:已打赏,真的是个困扰,这样一说舒服多了
 1852179630@qq.com 评论
href="/plus/view.php?aid=13215">在以盐桥搭建的Cu-Z:可以再详细点吗,大致懂了
1852179630@qq.com 评论
href="/plus/view.php?aid=13215">在以盐桥搭建的Cu-Z:可以再详细点吗,大致懂了
 1852179630@qq.com 评论
href="/plus/view.php?aid=13215">在以盐桥搭建的Cu-Z:可以再详细点吗,大致懂了
1852179630@qq.com 评论
href="/plus/view.php?aid=13215">在以盐桥搭建的Cu-Z:可以再详细点吗,大致懂了
