第十五讲:有机物的化学性质(二)烃的化学性质
时间:2021-05-27 10:32 来源:高中化学教学研究 作者:张德金 点击: 次 所属专题: 有机物化学性质 烃类
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
除了醇之外,其它各种简单有机物的特殊反应都很少,掌握起来并不难。
有机物的化学性质,是学懂有机物的最重要的一个环节。有机物的化学分离提纯,有机物的制取,有机合成流程的看懂与设计,各种有机实验等,都离不开有机物的化学性质。
有机物的化学性质的不同,是因为有机物的结构的不同,而结构常常与官能团有关。
一、有机物从单个官能团的角度分类
首先分为两大类,一类是只含有C、H两种原子的有机物叫烃,另一类是除C和H外,也含有其它元素的有机物叫烃的衍生物。
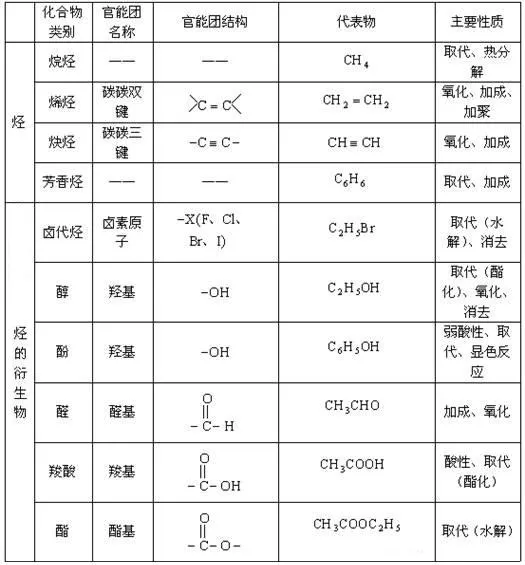
烃包括烷、烯、炔、芳香烃等。
烃的衍生物包括含卤素原子的卤代烃,含氧的醇、酚、醛、酸、酯、醚、酮,含氮的有机物,含硫的有机物,含磷的有机物,含更多种元素的有机物等。
二、烃的化学性质
(常见的烃的物理性质中注意两点,都难溶于水,都比水的密度小。)
所有的烃都有一个共同的化学性质,可燃性。石油的主要成分是饱和烃。天然气的主要成分是甲烷。它们都是重要的燃料和有机工业原料。
CxHy+[x+(y/4)]O2→点燃→xCO2+y/2H2O
甲烷的燃烧现象为淡蓝色火焰,乙烯为明亮火焰伴有黑烟,乙炔和苯为明亮火焰伴有浓烟。随着含碳量的增大,烟的浓度变大。
有机反应的反应条件的书写,如果知道,就写对应的反应条件。如果不知道,一般写催化剂、加热、加压等。气体反应会需要加压,有机反应的加热温度不会很高,因为多数有机物的稳定性低。
1、烷:每个C的周围是四个单键,其余为H。
(1)取代反应:与卤素单质反应。
①化学性质由周围有4个单键的C上的H体现。

有机物中只要有这样的H就有和烷一样的化学性质。
②甲烷与氯气的取代:CH4+Cl2→光照→CH3Cl+HCl
反应会继续进行,直到生成CCl4为止。
注意的是,此反应与复分解反应的最大区别是,不分反应阶段,只要反应一开始,四种有机产物CH3Cl、CH2Cl2、CHCl3、CCl4都存在。除非氯气过量,理论上有机产物只有CCl4。
(2)分解反应:多碳烷会分解。(石油的裂化裂解)
C16H34→催化剂加热加压→C8H18+C8H16(裂化:产生汽油)
C4H10→催化剂加热加压→C2H6+C2H4(裂解:产生有机化工原料)
反应原理与消去反应类似。
2、烯:含有碳碳双键(![]() )的官能团。
)的官能团。
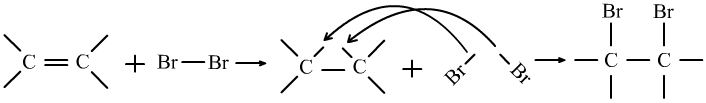
(1)加成反应:碳碳双键中的一个键不稳定,易断裂。
①乙烯的加成:CH2=CH2+Br2→CH2BrCH2Br
烯可以与很多物质发生加成反应。卤素单质、O2、HCl、H2O等。但与卤素单质Cl2、Br2等反应不需要条件。与O2、HCl、H2O等反应需要条件。
CH2=CH2+H2O→催化剂加热加压→CH3CH2OH
②不对称的烯烃与极性分子加成时,会产生同分异构体。
CH3-CH=CH2+HCl→催化剂→CH3-CHCl-CH3或CH3-CH2-CH2Cl
(2)二烯的1,4-加成和1,4-加聚
这儿的二烯特指的是有“-C=C-C=C-”结构的二烯,它能发生一种特殊的加成方式:1,4-加成和1,4-加聚。
CH2=CH-CH=CH2+Br2→CH2Br-CH=CH-CH2Br
nCH2=CH-CH=CH2→催化剂→-[-CH2-CH=CH-CH2-]n-
1,4-加聚在合成橡胶时是非常重要的一种反应。加聚后得到的高分子再加入一些化合物进行纵向加聚,就可以得到既有硬度又有韧性的橡胶。
(3)氧化反应:与酸性KMnO4反应。碳碳双键易被氧化断裂。
烯的氧化是从-C=C-中间断开,形成CO2、酸或酮:CH2=生成CO2,R-CH=生成R-COOH,RR’C=生成R![]() R’。
R’。
例如,5CH2=CH2+12KMnO4+18H2SO4→10CO2+6K2SO4+12MnsO4+28H2O
CH3CH=CH2+2KMnO4+3H2SO4→CH3COOH+CO2+K2SO4+2MnsO4+4H2O
5(CH3)2C=CHCH3+6KMnO4+9H2SO4→5CH3![]() CH3+5CH3COOH+3K2SO4+6MnsO4+9H2O
CH3+5CH3COOH+3K2SO4+6MnsO4+9H2O
有机物发生氧化反应或还原反应是得失电子数的计算方法是:
每增加一个O,失2e-,每减少一个H,失1e-。
每减少一个O,得2e-,每增加一个H,得1e-。
(4)烯的加聚反应(乙烯之间的连续加成)
nCH2=CH2→催化剂→-[- CH2-CH2-]n-


3、炔:含有碳碳三键(-C≡C-)的官能团。
(1)加成反应:碳碳三键中有两个键不稳定,都易断裂。
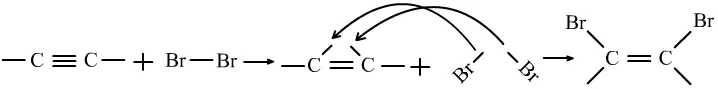
CH≡CH+Br2→CHBr=CHBr
CHBr=CHBr +Br2→CHBr2-CHBr2
(2)氧化反应:与酸性KMnO4反应。碳碳三键易被氧化断裂。
烯的氧化是从-C≡C-中间断开,形成CO2、酸:CH≡生成CO2,R-C≡生成R-COOH。
例如,5CH3C≡CH+8KMnO4+12H2SO4→5CH3COOH+5CO2+4K2SO4+8MnSO4+12H2O
(3)加聚反应:有的可以生成导电塑料。
nCH≡CH→催化剂→-[- CH=CH-]n-
4、芳香烃:含有苯环的特殊结构。
芳香烃注意的是苯环结构用的是键线式,苯环的上C如果没有侧链,则有一个H,如果有侧链,则没有H。
(1)取代反应:芳香烃的取代反应是苯环上的H所具有的性质。
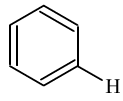
苯与溴的取代: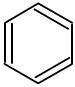 +Br2→FeBr3→
+Br2→FeBr3→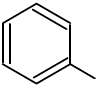 Br+HBr
Br+HBr
苯与硝酸的硝化: +HNO3→浓H2SO4Δ→
+HNO3→浓H2SO4Δ→ NO2+H2O(HNO3以HO-NO2的方式反应)
NO2+H2O(HNO3以HO-NO2的方式反应)
甲苯与硝酸的硝化: CH3+3HNO3→浓H2SO4Δ→
CH3+3HNO3→浓H2SO4Δ→ +3H2O
+3H2O
苯的取代反应与烷的取代反应属于不同的化学性质。
(2)加成反应:芳香烃的加成反应是因为苯环上的不饱和的碳碳键所具有的性质。但这种键既不是单键,也不是双键。所以,苯既不能像烷一样和卤素单质在光照下发生取代反应,也不能像乙烯一样被氧化,发生加聚反应或和氯气在常温下加成。
![]() +3H2→催化剂Δ→
+3H2→催化剂Δ→![]()
(3)氧化反应:当苯环连有侧链时,跟苯环直接相连的C上的H变得活泼,易被氧化,且无论侧链长短,其氧化产物中都有类似于苯甲酸的产物。如甲苯、均能使酸性高锰酸钾溶液褪色。
苯不能被酸性KMnO4氧化。甲苯、乙苯能。
5![]() CH3+6KMnO4+9H2SO4→5
CH3+6KMnO4+9H2SO4→5![]() COOH+3K2SO4+6MnSO4+14H2O
COOH+3K2SO4+6MnSO4+14H2O
5![]() CH2CH3+12KMnO4+18H2SO4→5
CH2CH3+12KMnO4+18H2SO4→5![]() COOH+5CO2+6K2SO4+12MnSO4+28H2O
COOH+5CO2+6K2SO4+12MnSO4+28H2O
跟苯环直接相连的C上没有H时,不被氧化。
【练习】
1、写出下列反应(注意书写反应条件)
(1)一分子的甲烷和三分子的氯气的反应: 。
(2)CH3CH=CHCH3的加聚反应: 。
(3)(CH3)2C=CH2与酸性KMnO4(H2SO4)反应: 。
(4)乙炔与酸性KMnO4(H2SO4)反应: 。
(5)甲苯与硝酸的硝化反应: 。
(6)甲苯与酸性KMnO4(H2SO4)反应: 。
(7)甲苯与H2反应: 。
2、回答下列问题。
(1)一分子的乙烷和三分子的氯气反应时,有机反应产物有哪几种。
(2)CH3CH2CH=CH2与HBr反应时,有机反应产物有哪几种。
(3)(CH3)2C=CHCH3与酸性KMnO4(H2SO4)反应时,有机反应产物有哪几种。
【练习答案】
1、(1)CH4+3Cl2→光照→CHCl3+3HCl。
(2)nCH3CH=CHCH3→催化剂→-[-CH(CH3)-CH(CH3)-]n-。
(3)5(CH3)2C=CH2+8KMnO4+12H2SO4→5CH3![]() CH3+ 5 CO2+4K2SO4+8MnSO4+17H2O
CH3+ 5 CO2+4K2SO4+8MnSO4+17H2O
(4)CH≡CH+2KMnO4+3H2SO4→2CO2+K2SO4+2MnSO4+4H2O
(5)
![]() CH3+3HNO3→浓H2SO4Δ→
CH3+3HNO3→浓H2SO4Δ→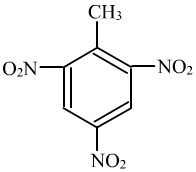 +3H2O
+3H2O
(6)
5![]() CH3+6KMnO4+9H2SO4→5
CH3+6KMnO4+9H2SO4→5![]() COOH+3K2SO4+6MnSO4+14H2O
COOH+3K2SO4+6MnSO4+14H2O
(7)
![]() CH3+3H2→催化剂Δ→
CH3+3H2→催化剂Δ→![]() -CH3
-CH3
2、(1)CH3CCl3、CHCl2CH2Cl(写成CCl3CH3、CH2ClCHCl2也可以)
(2)CH3CH2CH2CH2Br、CH3CH2CHBrCH3
(3)CH3![]() CH3、CH3COOH
CH3、CH3COOH

- 全部评论(0)
