氧化还原反应的发生条件及反应规律
时间:2016-03-25 10:03 来源:未知 作者:张红 点击: 次 所属专题: 氧化还原反应规律
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
(1)氧化剂的氧化能力必须大于氧化产物的氧化能力;还原剂的还原能力必须大于还原产物的还原能力。
常用氧化剂氧化能力和还原剂还原能力按顺序排列如下:
![]()
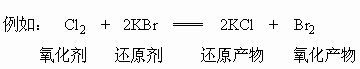
因为氧化能力Cl2>Br2,还原能力Cl-<Br-,所以反应能发生。反之,则不能发生。如Cu2+与Fe2+就不能发生反应,因Fe2+对应的氧化态为Fe3+,而Fe3+氧化性强于Cu2+,故Cu2+不能氧化Fe2+。
(2)同种元素不同价态物质间的氧化还原反应,高价态物质与低价态物质间需有中间价态物质存在,氧化还原反应才能发生。
![]() ,
,
Fe+FeCl2≠,
![]()
(3)同种元素不同价态物质间的氧化还原反应,氧化剂被还原到的价态不能低于还原剂被氧化到的价态(即遵循价态“归中”规律)
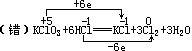 ,
,
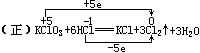
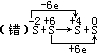 ,
,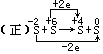
(4)氧化还原反应的邻位价态规律:氧化还原反应发生时,其价态一般变为邻位价态。
![]() ,
,![]()
(5)反应条件对氧化还原反应的影响:
①反应物浓度对氧化还原反应的影响
浓度大时氧化剂氧化性强,还原剂的还原性也强,如MnO2与浓盐酸反应才能生成Cl2,与稀盐酸不反应。再如:Cu跟浓H2SO4能发生氧化还原反应,而Cu跟稀H2SO4不反应。
②反应体系酸碱性的影响:
一般酸性条件下,含氧酸盐的氧化性比在碱性和中性环境中强。
![]() ,
,
KMnO4+NaCl(水溶液)≠
![]()
![]()
![]()
![]() 还原反应,但当向溶液中加入稀H2SO4后,很快产生淡黄色沉淀,即
还原反应,但当向溶液中加入稀H2SO4后,很快产生淡黄色沉淀,即
![]()
③温度对氧化还原反应的影响:
温度愈高,则氧化剂的氧化性愈强;还原剂的还原性也愈强。因此许多氧化还原反应的发生条件,需要加热,因这样可以增强反应物的氧化性与还原性。如CuO与H2反应需加热,因温度高时,CuO的氧化性增强,H2的还原性增强,容易反应,另外升高温度可以加快化学反应速率。又如CO、C还原某些金属氧化物均需加热,道理亦如此。
(6)氧化剂、还原剂的强弱与反应产物的关系:
同种还原剂,强氧化剂得到高价化合物,弱氧化剂,得到低价化合物,
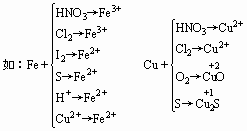
同种氧化剂,强还原剂得到低价化合物,弱还原剂得到高价化合物。
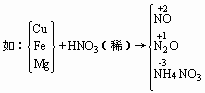

- 全部评论(0)
(1804609346) 评论 href="/plus/view.php?aid=12268">氧化还原反应的发生:真好,对高中化学帮助不少
