平均摩尔电子质量法
时间:2007-12-25 09:20 来源: 作者:爱莉 点击: 次 所属专题: 平均值法
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
“平均摩尔质量”法无法求解选项由“异价”金属组成的混合物的选择题,此类题需用“平均摩尔电子质量法”求解.
概念1 摩尔电子质量(E):某物质在反应中转移1摩尔电子所引起的质量改变。通常指在反应中提供单位物质的量的电子所需要的物质的质量。 单位:克/摩尔电子(g/mol•e)
概念2 平均摩尔电子质量(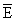 ):某混合物在反应中共转移1摩尔电子所引起的质量改变。单位:克/摩尔电子(g/mol•e)
):某混合物在反应中共转移1摩尔电子所引起的质量改变。单位:克/摩尔电子(g/mol•e)
例1、有两种金属混合粉末15克,加入足量的稀盐酸充分反应后,得到11.2升氢气(标况),则下列各组金属中肯定不能构成上述混合物的是(AC)
A、Mg、Al B、Mg、Al C、Cu、Zn D、Al、Fe
[巧解] H2~2e,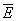 =
=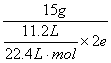 =15(g/mol•e)
=15(g/mol•e)
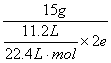 =15(g/mol•e)
=15(g/mol•e)金属单质的摩尔电子质量(在数值上)=原子量÷金属在该反应中所表现出的化合价。各金属的E值为:
Al: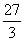 =9,Mg:
=9,Mg: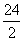 =12,Fe:
=12,Fe: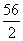 =28,Zn:
=28,Zn: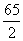 =32.5;不反应金属的E值可认为是+∞。
=32.5;不反应金属的E值可认为是+∞。
不能满足“E小<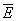 <E大”的选项A、C,即为符合题意的答案。
<E大”的选项A、C,即为符合题意的答案。
顺便指出,摩尔电子质量值越小的金属,其产生H2的能力就越强。将此观念应用到有关金属与酸反应及“托盘天平是否保持平衡”等问题中去,能使问题大为简化。
[练习1] 将下列各组中两种金属的混合物3g投入水中,收集到标准状况下H21.12L。不可能构成此种混合物的是(B)
A、Rb和Na B、Rb和K C、Na和Cu D、K和Na
[练习2] Na、Mg、Al、Fe四种金属中的两种组成的混合物12g,与足量的盐酸反应产生0.5g氢气,则混合物中一定含有的金属是(D)
A、Na B、Mg C、Al D、Fe
[练习3] 将Mg、Al和Fe的单质分别投入质量相等的稀硫酸中(稀硫酸过量)。反应结束后,各溶液的质量相等,则投入的Mg、Al、Fe三者的质量关系是(A)
A、Al>Mg >Fe B、Mg > Al >Fe C、Fe >Mg > Al D、Al=Mg =Fe
(责任编辑:化学自习室)

说点什么吧
- 全部评论(0)
还没有评论,快来抢沙发吧!
